随着现代社会生态环境的持续变化以及生活方式的转变,中国育龄人群的生殖健康正面临日益严峻的挑战,截至2020年,中国不孕症患病率进一步上升至17.6%[1]。女性不孕症是指35岁以下妇女有规律、未避孕性生活12个月以上未怀孕,或者35岁以上妇女6个月未怀孕[2]。因输卵管阻塞、粘连、积液引起输卵管通畅度异常改变导致的女性不孕称为输卵管性不孕[3]。在中国女性不孕症中,输卵管因素约占25%~35%,是女性不孕的主要原因之一[4]。输卵管炎症没有及时治疗就容易引发子宫内膜炎、输卵管脓肿、卵巢炎,导致输卵管性不孕或宫外孕。控制炎症是治疗输卵管性不孕的关键。妇科手术、宫内节育器(intrauterine device,IUD)的放置、不洁性生活史、邻近器官炎症都会导致输卵管炎性不孕,现该病发病率呈上升趋势[5]。现代医学手术治疗输卵管性不孕见效迅速,但难以避免术后子宫及附件发生出血、感染、粘连,产生腹痛、头晕、发热、阴道流血等副作用;药物治疗以头孢类抗生素、阿奇霉素联合甲硝唑等抗感染为主,但容易复发影响女性正常生活。
圆柱瘤蛋白(cylindroma protein,CYLD)是一种去泛素化酶,在炎症反应、免疫、肿瘤抑制等生理过程中发挥重要作用[6〗,其可以通去泛素化稳定YAP蛋白抑制前列腺癌细胞增殖[7]。TBK1通过CYLD磷酸化调节细胞凋亡,控制TNF介导的炎症[8]。巨噬细胞TXNIP缺乏会增强CYLD活性并激活NRF2-OASL1信号传导,诱发肝脏的炎症与损伤[9]。目前尚未有研究明确CYLD与输卵管炎性不孕的关系。肿瘤坏死因子受体相关因子6(TRAF6)是一种核心接头蛋白,作为IL-1受体、TNF-α受体和Toll样受体超家族的主要传导子,介导NF-κB(nuclear factor kappa-B,NF-κB)信号通路。NF-κB信号通路是重要的炎症通路,通过NF-κB的核移位促进炎症因子的转录,进而介导炎症[10]。泛素化是一种重要且丰富的翻译后修饰,通过76个氨基酸泛素(Ub,一种泛素分子)肽与底物蛋白的偶联发生。其中,TRAF6依靠K63连接的泛素链来激活下游信号通路称为泛素化。去泛素化是指CYLD可以从TRAF6中识别并去除K63特异性泛素链,影响蛋白之间的相互作用和细胞信号识别,抑制其泛素化从而限制其活性[11]。CYLD的缺失或下调导致细胞内泛素化水平过度升高,而过度泛素化促进了NF-κB信号通路的激活,导致炎症的发生[12]。炎症水平的升高会引起输卵管充血增粗、水肿、积液,降低输卵管上皮细胞活性,减缓输卵管正常蠕动,增加输卵管性不孕、宫外孕的风险。据此推测,CYLD可能参与调控输卵管炎性不孕,CYLD高表达可以抑制TRAF6泛素化,从而抑制NF-κB活化、减轻炎症。
材料与方法
1.动物:性成熟但未交配生育的SPF级雌性SD大鼠,体重250~300 g,8~10周龄,购自中国医学科学院实验动物研究所,生产许可证号为SCXK(湘)2019-0004。动物饲养环境是温度22~25 ℃,湿度30%~70%,昼夜交替,自由饮食饮水。
2.主要试剂:UB(10201-2-AP,美国proteintech)、NF-ΚB(66535-1-Ig,美国proteintech)、TRAF6、p-NFkB、IkBα、P-IkBα(ab137452,ab76302,ab32518,ab133462,英国abcam)、胰酶消化液(AWC0232,abiowell)、胎牛血清(10099141,Gibco)、双抗(青链霉素)(AWH0529a,abiowell)、PBS(AWC0409,abiowell)、IL-1β(JL20884,江莱生物)、IL-8(ml002885,上海酶联生物)、IL-6、TNF-α(CSB-E04640r、CSB-E11987r,武汉华美生物工程有限公司)、RIPA裂解液(P0013B,中国上海碧云天)、蛋白酶抑制剂(583794,中国北京金泰宏达)、蛋白磷酸酶抑制剂(P1260,中国北京普利莱)。
3.仪器:台式高速冷冻离心机(H1650R,湖南湘仪实验室仪器开发有限公司)、全自动酶标洗板机、多功能酶标分析仪(PW-812、MB-530,深圳市汇松科技发展有限公司)、电热恒温培养箱(DHP-500,北京市永光明医疗仪器有限公司)、台式冷冻离心机(H1650R,中国湖南湘仪)、电泳仪、转膜仪(DYY-6C、DYCZ-40D,中国北京六一)、旋涡混合器(GL-88B,中国江苏其林贝尔)、磁力搅拌器、精密PH计(JB-13、PHS-3C,中国雷磁)、生物样品均质仪(BioPrep-24,中国杭州奥盛)。
4.大鼠输卵管上皮细胞分离培养:给大鼠吸入过量麻醉(2%的戊巴比妥钠0.5 mL)然后处死,取出输卵管放入5 mL HBSS的diss中,在解剖镜上去除组织上的脂肪和卵巢。在超净台上,用HBSS把输卵管洗净,在diss中用眼科剪把组织剪碎成糜状,把剪碎的组织转移至装有0.25% Trypsin的培养瓶中,37℃水浴摇床中酶解30 min。把混合液转移至离心管中,100 r/min离心5 min。弃上清,把组织转移至装有1 mg/mL collagenase(HBSS)的培养瓶中,37℃水浴摇床中酶解 30 min。把混合液转移至离心管中,1 000 r/min离心5 min。弃上清,加入1 mL DMEM/F-12培养基,轻轻吹打制成细胞悬液,并把细胞悬液转移到一次性培养瓶中。37℃、5% CO2培养箱中培养约4 h后再将上层细胞悬液吸出,1 000 r/min离心5 min。弃上清,加入1 mLDMEM/F-12培养基,轻轻吹打后接种至一次性培养皿中,37℃、5% CO2培养箱中培养,每48 h换液一次。待输卵管上皮细胞长至 80%汇合或铺满皿底时,可进行传代培养。大鼠输卵管上皮细胞培养于含10%FBS+1%双抗的DMEM/F12培养基中,37℃,5% CO2,饱和湿度培养箱中培养。
5.细胞鉴定:IF检测细胞角蛋白18的阳性率,将切片取出,用磷酸盐缓冲液(PBS)洗涤2至3次,以4%的多聚甲醛溶液固定30 min,再用PBS进行3次冲洗(每次5 min)。在0.3%的曲拉通溶液中放置制片37 ℃封闭30 min,洗净后,使用5%的牛血清白蛋白(BSA)在37 ℃条件下封闭60 min,PBS洗三次(每次3 min)。与针对细胞角蛋白18和Vimentin的一抗在4 ℃下过夜孵育,PBS冲洗三次(每次5 min)。在孵育二抗时,滴加50到100 μL的标记有荧光的二抗(Alexa Fluor 488 Goat Anti-Rabbit IgG(H+L) Secondary Antibody,(AWS0005b)),在37 ℃浸泡90 min,用PBS冲洗三次(每次5 min)。用DAPI工作液在37 ℃下染核10 min,PBS冲洗三次(每次5 min)。用甘油封片,并将制片避光保存或放置于荧光显微镜下进行观察。
6.大鼠输卵管上皮细胞炎症模型的建立及分组:制备模型细胞前进行转染,首先设立IP(si-NC组,si-CYLD组)、input(si-NC组,si-CYLD组)、再分别建立oe-NC组、oe-CYLD组、oe-CYLD+oe-NC组、oe-CYLD+oe-TRAF6组。每组5个样本。制作输卵管上皮细胞炎症模型,如直接采用输卵管炎性不孕大鼠的输卵管标本进行培养,输卵管炎性上皮细胞在营养良好的培养基中生长,炎性程度将逐渐减轻,故可能影响药物对炎性细胞治疗作用的观察。为确保试验结果的准确性,选择未造模空白组大鼠的输卵管,取上皮细胞进行原代及传代培养,利用脂多糖(LPS)诱导细胞炎症模型。在培养的大鼠输卵管上皮细胞中添加200 ng/mL浓度的LPS进行刺激,以培养基替代LPS 作为阴性对照(0 ng/mL LPS)。并在 24 h不同时间点收取样品。
7.Co-IP检测TRAF6与CYLD灰度:用冰预冷PBS洗涤细胞,加适量RIPA裂解液,12 000 rpm离心15 min后转移倒1.5 mL的离心管中提取蛋白,分为2管,加入一定量的抗体混匀后孵育过夜,偶联琼脂糖珠获得沉淀,75V,130 min电泳后300 mA恒定电流转膜,用1×PBST配制5%脱脂奶粉/BSA封闭,一抗孵育10 min,4℃,1×PBST洗3次;二抗孵育用1×PBST洗3次,每次15 min。使用ECL化学发光液与膜孵育1 min,用滤纸吸尽液体,用塑封膜将膜包裹杂交膜,在凝胶成像系统成像。使用ECL化学发光液与膜孵育1 min,用滤纸吸尽液体,用塑封膜将膜包裹杂交膜,凝胶成像系统成像。
8.Western blot检测CYLD、TRAF6、NF-κBp65、p-p65、IkB-a、p-IkB-a表达:用冰预冷PBS洗涤细胞,加适量RIPA裂解液,12 000 rpm离心15 min取上清液即为细胞全蛋白,BCA法测定蛋白浓度,75V,130 min电泳,300 mA恒定电流转膜,用1×PBST配制5%脱脂奶粉/BSA封闭,一抗孵育10 min,4℃,1×PBST洗3次;二抗孵育用1×PBST洗3次,4℃,每次15 min。使用ECL化学发光液与膜孵育1 min,用滤纸吸尽液体,用塑封膜将膜包裹杂交膜,凝胶成像系统成像。
9.CCK8检测细胞活力:分组的细胞以1×104个细胞/孔密度接种于48孔板内,每孔300 μL。各组均设3个复孔;培养贴壁后处理合适时间,按照每孔加入30 μL/孔的cck8,用完全培养基配置cck8溶液,去除含药培养基每孔加入300 uL含有cck8的培养基;37℃,5%CO2继续孵育4 h后于汇松酶标仪分析450 nm处吸光度(OD)值,取3次实验均值做柱状图。
10.ELISA检测细胞上清中IL-1β、IL-8、IL-6、TNF-α含量:标本于2~8℃ 1 000 g离15 min取细胞上清,按照试剂盒说明书操作,以标准品的浓度为纵坐标,OD值为横坐标,使用专业制作曲线软件“Curve Expert”进行分析,并根据提示制作标准曲线。根据标准品的浓度与OD值计算出标准曲线的回归方程式,将样本的OD 值代入方程式,计算出样本浓度。样本检测前进行过稀释,最后计算时乘以相应的稀释倍数,得到样本的实际浓度后取3次实验的均值。
11.统计学处理:使用 Graphpad Prism 8.0进行统计分析。计算测量数据的均值±标准差。两组或多组之间的比较采用t检验或单向方差分析(ANOVA)。P<0.05表示差异有统计学意义。
结果
1.鉴定大鼠输卵管上皮细胞:从大鼠输卵管组织中分离出上皮细胞IF显示细胞中有细胞角蛋白18存在,证实分离出的细胞为输卵管上皮细胞,见图1。
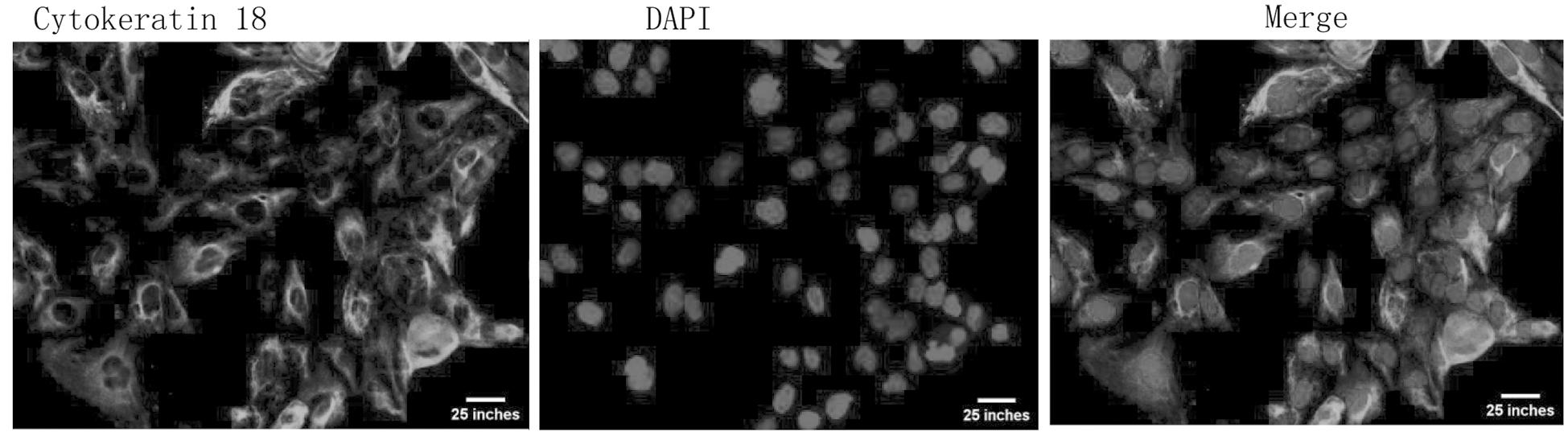
图1 IF鉴定大鼠输卵管上皮细胞
2.TRAF6的泛素化检测:首先设立IP(si-NC组,si-CYLD组)、input(si-NC组,si-CYLD组),比较各组TRAF6、Ub的灰度,发现IP(si-NC组)低于IP(si-CYLD组)TRAF6、Ub的灰度,与input(si-NC组,si-CYLD组)灰度结果相符,见图2。证明CYLD介导TRAF6泛素化。
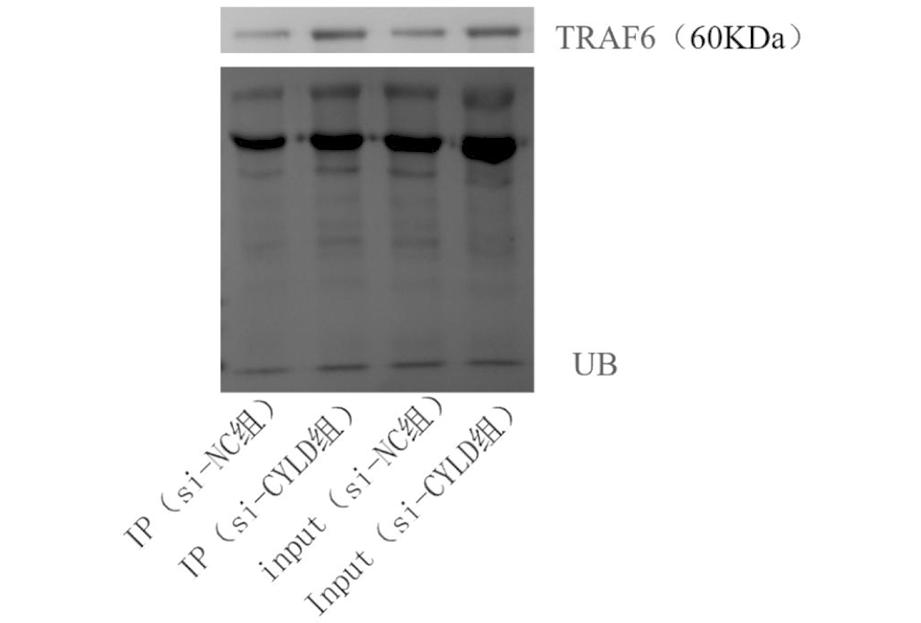
图2 IP检测各组TRAF6、UB水平
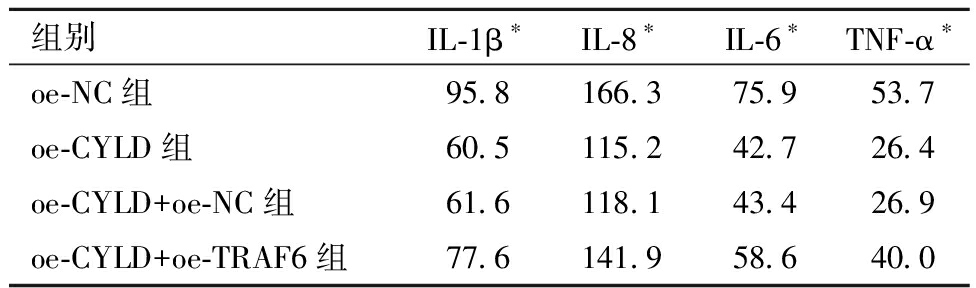
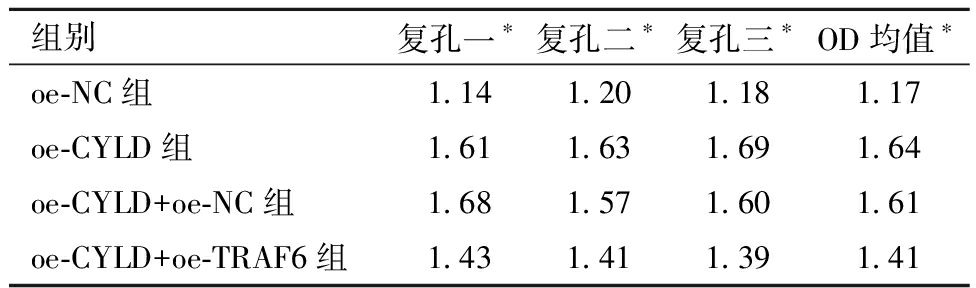
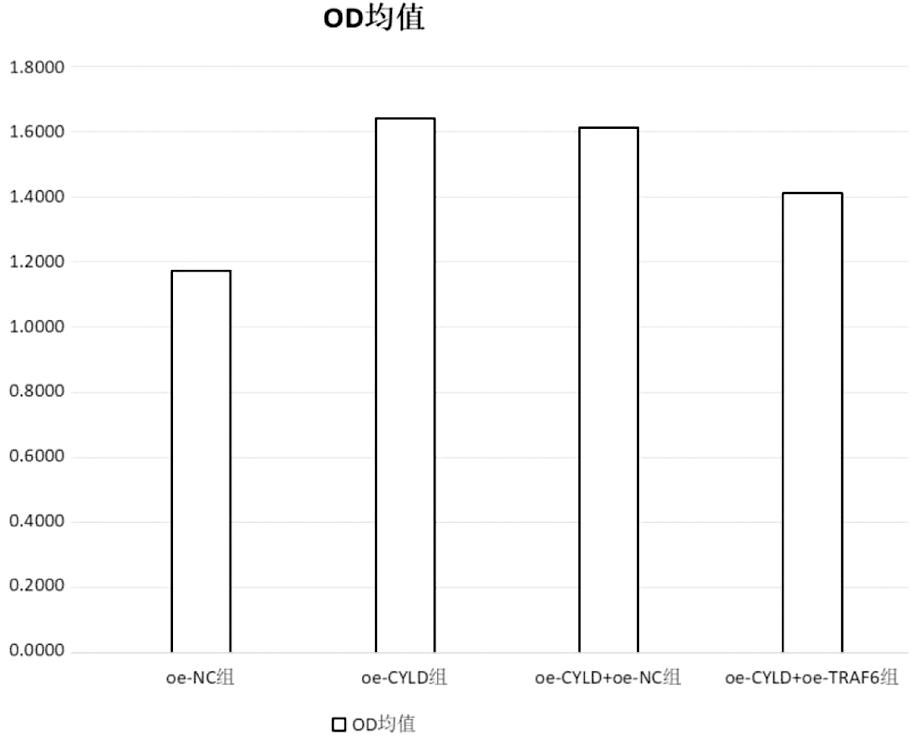
3.TRAF6/NF-κB信号通路相关指标的比较:对比各组NF-κBp65、p-p65、IkB-a、p-IkB-a、TRAF6灰度,oe-CYLD组 图3 各组TRAF6/NF-κB信号通路相关指标表达 4.输卵管上皮细胞中炎症因子的比较:各组炎症因子的表达oe-CYLD组 表1 各组细胞炎症水平比较 组别IL-1β∗IL-8∗IL-6∗TNF-α∗oe-NC组95.8166.375.953.7oe-CYLD组60.5115.242.726.4oe-CYLD+oe-NC组61.6118.143.426.9oe-CYLD+oe-TRAF6组77.6141.958.640.0 组间比较,*P<0.05 5.输卵管上皮细胞活性的比较:对比各组细胞活性oe-CYLD组>oe-CYLD+oe-NC组>oe-CYLD+oe-TRAF6组>oe-NC组,组间差异均具有统计学意义,见表2、图4。提示CYLD可提高输卵管上皮细胞活性,TRAF6降低输卵管上皮细胞活性。 表2 大鼠输卵管上皮细胞经不同处理后细胞活性情况 组别复孔一∗复孔二∗复孔三∗OD均值∗oe-NC组1.141.201.181.17oe-CYLD组1.611.631.691.64oe-CYLD+oe-NC组1.681.571.601.61oe-CYLD+oe-TRAF6组1.431.411.391.41 组间比较,*P<0.05 图4 各组输卵管上皮细胞活性检测 在现代社会,女性不孕症的发病率呈持续增长趋势,而输卵管病变是该病主要的致病因素之一[13]。输卵管炎是盆腔炎性疾病(pelvic inflammatory disease,PID)中最常见的类型,也是导致不孕症的主要原因,盆腔炎会引起输卵管局部组织损伤、粘连、积水、扭曲,影响输卵管的拾卵运卵[14]。当人体免疫力低下,多种微生物侵犯输卵管易引发输卵管炎,主要病原体为淋病奈瑟菌、沙眼衣原体、支原体、阴道毛滴虫[15]。其中,沙眼衣原体是最常见的导致输卵管性不孕的病原微生物[16]。炎症发生时,内、外源微生物刺激大量的炎性细胞活化产生IL-1β、IL-8、IL-6、TNF-α等促炎因子。正常输卵管组织中有一定含量肿瘤坏死因子α(TNF-α),生理水平的TNF-α参与抗感染,有助于组织修复,但高水平的TNF-α可直接诱导中性粒细胞产生大量自由基,刺激输卵管分泌大量白细胞介素-1(interleukin-1,IL-1)、IL-6、IL-8等炎症因子[17]。持续的输卵管炎症过度激活NF-κB信号通路,会加速盆腔炎症循环,严重影响女性输卵管通畅度。目前输卵管炎症相关进展,有实验研究表明[18],hucMSC-EV通过NF-κB信号通路可诱导巨噬细胞从M1型转变为M2型,改善了输卵管局部炎症微环境并抑制了输卵管炎症,从而提高妊娠率改善生殖结局;因此hucMSC-EV可能成为治疗慢性输卵管炎引起的不孕症的一种方法。研究发现[19],人脐带间充质干细胞可通过调节巨噬细胞相关炎症因子缓解慢性输卵管炎。另有研究发现,电针能够通过下调TGF-β1/MAPK信号通路减轻慢性输卵管炎[20]。 NF-κB信号通路是重要的炎症通路,核因子-kB(NF-κB)是细胞内重要的核转录因子,参与机体炎症反应、免疫应答、调节细胞凋亡,其过度激活会导致输卵管炎性病变,p65是其家族成员之一。circRNF10与DHX15相互作用来拮抗DHX15-p65正反馈环,阻断NF-κB信号通路,抑制乳腺癌的发展[21]。NF-κB信号通路通过NF-κB的核移位促进炎症因子的转录介导炎症,TRAF6是一种核心衔接蛋白,作为IL-1受体、TNF-α受体和Toll样受体超家族的主要传导子,介导NF-κB信号通路。NF-κB信号传导的一个核心步骤是激活IKK,使得NF-κB抑制蛋白(IKBs)磷酸化,从而引发IκB蛋白的降解和NF-κB的核转位[22]。不同受体信号激活IKK需要将k63连接的泛素链与其信号元件结合,包括NEMO和上游调控因子,如Tak1、TRAF2、TRAF6等[23]。TRAF6依靠K63连接的泛素链来激活下游信号通路,因此,去泛素化酶可以通过解聚K63链来对NF-κB信号通路进行负调控。CYLD是一种去泛素化酶,可以从各种信号转导相关底物中去除K63连接的多聚泛素链,对NF-κB信号通路进行负调控[24]。泛素化是指泛素分子在特殊酶的作用下,分类细胞内蛋白质,选出靶蛋白分子后进行特异性修饰,影响蛋白质的定位、代谢、功能、降解,从而调控机体生命活动[25]。CYLD既有参与泛素化过程的功能,又是NF-κB信号通路的重要负调控因子,可从TRAF6中去除K63特异性泛素链,抑制其泛素化从而限制其活性,是TARF6的关键去泛素化酶[26]。CYLD的下降会导致细胞内TRAF6泛素化水平升高,促进NF-κB信号通路的激活,引发输卵管炎症。研究证明[27],CYLD的缺失会活化JNK信号通路促进炎症发生。TRAF2 在被多泛素化和激活后,可能是通过自泛素化机制,导致 ERK1/2(细胞外调节蛋白激酶)的激活,介导JNK信号通路传导[28]。与TRAF6相同,TRAF2也被证明是 E3泛素连接酶,通过结合K63使自身泛素化,受 CYLD的调控[29]。本实验未进一步研究CYLD是否通过调控TRAF2影响JNK炎症通路。在以后的研究中,应考虑CYLD对TRAF2等其他衔接蛋白介导的多种炎症通路的调控作用,进一步探索CYLD调控机体炎症的更多机制。 本研究发现,敲减CYLD会增加TRAF6、Ub的灰度,表明敲减CYLD可增加TRAF6泛素化。NF-κB信号通路相关指标NF-κBp65、p-p65、IkB-a、p-IkB-a灰度比较,发现oe-NC+组灰度最深,oe-CYLD组灰度最浅,oe-CYLD+oe-TRAF6组比oe-CYLD+oe-NC组灰度深,表明CYLD介导TRAF6去泛素化调控NF-κB信号通路;检测各组IL-1β、IL-8、IL-6、TNF-α炎症因子,发现oe-CYLD+oe-TRAF6组炎症水平组高于oe-CYLD组,且oe-CYLD组炎症水平低于oe-NC组和oe-CYLD+oe-NC组,表明CYLD介导TRAF6/NF-κB信号通路调控炎症水平,即调高CYLD可以增加对TRAF6的去泛素化从而抑制NF-κB信号通路激活,降低炎症水平;oe-CYLD组输卵管炎症上皮细胞活性最高,oe-CYLD+oe-NC组优于oe-CYLD+oe-TRAF6组,表明CYLD增加TRAF6去泛素化可降低炎症水平,提高输卵管上皮细胞活性。 综上所述,CYLD高表达可降低TRAF6泛素化水平,从而抑制NF-κB信号通路激活,控制输卵管炎症,提高输卵管上皮细胞活性。因此,以CYLD为切入点,研究提高其表达水平的药物增加TRAF6去泛素化抑制NF-κB信号通路可为治疗输卵管炎性不孕提供新的治疗思路。 1 Qiao J,Wang Y,Li X,et al.A Lancet Commission on 70 years of women′s reproductive,maternal,newborn,child,and adolescent health in China.The Lancet,2021,397:2497-2536. 2 Klein EJ,Vrees R,Frishman GN.Female Infertility//Clinical Reproductive Medicine and Surgery:A Practical Guide.Cham:Springer International Publishing,2022:281-301. 3 朱慧莉,黄薇.输卵管性不孕的流行病学及病因.国际生殖健康/计划生育杂志,2016,35:212-216. 4 中华预防医学会生殖健康分会.输卵管性不孕全流程管理中国专家共识(2023年版).中国实用妇科与产科杂志,2023,39:318-324. 5 林小娜,黄国宁,孙海翔,等.输卵管性不孕诊治的中国专家共识.生殖医学杂志,2018,27:1048-1056. 6 Marín-Rubio JL,Raote I,Inns J,et al.CYLD in health and disease.Dis Model Mech,2023,16:dmm050093. 7 Gu Y,Wu S,Fan J,et al.CYLD regulates cell ferroptosis through Hippo/YAP signaling in prostate cancer progression.Cell Death Dis,2024,15:79. 8 Taft J,Markson M,Legarda D,et al.Human TBK1 deficiency leads to autoinflammation driven by TNF-induced cell death.Cell,2021,184:4447-4463.e20. 9 Zhan Y,Xu D,Tian Y,et al.Novel role of macrophage TXNIP-mediated CYLD-NRF2-OASL1 axis in stress-induced liver inflammation and cell death.JHEP Rep,2022,4:100532. 10 Liu J,Guo S,Jiang K,et al.miR-488 mediates negative regulation of the AKT/NF-κB pathway by targeting Rac1 in LPS-induced inflammation.J Cell Physiol,2020,235:4766-4777. 11 Massoumi R.Ubiquitin chain cleavage:CYLD at work.Trends Biochem Sci,2010,35:392-399. 12 Trompouki E,Hatzivassiliou E,Tsichritzis T,et al.CYLD is a deubiquitinating enzyme that negatively regulates NF-kappaB activation by TNFR family members.Nature,2003,424:793-796. 13 中华预防医学会生育力保护分会,中国医师协会生殖医学专业委员会.育龄人群不孕不育防治临床实践指南(2024).中华生殖与避孕杂志,2024,44:1215-1234. 14 韩晨光,王芳,李红义,等.1771对夫妇不孕症成因分析及伦理因素探讨.解放军预防医学杂志,2020,38:35-38. 15 Zhai YJ,Feng Y,Ma X,et al.Defensins:defenders of human reproductive health.Hum Reprod Update,2023,29:126-154. 16 AlSaeghi S,Al-Mahrouqi T,Al-Khadhuri M,et al.Parental consanguinity and ovarian reserve:A retrospective cohort study.Int J Reprod Biomed,2023,21:1013-1020. 17 蒿长玲,陈萍.输卵管炎性不孕的研究进展.光明中医,2019,34:1611-1614. 18 Zhang C,Liao W,Li W,et al.Human umbilical cord mesenchymal stem cells derived extracellular vesicles alleviate salpingitis by promoting M1-to-M2 transformation.Front Physiol,2023,14:1131701. 19 Liao W,Li X,Tang X.Human Umbilical Cord Mesenchymal Stem Cells Alleviate Chronic Salpingitis by Modulating Macrophage-Associated Inflammatory Factors.Curr Stem Cell Res Ther,2024,19:1442-1448. 20 Xijiao HU,Yinglong C,Huanan K,et al.Electroacupuncture attenuates chronic salpingitis transforming growth factor-β1/p38 mitogen-activated protein kinase signaling pathway.J Tradit Chin Med,2022,42:781-787. 21 Zheng W,Wang X,Yu Y,et al.CircRNF10-DHX15 interaction suppressed breast cancer progression by antagonizing DHX15-NF-κB p65 positive feedback loop.Cell Mol Biol Lett,2023,28:34. 22 Iacobazzi D,Convertini P,Todisco S,et al.New insights into NF-κB signaling in innate immunity:focus on immunometabolic crosstalks.Biology,2023,12:776. 23 Sun SC.Deubiquitylation and regulation of the immune response.Nat Rev Immunol,2008,8:501-511. 24 Massoumi R.Ubiquitin chain cleavage:CYLD at work.Trends Biochem Sci,2010,35:392-399. 25 Rennie ML,Chaugule VK,Walden H.Modes of allosteric regulation of the ubiquitination machinery.Curr Opin Struct Biol,2020,62:189-196. 26 Zhang Z,Zhang S,Jiang X,et al.Spata2L Suppresses TLR4 Signaling by Promoting CYLD-MediatedDeubiquitination of TRAF6 and TAK1.Biochemistry(Mosc),2022,87:957-964. 27 Reiley W,Zhang M,Sun SC.Negative regulation of JNK signaling by the tumor suppressor CYLD.J Biol Chem,2004,279:55161-55167. 28 Oh YT,Yue P,Sun SY.DR5 suppression induces sphingosine-1-phosphate-dependent TRAF2 polyubiquitination,leading to activation of JNK/AP-1 and promotion of cancer cell invasion.Cell Commun Signal,2017,15:18. 29 Kovalenko A,Chable-Bessia C,Cantarella G,et al.The tumour suppressor CYLD negatively regulates NF-kappaB signalling by deubiquitination.Nature,2003,424:801-805.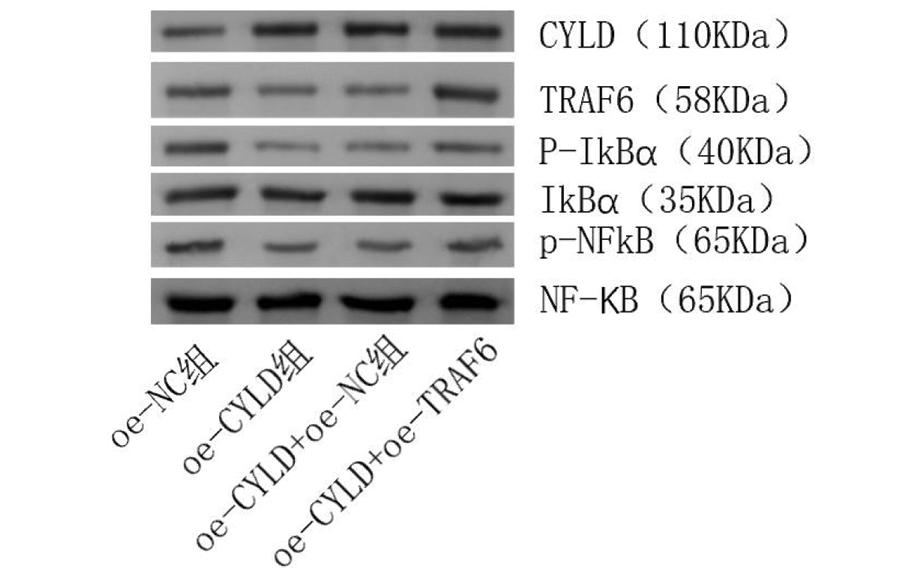
![]()
讨论