TORCH是包括巨细胞病毒(cytomegalovirus,CMV)、单纯疱疹病毒(herpes simplex virus,HSV)、风疹病毒(rubella virus,RV)、弓形虫(toxoplasma gondii,TOX)和其他病原体的一组病原体。TORCH感染可以从母体传播给胎儿或新生儿,并对其构成风险。感染可以发生在宫内和新生儿的不同时期,如在子宫内、分娩时或产后。TORCH感染可导致流产、死产、先天性畸形、早产、宫内发育迟缓,还可能在新生儿期表现为无症状感染但持续存在,最终导致慢性神经系统后遗症[1]。体外受精-胚胎移植(in vitro fertilization and embryo transfer, IVF-ET)和卵胞浆内单精子注射(intracytoplasmic sperm injection,ICSI)技术是不孕症患者的可靠治疗手段。本研究的对象是实施IVF/ICSI-ET 治疗患者,并且选择仍有众多争议的 TORCH 感染与自然流产的关联为研究方向,结合倾向性评分匹配(propensity score matching,PSM)的统计学方法,具有创新性。由于研究人群的特殊性,本研究通过对IVF/ICSI-ET患者自然流产的调查分析,帮助辅助生殖接受咨询的人群根据风险大小制定妊娠和生育计划。
对象与方法
1.对象:选取2017年1月1日至2020年12月31日在山东大学附属生殖医院行IVF/ICSI-ET治疗的患者为研究对象,进行TORCH血清学筛查,随访患者自确立妊娠起至16个月,记录妊娠结局,根据纳入、排除标准共筛选出1 265名自然流产患者(自然流产组)和4 562名正常分娩患者(正常分娩组)纳入研究。纳入标准包括(1)行IVF/ICSI-ET治疗的不孕女性;(2)患者的临床资料及TORCH检测结果完整;(3)配合完成随访过程。排除标准包括(1)因染色体异常、内分泌异常、解剖异常等明确原因导致的自然流产患者;(2)合并糖尿病及高血压患者;(3)肝肾功能及代谢功能异常。
2.试剂与仪器:全套由意大利索灵诊断医疗设备有限公司生产的 TORCH 配套质控品与试剂;LIAISON 全自动免疫化学发光分析仪。
3.样本采集:通过无菌静脉穿刺方法采集受试对象静脉血5 mL于不添加抗凝剂的真空管中,转速3 500 r/min离心10 min,分离血清置于全自动化学发光分析仪上检测TORCH-免疫球蛋白M(IgM)和TORCH-免疫球蛋白G(IgG)。
4.统计学处理:应用 R 软件(R 4.2.1)采用PSM的统计学方法对自然流产组和正常分娩组进行1∶1匹配,卡钳值设定为0.001,匹配因素为不孕年限、年龄、体重指数(body mass index,BMI)、季节、学历、地区、年度,以 P<0.05为差异具有统计学意义。运用 SPSS 21.0 对所得资料进行统计学处理。计数数据为病例数或百分率,组间阳性率(%)比较采用 χ 2检验。多因素分析采用多因素Logistic回归分析,P<0.05为差异具有统计学意义。
结果
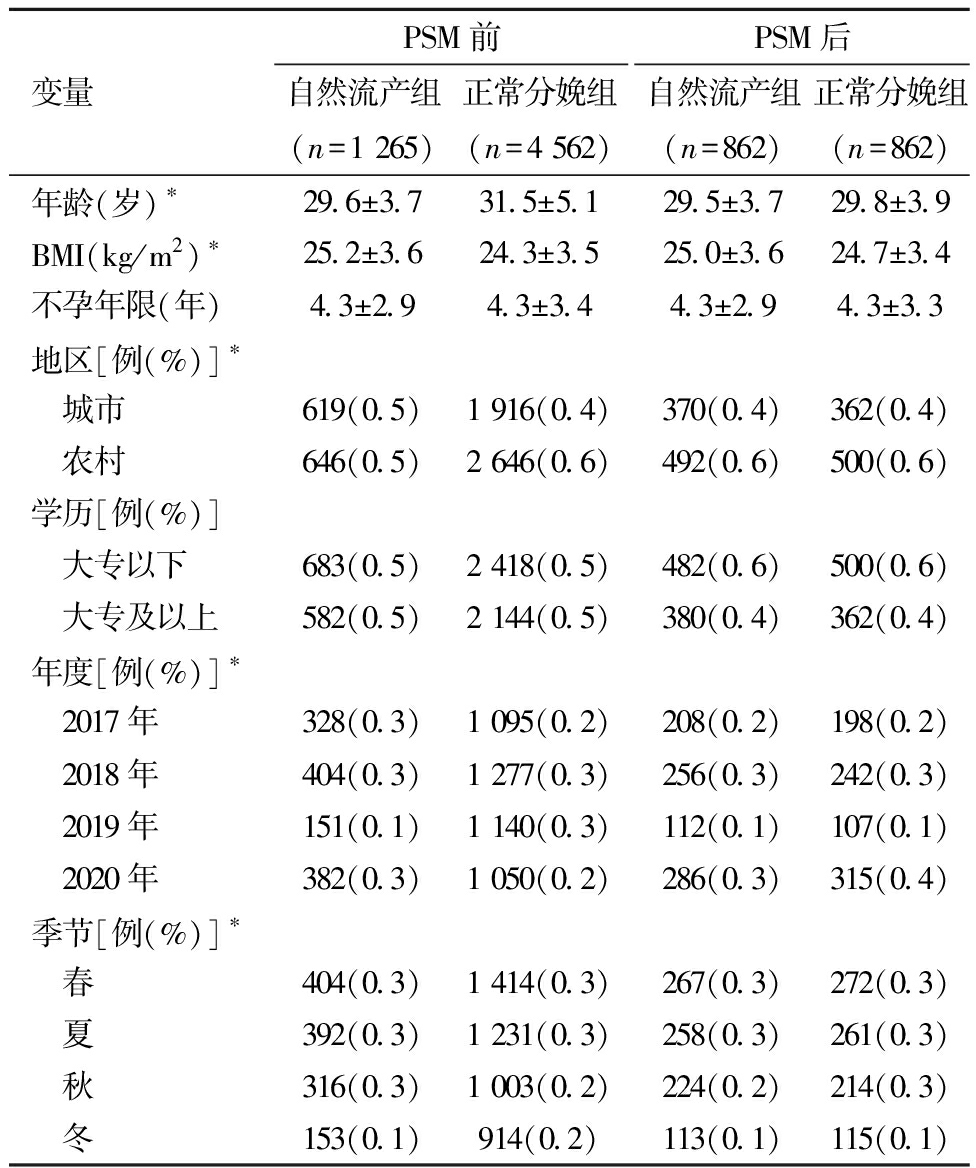
1.PSM前后自然流产组与正常分娩组基线资料比较:PSM 前,自然流产组的年龄、BMI、地区分布、年度分布、季节分布与正常分娩组相比,差异均有统计学意义。PSM 后,自然流产组与正常分娩组基线资料分布平衡(P>0.05)。见表1。
表1 PSM前后自然流产组与正常分娩组基线资料比较
变量PSM前自然流产组(n=1 265)正常分娩组(n=4 562)PSM后自然流产组(n=862)正常分娩组(n=862)年龄(岁)∗29.6±3.731.5±5.129.5±3.729.8±3.9BMI(kg/m2)∗25.2±3.624.3±3.525.0±3.624.7±3.4不孕年限(年)4.3±2.94.3±3.44.3±2.94.3±3.3地区[例(%)]∗ 城市619(0.5)1 916(0.4)370(0.4)362(0.4) 农村646(0.5)2 646(0.6)492(0.6)500(0.6)学历[例(%)] 大专以下683(0.5)2 418(0.5)482(0.6)500(0.6) 大专及以上582(0.5)2 144(0.5)380(0.4)362(0.4)年度[例(%)]∗ 2017年328(0.3)1 095(0.2)208(0.2)198(0.2) 2018年404(0.3)1 277(0.3)256(0.3)242(0.3) 2019年151(0.1)1 140(0.3)112(0.1)107(0.1) 2020年382(0.3)1 050(0.2)286(0.3)315(0.4)季节[例(%)]∗ 春404(0.3)1 414(0.3)267(0.3)272(0.3) 夏392(0.3)1 231(0.3)258(0.3)261(0.3) 秋316(0.3)1 003(0.2)224(0.2)214(0.3) 冬153(0.1)914(0.2)113(0.1)115(0.1)
PSM前,与正常分娩组比较,*P<0.05
2.PSM前不同妊娠结局与TORCH的关系:
(1)PSM前不同妊娠结局与TORCH-IgM的关系。
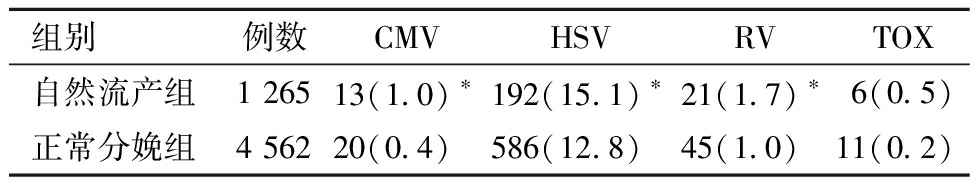
PSM前,自然流产组的CMV-IgM、HSV-IgM、RV-IgM阳性率高于正常分娩组,差异有统计学意义。自然流产组的TOX-IgM阳性率与正常分娩组比较,差异无统计学意义。见表2。
表2 PSM前不同妊娠结局与TORCH-IgM感染的关系 [例(%)]
组别例数CMVHSVRVTOX自然流产组1 26513(1.0)∗192(15.1)∗21(1.7)∗6(0.5)正常分娩组4 56220(0.4)586(12.8)45(1.0)11(0.2)
与正常分娩组比较,*P<0.05
(2)PSM前不同妊娠结局与TORCH-IgG的关系。
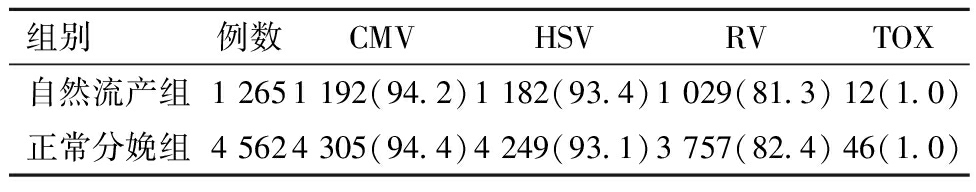
PSM前,自然流产组的CMV-IgG、HSV-IgG、RV-IgG、TOX-IgG阳性率与正常分娩组比较,差异均无统计学意义。见表3。
表3 PSM前不同妊娠结局与TORCH-IgG的关系[例(%)]
组别 例数CMVHSVRVTOX自然流产组1 2651 192(94.2)1 182(93.4)1 029(81.3)12(1.0)正常分娩组4 5624 305(94.4)4 249(93.1)3 757(82.4)46(1.0)
3.PSM后不同妊娠结局与TORCH的关系:
(1)PSM后不同妊娠结局与TORCH-IgM的关系。
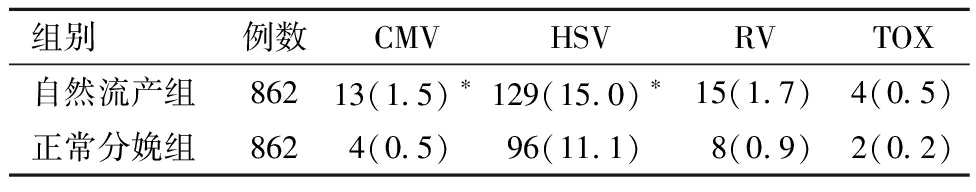
表4 PSM后不同妊娠结局与TORCH-IgM的关系[例(%)]
组别例数CMVHSVRVTOX自然流产组86213(1.5)∗129(15.0)∗15(1.7)4(0.5)正常分娩组8624(0.5)96(11.1)8(0.9)2(0.2)
与正常分娩组比较,*P<0.05
PSM后,自然流产组的CMV-IgM、HSV-IgM阳性率高于正常分娩组,差异有统计学意义。自然流产组的RV-IgM、TOX-IgM阳性率与正常分娩组比较,差异无统计学意义。见表4。
(2)PSM后不同妊娠结局与TORCH-IgG的关系。
PSM后,自然流产组的CMV-IgG、HSV-IgG、RV-IgG、TOX-IgG阳性率与正常分娩组比较,差异均无统计学意义。见表5。
表5 PSM后不同妊娠结局与TORCH-IgG的关系[例(%)]
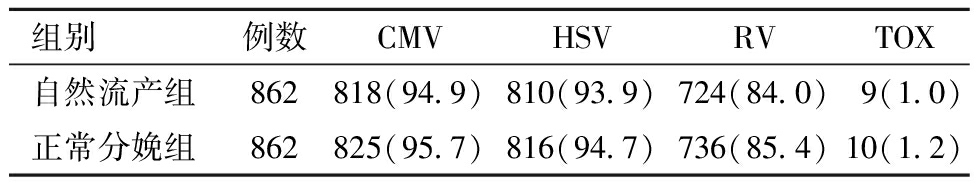
组别例数CMVHSVRVTOX自然流产组862818(94.9)810(93.9)724(84.0)9(1.0)正常分娩组862825(95.7)816(94.7)736(85.4)10(1.2)
4.行IVF/ICSI-ET的自然流产患者PSM后多因素Logistic回归分析:PSM后,以是否发生自然流产为因变量,CMV感染、HSV感染、RV感染、TOX感染为自变量并赋值,见表6。
表6 自变量赋值情况

自变量赋值情况10CMV-IgM(+)是否CMV-IgG(+)是否HSV-IgM(+)是否HSV-IgG(+)是否RV-IgM(+)是否RV-IgG(+)是否TOX-IgM(+)是否TOX-IgG(+)是否
多因素Logistic回归分析发现,CMV-IgM(+)、HSV-IgM(+)是自然流产的独立危险因素。见表7。
表7 PSM后自然流产的多因素Logistic回归分析
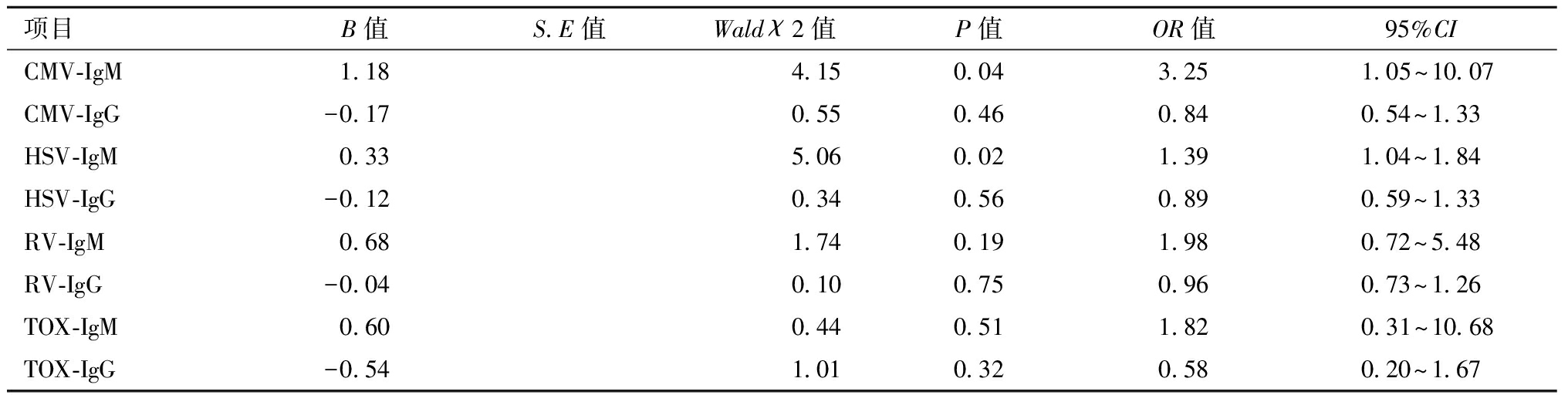
项目B值S.E值Wald χ 2值P值OR值95%CICMV-IgM1.180.584.150.043.251.05~10.07CMV-IgG-0.170.230.550.460.840.54~1.33HSV-IgM0.330.155.060.021.391.04~1.84HSV-IgG-0.120.210.340.560.890.59~1.33RV-IgM0.680.521.740.191.980.72~5.48RV-IgG-0.040.140.100.750.960.73~1.26TOX-IgM0.600.900.440.511.820.31~10.68TOX-IgG-0.540.541.010.320.580.20~1.67
讨论
妊娠期间CMV、HSV、RV和TOX原发感染可带来多种临床症状,具体取决于妊娠阶段。妊娠初期的TORCH感染可能导致自然流产、先天性畸形、宫内生长受限或胎儿死亡。一些研究[2-4]报道了TORCH血清阳性与产科不良妊娠结局之间的相关性,但目前缺乏IVF/ICSI-ET不孕女性关于TORCH感染状态和自然流产的基线数据,本研究通过补充数据为临床医生的治疗方案提供理论基础。本研究追踪随访进行TORCH-IgM及TORCH-IgG检查的病例,分析行IVF/ICSI-ET技术实现妊娠女性的自然流产发生率,多因素Logistic回归分析发现自然流产的危险因素,从而为行IVF/ICSI-ET技术的人群降低不良妊娠的发生提供理论指导,为生殖科、产科医生针对患者咨询和治疗提供建议。
PSM是一种可以减少混杂偏倚的方法,研究发现[5-6],不孕年限、年龄、体重指数、季节、学历、地区、年度等混杂因素在TORCH感染时,会对不良妊娠结局影响时的可靠程度产生干扰。为减少不同组之间混杂因素的影响,具有可比性,使用PSM的方法进行研究。本研究发现,PSM前,自然流产组RV-IgM的阳性率显著高于正常分娩组。PSM后,自然流产组与正常分娩组RV-IgM的阳性率无显著性差异,与以往研究[2]观点一致。提示探究TORCH病原体感染对自然流产的影响需排除混杂因素后进行研究。
自然流产是指孕妇妊娠不足28周且胎儿体重不足1 kg产生的妊娠失败[7]。研究发现[2],有自然流产史的妇女CMV-IgM、HSV-IgM、TOX-IgM的阳性率高于正常女性,RV-IgM与自然流产无相关性。本研究PSM后发现,自然流产女性CMV-IgM、HSV-IgM阳性率高于正常分娩女性,多因素Logistic回归分析发现CMV-IgM、HSV-IgM是自然流产的危险因素。提示行IVF/ICSI-ET不孕女性进行自然流产原因分析时,应考虑是否存在CMV、HSV感染因素。自然流产有多种病因和可能导致胎儿死亡的潜在致病机制。关于CMV导致自然流产的原因从以下几方面分析。CMV 感染相对常见,具有较高的经胎盘传播率[8],并且与已知导致胎儿畸形和宫内死亡的胎盘损伤有关[9]。CMV可以在原发性母体感染的情况下感染胎儿。在妊娠期前,或者在妊娠期间CMV血清阳性的女性中,进行病毒再激活或再感染,病毒向发育中的胎儿传播,导致流产和包括神经系统在内的其他后遗症。在接受TORCH检查的人群中,先天性CMV感染的可能性与育龄妇女的血清阳性率成正比[10-11]。CMV 血清阳性率随着年龄的增长而增加[12],并因地理区域和社会经济地位而异[13]。先天性 CMV 感染可直接对胎儿造成损伤,也可通过感染或免疫介导的病理机制引起胎盘功能障碍间接导致胎儿损伤[14]。CMV经胎盘感染胚胎或胎儿被认为会导致与胎盘病理相关的不良妊娠结局,包括自然流产、宫内发育迟缓和死产[15-16]。HSV感染可导致流产,若孕晚期检测出HSV感染建议经剖宫产分娩[17]。HSV-2通过性接触传播导致生殖器疱疹,而HSV-1 通过非性接触传播,导致皮肤黏膜疾病主要涉及口腔和黏膜[18-19]。超过 75% 的原发性生殖器 HSV 感染仍然无症状或未被识别,但在怀孕期间,它可能导致自然流产、早产和新生儿疱疹[20]。妊娠前半期原发性 HSV 感染与胎儿发病率和死亡率增加有关。妊娠晚期HSV感染与新生儿传播的风险增高有关[21]。本研究未发现TOX与自然流产存在相关性,关于TOX感染与自然流产的关联,不同研究得出的结论不同,有的研究[22]未发现TOX血清阳性率与自然流产之间存在关联,有的研究[23]显示TOX血清阳性率与自然流产存在关联,产生差异的原因可能与研究人群以及地理区域的不同有关。
本研究发现行IVF/ICSI-ET不孕女性既往TORCH感染不会增加自然流产的发生,多因素Logistic回归分析发现TORCH-IgG不是自然流产的危险因素。关于既往TORCH感染是否是自然流产的危险因素,学者的研究结果也不尽一致。有的研究发现[24],TORCH-IgG不会增加自然流产发生的风险。有的研究[2]发现,HSV-IgG自然流产女性的阳性率显著高于未发生自然流产的女性,这可能与研究对象不同有关,也可能与地域差异有关。大部分研究分析TORCH-IgG对女性生殖系统的影响机制未得出确切的结论,这需要更多大规模临床数据的支持。
急性CMV、HSV感染是自然流产的危险因素,因此,提倡以预防为主,并广泛针对辅助生殖女性宣传TORCH感染的危害。妊娠早期母体TORCH筛查被证明是早期检测和治疗感染的二级预防策略。在过去的十年中,为诊断孕产妇早期感染,实验室做出了重大努力。通过母体血清学检测在人群中进行TORCH筛查被列为中国孕前保健指南的重要项目[25]。如果女性在孕早期的TORCH血清学筛查检测呈阳性,则有可能发现不良妊娠结局,例如流产和胎儿发育异常,但这种情况发生的可能性以及它将如何影响个体女性仍有待解答。鉴于筛查和诊断检测之间的时间差,因此从流行病学角度来看,需要更好地了解 CMV、HSV 筛查呈阳性的不孕女性与自然流产之间的关系。为帮助接受咨询的人群根据风险的大小制定妊娠和生育计划,量化行IVF/ICSI-ET助孕前血清学TORCH筛查呈阳性的女性自然流产的风险仍是今后研究中需要解决的问题。
1 Qi Y,Zhu S,Li C,et al.Seroepidemiology of TORCH antibodies in the reproductive-aged women in China.Eur J Obstet Gynecol Reprod Biol,2020,254:114-118.
2 王甲甲,王智斌,黄文芳.TORCH 病原体感染与自然流产的关系及影响因素.中国计划生育和妇产科,2015:49-52.
3 Qin X,Zhang S,Liu H,et al.Seroepidemiology of TORCH Infections among 1.7 Million Women of Childbearing Age in Rural China:A Population-Based Cross-Sectional Study.Am J Trop Med Hyg,2021,105:1202-1209.
4 Song X,Li Q,Diao J,et al.Association between first-trimester maternal cytomegalovirus infection and stillbirth:A prospective cohort study.Front Pediatr,2022,10:803568.
5 张晓冬,王鑫,高选,等.基于IVF-ET技术的自然流产患者TORCH感染情况调查.检验医学与临床,2023,20:920-924.
6 杨娟,张月,张东梅,等.深圳市330 115例孕前优生健康检查育龄女性TORCH筛查结果分析.中华生殖与避孕杂志,2021,41:1011-1018.
7 Nguyen BT,Chang EJ,Bendikson KA.Advanced paternal age and the risk of spontaneous abortion:an analysis of the combined 2011-2013 and 2013-2015 National Survey of Family Growth.Am J Obstet Gynecol,2019,221:476.e1-476.e7.
8 Kumar M,Nizam MB,Mugunthan M.Seroprevalence of cytomegalovirus infection in antenatal women in a Tertiary Care Center in Western India.J Marine Med Soc,2017,19:51-54.
9 Tomac J,Mazor M,Lisnic′ B,et al.Viral infection of the ovaries compromises pregnancy and reveals innate immune mechanisms protecting fertility.Immunity,2021,54:1478-1493.e6.
10 de Vries JJ,van Zwet EW,Dekker FW,et al.The apparent paradox of maternal seropositivity as a risk factor for congenital cytomegalovirus infection:a population-based prediction model.Rev Med Virol,2013,23:241-249.
11 Hamilton ST,van Zuylen W,Shand A,et al.Prevention of congenital cytomegalovirus complications by maternal and neonatal treatments:a systematic review.Rev Med Virol,2014,24:420-433.
12 杨峻.孕前优生健康检查TORCH检测结果的分析.中国医药指南,2025,23:97-100.
13 Radoi CL,Zlatian O,Balasoiu M,et al.Seroprevalence of infections with TORCH agents in Romania:A systematic review.Microorganisms,2023,11:2120.
14 Njue A,Coyne C,Margulis AV,et al.The Role of Congenital Cytomegalovirus Infection in Adverse Birth Outcomes:A Review of the Potential Mechanisms.Viruses,2020,13:20.
15 王仙凤,谭晓霞.丽水市孕前检查TORCH感染及与死胎死产、自然流产史的关系.中国妇幼保健,2016,31:342-344.
16 Yamada H,Tanimura K,Tairaku S,et al.Clinical factor associated with congenital cytomegalovirus infection in pregnant women with non-primary infection.J Infect Chemother,2018,24:702-706.
17 段忠亮,李翠,应春妹.上海地区1072例育龄妇女孕前TORCH感染情况及与不良妊娠结局的相关性.中国妇幼保健,2021,36:4292-4294.
18 Prasoona KR,Srinadh B,Sunitha T,et al.Seroprevalence and influence of torch infections in high risk pregnant women:A large study from south india.J Obstet Gynaecol India,2015,65:301-309.
19 Lao TT,Mak J,Li TC.Hepatitis B virus infection status and infertility causes in couples seeking fertility treatment-Indicator of impaired immune response.Am J Reprod Immunol,2017,77:e12636.
20 Egan KP,Hook LM,Naughton A,et al.An HSV-2 nucleoside-modified mRNA genital herpes vaccine containing glycoproteins gC,gD,and gE protects mice against HSV-1 genital lesions and latent infection.PLoS Pathog,2020,16:e1008795.
21 Dinkar A,Singh J.Seroprevalence of Toxoplasma,Rubella,CMV and HSV infection at a teaching hospital:A 7 year study from North India.J Family Med Prim Care,2020,9:2253-2257.
22 Alvarado-Esquivel C,Pacheco-Vega SJ,Hernández-Tinoco J,et al.Miscarriage history and Toxoplasma gondii infection:A cross-sectional study in women in Durango City,Mexico.Eur J Microbiol Immunol(Bp),2014,4:117-122.
23 Al-Adhroey AH,Mehrass A,Al-Shammakh AA,et al.Prevalence and predictors of Toxoplasma gondii infection in pregnant women from Dhamar,Yemen.BMC Infect Dis,2019,19:1089.
24 Al-Hakami AM,Paul E,Al-Abed F,et al.Prevalence of toxoplasmosis,rubella,cytomegalovirus,and herpes(TORCH) infections among women attending the antenatal care clinic,maternity hospital in Abha,Southwestern Saudi Arabia.Saudi Med J,2020,41:757-762.
25 中华医学会妇产科学分会产科学组.孕前和孕期保健指南(2018).中华妇产科杂志,2018,53:7-13.