妊娠期糖尿病(gestational diabetes mellitus,GDM)是指在妊娠期间首次发现或确诊的糖耐量异常状态,发病率逐年上升[1-2]。GDM全球发病率约为18%[3],是临床常见的妊娠急性并发症,增加了孕产妇和胎儿致死致残率,严重影响母婴健康[4]。因此早筛查、早发现、早干预在GDM母婴结局中起到重要作用。外泌体是一种由细胞主动分泌的具有脂质双分子层膜结构的小囊泡(直径约40~120 nm)[5-6],作为生物体重要的信息载体,可将生物信息物质(microRNA、lncRNA、DNA、蛋白质等)传递给靶细胞。富亮氨酸α-2 糖蛋白1(leucine-rich-alpha-2-glycoprotein 1,LRG1)是一种分泌性蛋白,在多种疾病的发生发展过程中起了关键作用,其中在自身免疫性疾病、肿瘤、炎症性疾病等标本中均检测到LRG1,它是一种多功能调节蛋白,可与胰岛素受体结合,促进胰岛β细胞增殖和胰岛分泌,在糖尿病、肥胖、炎症等疾病中发挥重要作用[7]。细胞外基质蛋白1(extracellular matrix protein-1,ECM1)是新近发现的一种分泌性糖蛋白,能够形成细胞之间的杂质基质,在调节细胞内运输,信号转导和能量交换过程中发挥关键作用[8-10],已证明ECM 1在表皮细胞的分化以及表皮层糖蛋白与胶原蛋白连接中具有重要作用[11-12]。研究发现糖尿病患者体内ECM1大量积聚会引起糖尿病早期肾性改变[13]。研究证实GDM与健康孕产妇体内外泌体的含量和生物活性均存在差异,但是外泌体LRG1和ECM1在孕产妇脐带血中研究甚少。本研究对比GDM和健康(normal glucose tolerance,NGT)孕妇脐带血中外泌体LRG1和ECM1的含量,初步探讨外泌体LRG1、ECM1与GDM的关系。
对象与方法
1.对象:选择2021年3月到8月在青海省人民医院产检并确诊为GDM孕妇(GDM组)15例,同期产检的NGT孕妇15例。妊娠期糖尿病的诊断标准参照国际糖尿病与妊娠研究组制定的标准[14]。入组孕妇均为单胎妊娠,不吸烟、不喝酒、不吸毒;既往无糖尿病、高血压、先天性心脏病、自身免疫性疾病、家族遗传病等。本研究获得受试者知情同意,经青海省人民医院伦理委员会审核批准。
2.脐带血标本采集:收集研究对象的脐带血5 mL,部分暂放于4 ℃保存,部分进行离心(4 ℃、13 000 r、15 min)收取集血浆,用于提取外泌体。
3.脐带血外泌体提取及浓度测定:将离心所得的血浆,离心(4 ℃、8 000 r、30 min)取上清。按照外泌体提纯试剂盒(System Biosciences,Palo Alto,CA,USA)操作说明,在上清中加入试剂,4 ℃孵育30 min,去掉上清,管底沉淀为外泌体。通过CD63和胎盘碱性磷酸酶ELISA试剂盒(Beyotime,南京,中国)对提取的外泌体进行定量。
4.免疫印迹(WB)和ELISA检测脐带血中LRG1和ECM1的水平:
(1)免疫印迹(WB)操作方法。
在装有外泌体沉淀物的EP管中,加入适量RIPA裂解液及蛋白酶抑制剂,冰上静置20 min,离心(4 ℃、12 000 r、20 min)取上清。将提取的上清即外泌体蛋白按BCA法进行蛋白浓度测定。在外泌体蛋白样品中加入5×loading buffer稀释液,进行100 ℃金属浴10 min,自然冷却后放-20 ℃保存。外泌体蛋白上样-电泳-转印-封闭-加入一抗低温孵育14 h-T洗膜-二抗室温1 h-洗膜-显影-拍照分析。
(2)ELISA操作方法。
取出4 ℃保存的脐带血,室温平衡15 min,离心(4 ℃、12 000 r、15 min)取上清。按照ELISA试剂盒说明书检测脐带血血清中LRG1和ECM1蛋白含量。
5.统计学处理:采用SPSS 20.0软件进行统计分析,计量资料以均数±标准误表示。组间比较采用t检验或单因素方差分析。P<0.05认为差异有统计学意义。
结果
1.研究对象一般资料:NGT和GDM孕妇组的基础资料身高、体重、体重指数、孕周、收缩压和舒张压等都无显著差异性(P>0.05),见表1。
表1 研究对象的一般临床资料

组别例数年龄(岁)身高(cm)体重(kg)体重指数(%)孕周(w)SBP(mm/Hg)DBP(mm/Hg)GDM1525.4±2.9158.1±1.265.2±3.525.9±1.237.7±2.3113.5±2.466.4±1.5NGT1524.7±5.3156.5±0.960.4±9.926.1±0.838.7±1.8107.1±2.566.5±2.1
SBP为收缩压,DBP为舒张压
2.脐带血外泌体特异性标志蛋白CD63含量及脐带血中胎盘来源外泌体PLAP水平比较:ELISA结果显示,GDM组孕妇脐血外泌体特异性标志蛋白CD63含量及脐带血中胎盘来源外泌体PLAP水平均显著高于NGT组(P均<0.05),见表2。
表2 脐带血外泌体特异性标志蛋白CD63含量的比较

组别例数CD63含量(pg/mL) PLAP(pg/mL)GDM15245.2±4.9∗540.1±1.9∗NGT15185.0±4.4386.5±2.7
与NGT组比较,*P<0.05
3.脐带血中外泌体LRG1和ECM1的表达:免疫印迹结果显示,GDM组和NGT组脐带血中提取的外泌体中均有LRG1和ECM1蛋白表达,提示外泌体LRG1和ECM1分离、提取成功。ELISA实验结果显示,GDM组脐带血中外泌体LRG1和ECM1含量均明显高于NGT组(P<0.05),见图1。
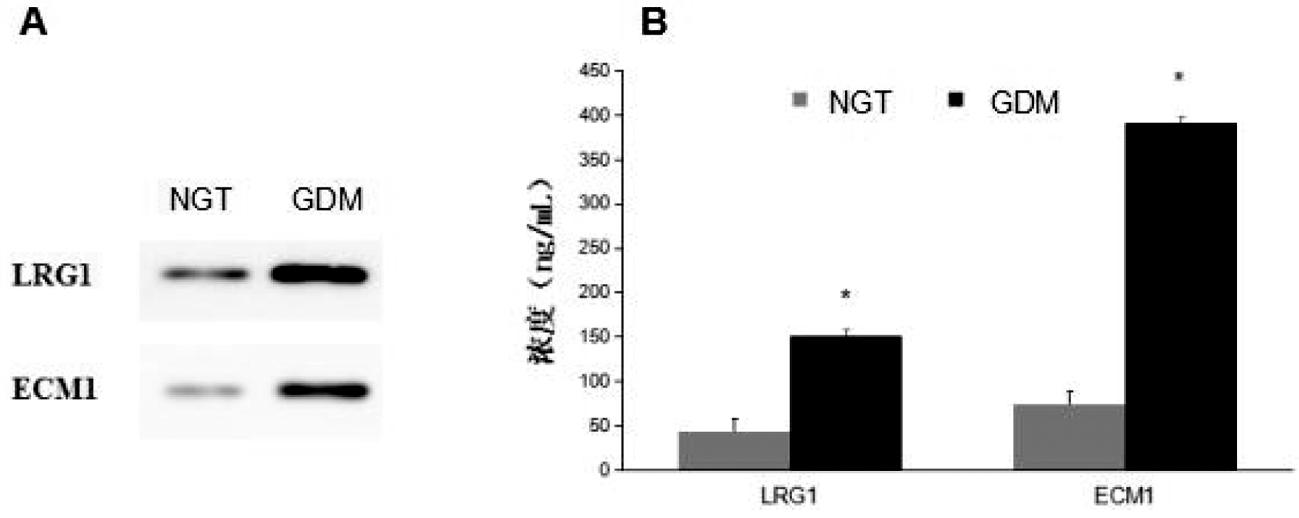
图1 外泌体LRG1和ECM1在不同组脐带血中表达情况(*P<0.05)
讨论
GDM是妊娠期间发生的严重并发症,能引起循环、神经内分泌系统等器官功能损伤甚至衰竭,是孕产妇死亡的重要因素[12]。目前对于GDM的发病机制尚未阐明,大多认为血管内皮功能紊乱是其重要的病理变化特征[13]。妊娠期间孕妇胎盘会分泌一些外泌体参与妊娠期间母体和胎儿的免疫调节、子宫螺旋动脉重塑以及胎盘屏障形成等,在维持正常妊娠过程中起到关键作用[15]。研究表明,GDM的发生与胎盘释放的大量激素、细胞因子、胎盘特异性蛋白等物质密切相关[16]。外泌体是纳米级胞外囊泡,有特异性分子如CD63包裹,能选择性的将携带的生物信息物质转移到靶细胞发挥作用。目前,胎盘来源外泌体在妊娠期高血压,高血糖等致病机制研究中深受关注。
本研究从脐带血中成功提取到外泌体,通过检测外泌体特异性相关蛋白CD63,发现GDM组脐带血中外泌体含量明显高于NGT组(P<0.05),提示孕期外泌体含量显著高于孕期正常范围,可作为预测和诊断GDM的一项生物标志物。胎盘来源外泌体(placental alkaline phosphatase,PLAP)是一种主要分布在胎盘的糖基化碱性磷酸酶,通过检测PLAP含量可以反应胎盘来源外泌体的数量[17]。本研究检测了PLAP数量的变化,结果显示,GDM组脐带血PLAP含量明显高于NGT组(P<0.05),提示PLAP可能在GDM的预测和早期诊断中发挥作用。已有研究发现,LRG1和ECM1在促进胎盘血管生成发挥重要作用,与糖尿病发生存在关系[18],但是脐带血中相关研究甚少。本研究从两组孕产妇脐带血中均检测到了LRG1和ECM1外泌体表达,并发现GDM组中LRG1和ECM1外泌体含量均明显高于NGT组(P<0.05)。在体内外实验研究结果均表明LRG1和ECM1外泌体在促进妊娠期糖尿病孕妇胎盘血管生成中起到重要作用[18],这与本研究结果一致。综上所述,外泌体LRG1和ECM1高表达,可能通过调节胎盘血管生成引起妊娠期血糖异常,有可能成为GDM疾病治疗靶点。由于本研究样本量较少,因此外泌体LRG1和ECM1与GDM之间的关系还需要深入研究。
1 Marathe PH,Gao HX,Close KL.American diabetes association standards of medical care in diabetes 2017.J Diabetes,2017,9:320-324.
2 Liu Q,Xia W,Xiong X,et al.Associations of gestational diabetes mellitus and excessive gestational weight Gain with offspring obesity risk.Curr Med Sci,2022,42:520-529.
3 Sacks DA,Hadden DR,Maresh M,et al.Frequency of gestational diabetes mellitus at collaborating centers based on IADPSG consensus panel-recommended criteria:the Hyperglycemia and Adverse Pregnancy Outcome(HAPO) Study.Diabetes Care,2012,35:526-528.
4 Noever K,Schubert J,Reuschel E,et al.Changes in Maternal Body Mass Index,Weight Gain and Outcome of Singleton Pregnancies from 2000 to 2015:A Population-based Retrospective Cohort Study in Hesse/Germany.Geburtshilfe Frauenheilkd,2020,80:508-517.
5 Ghafourian M,Mahdavi R,Akbari Jonoush Z,et al.The implications of exosomes in pregnancy:emerging as new diagnostic markers and therapeutics targets.Cell Commun Signal,2022,20:51.
6 Gurunathan S,Kang MH,Song H,et al.The role of extracellular vesicles in animal reproduction and diseases.J Anim Sci Biotechnol,2022,13:62.
7 张利玲,安昱静,张肖,等.妊娠糖尿病患者血清LRG1和CCL2水平对产后血糖转归的预测价值.临床和实验医学杂志,2024,23:1192-1196.
8 Freedman BR,Bade ND,Riggin CN,et al.The(dys)functional extracellular matrix.Biochim Biophys Acta,2015,1853:3153-3164.
9 Kim SH,Turnbull J,Guimond S.Extracellular matrix and cell signalling:the dynamic cooperation of integrin,proteoglycan and growth factor receptor.J Endocrinol,2011,209:139-151.
10 Silver FH,DeVore D,Siperko LM.Invited Review:Role of mechanophysiology in aging of ECM:effects of changes in mechanochemical transduction.J Appl Physiol(1985),2003,95:2134-2141.
11 Jacobsen DP,Lekva T,Moe K,et al.Pregnancy and postpartum levels of circulating maternal sHLA-G in preeclampsia.J Reprod Immunol,2021,143:103249.
12 Cvitic S,Novakovic B,Gordon L,et al.Human fetoplacental arterial and venous endothelial cells are differentially programmed by gestational diabetes mellitus,resulting in cell-specific barrier function changes.Diabetologia,2018,61:2398-2411.
13 孔丽丽.GSK3β抑制剂对糖尿病肾病大鼠肾组织TGF-β1和血清PAI-1表达的影响.吉林大学,2012.
14 Sweeting A,Wong J,Murphy HR,et al.A clinical update on gestational diabetes mellitus.Endocr Rev,2022,43:763-793.
15 李玉静,刁振宇,薛平平,等.血清中胎盘来源外泌体的分离与鉴定.医学研究生学报,2015:632-636.
16 郑芳,肖新益.miR-22-3p在妊娠期糖尿病患者胎盘外泌体中的表达及其对血管内皮细胞功能的影响.广西医科大学学报,2021,38:1477-1484.
17 Truong G,Guanzon D,Kinhal V,et al.Oxygen tension regulates the miRNA profile and bioactivity of exosomes released from extravillous trophoblast cells-Liquid biopsies for monitoring complications of pregnancy.PLoS One,2017,12:e0174514.
18 Yao J,Chang X,He Q,et al.Exosome enriched leucine-rich alpha-2-glycoprotein-1 and extracellular matrix protein 1 proteins induce abnormal placental angiogenesis in pregnant mice.Placenta,2023,143:45-53.