宫颈癌已经成为危害中国女性身体健康的主要妇科恶性肿瘤之一,且逐渐有年轻化的趋势。宫颈鳞状细胞癌(squamous cell carcinoma,SCC)是宫颈癌的最常见类型,宫颈鳞状上皮内病变(cervical squamous intraepithelial lesion,SIL)是导致宫颈鳞状细胞癌发生发展的重要因素。研究证实[1-2]在SIL由低度鳞状上皮内病变(low-grade cervical squamous intraepithelial lesion,LSIL)发展为宫颈癌是一个漫长持续的过程,在这个过程中高危型人乳头瘤病毒(High-risk human papillomavirus,HR-HPV)持续感染扮演重要角色[3]。随着宫颈癌研究的不断深入,人们发现阴道微生态紊乱也参与了阴道及宫颈疾病的发生发展过程[4]。血清25羟基维生素D[25(OH)D]是维生素D的主要代谢物,是外周血常见的因子,可有效反映体内维生素水平。研究表明[5-6],维生素D可对免疫系统抗原呈递细胞(Antigen-presenting cells,APC)发生作用来抑制肿瘤的发生发展,25(OH)D羟基化形成1,25(OH)D可有效抑制肿瘤细胞增殖,因此在子宫内膜癌、乳腺癌等妇科肿瘤中25(OH)D存在显著降低的情况,但在LSIL发生发展至宫颈癌的过程中是否存在异常,目前研究尚不多见。因此,本研究对LSIL患者血清25(OH)D、阴道微生态变化及HPV感染情况进行了检测,分析了各指标相关性及与LSIL发生发展的潜在联系,具体结果总结如下。
对象与方法
1.研究对象:选取本院2020年1月—2022年12月诊断为LSIL患者60例作为LSIL组,年龄21~62岁,平均(42.3±3.7)岁,孕次0~5次,平均(2.3±0.5)次,产次0~5次,平均(2.0±0.3)次。纳入标准为(1)月经规律,检查时非月经期;(2)经宫颈液基薄层细胞学(thinprep cytologic test,TCT)检测为LSIL;(3)近期无阴道上药、灌洗;(4)均自愿参与本研究并签署知情同意书。排除标准为(1)就诊时存在阴道不规律出血者;(2)妊娠哺乳期女性;(3)合并内分泌疾病、免疫系统疾病及恶性肿瘤者;(4)合并其他影响本研究的因素。另选取同期于本院接受HPV及阴道微生态检查的60例慢性宫颈炎患者作为慢性宫颈炎组及无宫颈病变的健康育龄女性60例作为对照组,研究对象均经知情同意,自愿参与本研究。其中慢性宫颈炎组年龄21~60岁,平均(41.9±3.2)岁,孕次0~5次,平均(2.4±0.4)次,产次0~4次,平均(2.0±0.4)次;对照组年龄22~60岁,平均(42.4±3.5)岁,孕次0~5次,平均(2.3±0.4)次,产次0~5次,平均(1.9±0.4)次。三组研究对象临床一般资料比较,差异无统计学意义,具有可比性。本研究取得北京电力医院医学伦理委员会批准通过(伦理号:2020033010326)。
2.研究方法:
(1)宫颈液基薄层细胞学检测。患者取膀胱截石位,一次性窥器充分暴露宫颈,先行细胞学采样,后行HPV采样,无菌棉拭子擦干净分泌物,放入装有保存液的样本管中待检。宫颈液基薄层细胞学检测采用液基波层细胞学(thinprep cytologic test,TCT)检测,并依照TBS分类法诊断,分为不典型鳞状细胞(atypical squamous cells,ASC)、未见上皮内病变或恶性细胞(negative for intraepithelial lesion or malignancy,NILM)两类。ASC包括低度鳞状上皮内病变(LSIL)、高度鳞状上皮内病变(HSIL)、意义不明确的不典型鳞状细胞(atypical squamous cells of undetermined significance,ASC-US)、不能除外高级别鳞状上皮内病变不典型鳞状细胞(atypical squamous cells, cannot exclude high-gradesquamous intraepithelial lesion,ASC-H)、鳞状细胞癌(SCC)。
(2)HPV检测。利用凯普HPV分型检测试剂系统(购自广东凯普生物科技股份有限公司),采用反向点杂交法聚合酶链式反应(polymerase chain reaction,PCR)检测和鉴别低危型HPV-6、11、42、43、44、81,高危型HPV-16、18、31、33、35、39、45、51、52、53、56、58、59、66、68。
(3)阴道微生态检测。患者取膀胱截石位,一次性窥器充分暴露宫颈,采用无菌棉拭子从引导侧壁上1/3处取适量分泌物放入特定样本管中送检。检测内容包括菌群密度、菌群多样性、滴虫、乳酸杆菌、加德纳菌、pH值、孢子、唾液酸苷酶(sialidase,SNA)阳性、白细胞酯酶(leukocyte esterase,LE)阳性、阴道清洁度、Nugent评分、Donders评分等。其中,SNA阳性为厌氧菌感染,LE阳性存在炎症反应;Nugent评分≤3分为正常,4~6分为中间型细菌性阴道病,≥7分为细菌性阴道病;Donders评分≥3分为细菌性阴道炎。患者上述检测内容中任意3项及以上同时异常即为阴道微生态异常,少于3项定义为正常。
(4)血清25(OH)D检测。所有研究对象抽取5 mL空腹静脉血,采用贝克曼DX-800化学发光全自动免疫分析仪及配套试剂盒(购自美国贝克曼公司)检测血清25(OH)D水平。
3.统计学处理:本研究数据采用SPSS 20.0统计学软件进行数据分析,计数资料采用百分比(%)表示,组间比较采用χ2检验;计量资料采用均值±标准差表示,组间两两比较采用t检验,三组及以上比较采用F检验;Logistic回归分析影响LSIL发生发展的风险因素。P<0.05为差异具有统计学意义。
结果
1.三组研究对象血清25(OH)D水平比较:对照组、慢性宫颈炎组、LSIL组血清25(OH)D水平比较,差异具有统计学意义,且呈逐渐降低趋势(P<0.05)。见表1。
表1 三组研究对象血清25(OH)D水平比较

组别例数25(OH)D(ng/mL)∗对照组6057.9±5.4#慢性宫颈炎组6050.3±5.6#LSIL组6044.2±5.1#
三组比较,*P<0.05;三组之间两两比较,#P<0.05
2.三组研究对象阴道微生态指标比较:对照组、慢性宫颈炎组、LSIL组三组间菌群密度、菌群多样性、滴虫、乳酸杆菌、加德纳菌、pH值、孢子、唾液酸苷酶(SNA)阳性、白细胞酯酶(LE)阳性、阴道清洁度、Nugent评分、Donders评分异常情况比较差异有统计学意义,除滴虫、加德纳菌、孢子、阴道清洁度以外,其余指标的异常率三组间呈上升趋势(P<0.05)。见表2。
表2 三组阴道微生态指标异常比例比较 [例(%)]
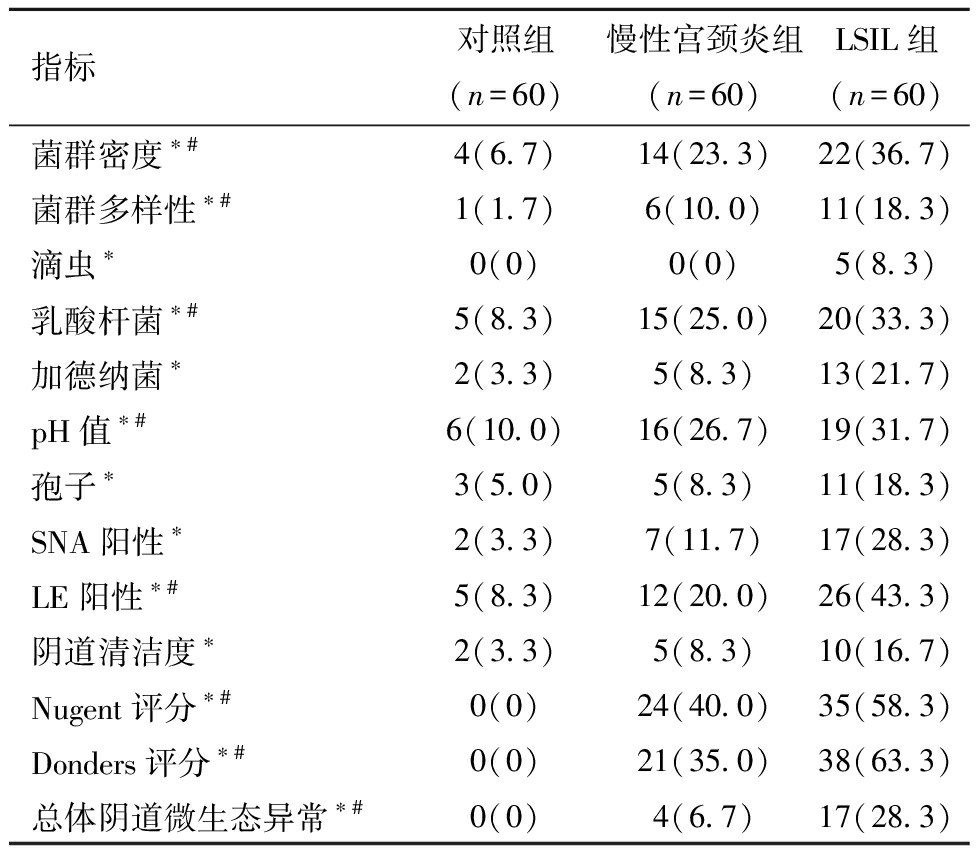
指标对照组(n=60)慢性宫颈炎组(n=60)LSIL组(n=60)菌群密度∗#4(6.7)14(23.3)22(36.7)菌群多样性∗#1(1.7)6(10.0)11(18.3)滴虫∗0(0)0(0)5(8.3)乳酸杆菌∗#5(8.3)15(25.0)20(33.3)加德纳菌∗2(3.3)5(8.3)13(21.7)pH值∗#6(10.0)16(26.7)19(31.7)孢子∗3(5.0)5(8.3)11(18.3)SNA阳性∗2(3.3)7(11.7)17(28.3)LE阳性∗#5(8.3)12(20.0)26(43.3)阴道清洁度∗2(3.3)5(8.3)10(16.7)Nugent评分∗#0(0)24(40.0)35(58.3)Donders评分∗#0(0)21(35.0)38(63.3)总体阴道微生态异常∗#0(0)4(6.7)17(28.3)
三组比较,*P<0.05;#P趋势<0.05
3.慢性宫颈炎组、LSIL组HPV感染亚型比较:对照组、慢性宫颈炎组、LSIL组HPV低危型感染率比较差异无统计学意义。LSIL组HPV高危型HPV-16、18等11个亚型的感染率与慢性宫颈炎组比较,差异具有(临界)统计学意义,见表3。
表3 慢性宫颈炎组与LSIL组HPV感染亚型比较 [例(%)]
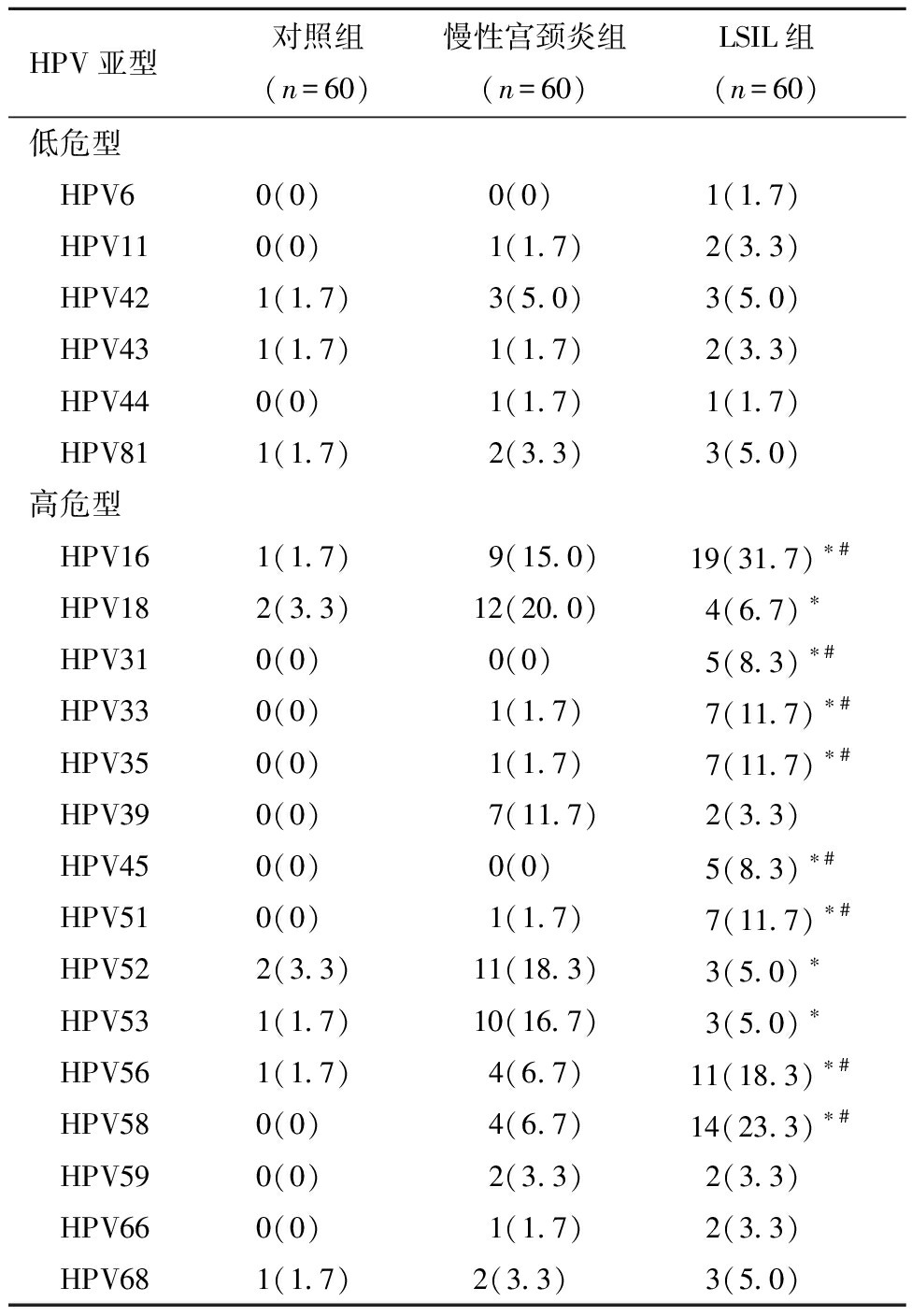
HPV亚型对照组 (n=60) 慢性宫颈炎组 (n=60) LSIL组 (n=60) 低危型 HPV60(0)0(0)1(1.7) HPV110(0)1(1.7)2(3.3) HPV421(1.7)3(5.0)3(5.0) HPV431(1.7)1(1.7)2(3.3) HPV440(0)1(1.7)1(1.7) HPV811(1.7)2(3.3)3(5.0)高危型 HPV161(1.7)9(15.0)19(31.7)∗# HPV182(3.3)12(20.0)4(6.7)∗ HPV310(0)0(0)5(8.3)∗# HPV330(0)1(1.7)7(11.7)∗# HPV350(0)1(1.7)7(11.7)∗# HPV390(0)7(11.7)2(3.3) HPV450(0)0(0)5(8.3)∗# HPV510(0)1(1.7)7(11.7)∗# HPV522(3.3)11(18.3)3(5.0)∗ HPV531(1.7)10(16.7)3(5.0)∗ HPV561(1.7)4(6.7)11(18.3)∗# HPV580(0)4(6.7)14(23.3)∗# HPV590(0)2(3.3)2(3.3) HPV660(0)1(1.7)2(3.3) HPV681(1.7)2(3.3)3(5.0)
与慢性宫颈炎组比较,*P≤0.05;与对照组比较,#P<0.05
4.HPV阴性组和HPV阳性组血25(OH)D水平:根据HPV感染情况分为HPV阴性组和HPV阳性组,HPV阳性组慢性宫颈炎及LSIL患者较阴性组血25(OH)D均出现不同程度下降,差异具有统计学意义。见表4。
表4 HPV阴性组和HPV阳性组血25(OH)D水平比较(ng/mL)

指标慢性宫颈炎组∗HPV阴性(n=16)HPV阳性(n=44)LSIL组∗HPV阴性(n=27)HPV阳性(n=33)25(OH)D54.6±3.648.6±3.447.2±3.342.1±3.9
HPV阳性组与HPV阴性组比较,*P<0.05
5.LSIL患者HPV阴性组和HPV阳性组阴道微生态指标比较:LSIL患者HPV阴性组和HPV阳性组菌群密度、菌群多样性、滴虫、乳酸杆菌、加德纳菌、pH值、孢子、SNA阳性、LE阳性、阴道清洁度、Nugent评分、Donders评分异常比例比较,差异具有统计学意义。见表5。
表5 LSIL患者HPV阴性组和HPV阳性组阴道微生态指标异常比例比较
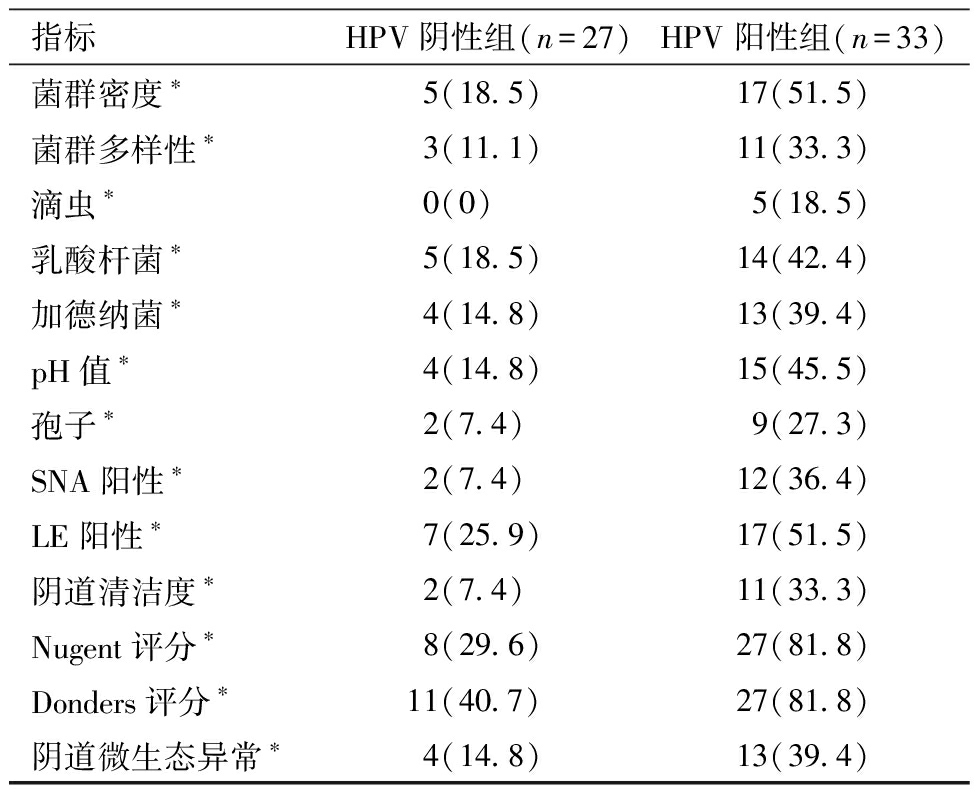
指标HPV阴性组(n=27)HPV阳性组(n=33)菌群密度∗5(18.5)17(51.5)菌群多样性∗3(11.1)11(33.3)滴虫∗0(0)5(18.5)乳酸杆菌∗5(18.5)14(42.4)加德纳菌∗4(14.8)13(39.4)pH值∗4(14.8)15(45.5)孢子∗2(7.4)9(27.3)SNA阳性∗2(7.4)12(36.4)LE阳性∗7(25.9)17(51.5)阴道清洁度∗2(7.4)11(33.3)Nugent评分∗8(29.6)27(81.8)Donders评分∗11(40.7)27(81.8)阴道微生态异常∗4(14.8)13(39.4)
两组比较,*P<0.05
6.LSIL发生发展的多因素回归分析:对单因素分析存在统计学意义的因素进行赋值,阴道微生态正常=0、异常=1,HPV低危型/未感染=0、高危型HPV感染=1,25(OH)D≤50.3 ng/mL=0、>50.3 ng/mL=1,分析LSIL(LSIL组=1,健康对照组=0)发生发展的风险因素,Logistic回归分析结果表明阴道微生态异常、高危型HPV感染和25(OH)D降低为LSIL的风险因素(P<0.05)。见表6。
表6 LSIL发生发展的Logistic多因素回归分析
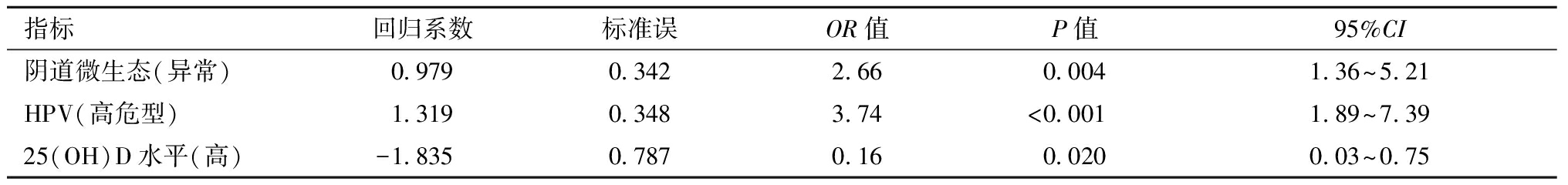
指标回归系数标准误OR值P值95%CI阴道微生态(异常)0.9790.3422.660.0041.36~5.21HPV(高危型)1.3190.3483.74<0.0011.89~7.3925(OH)D水平(高)-1.8350.7870.160.0200.03~0.75
讨论
宫颈癌是生殖系统病变,严重威胁女性健康。早期宫颈癌无典型临床症状,许多患者确诊时已处于中晚期,预后往往较差。因此,宫颈癌早期病变的筛查、预防和治疗具有重要意义。多项研究证实[7-8],高危型HPV感染是发生宫颈细胞癌的重要影响因素之一。HPV分为高风险和低风险亚型,其中高风险亚型(如16型和18型)与宫颈癌和低度鳞状上皮内病变的发生更为密切。HPV病毒可以感染宫颈上皮细胞,导致细胞的异常增殖和改变,进而引发低度鳞状上皮内病变,继而向宫颈细胞癌发展。本研究中,相较于慢性宫颈炎组,LSIL患者高危型HPV16、18、31、33、35、45、51、52、53、56、58比较差异显著,提示LSIL患者高危型HPV感染更加普遍,LSIL的发生发展与高危型HPV持续感染存在一定联系。
25(OH)D为维生素D的代谢产物,近年来随着研究的深入,越来越多研究表明25(OH)D与心血管疾病、免疫系统疾病、内分泌疾病及恶性肿瘤等的发生发展存在密切关系[9]。25(OH)D经羟基化形成1,25(OH)D可与维生素D受体(vitamin D receptor,VDR)结合抑制恶性肿瘤细胞的浸润、增殖和分化。另有研究证实[10],机体1,25(OH)D水平越低,宫颈癌分化程度越高。本研究中,对照组、慢性宫颈炎组、LSIL组血清25(OH)D水平呈逐渐降低趋势,提示血清25(OH)D水平降低与宫颈病变的发生发展关系密切。研究显示[11],血清25羟基维生素D水平与低度鳞状上皮内病变之间可能存在一定的关联,低血清25(OH)D水平与低度鳞状上皮内病变的发生和进展有关。维生素D具有抗炎和免疫调节作用,可以抑制宫颈细胞的异常增殖和炎症反应,从而可能降低低度鳞状上皮内病变的风险。因而,对LSIL患者血清25(OH)D水平检测可能对于宫颈鳞状上皮内病变和宫颈癌的预防和治疗起到一定辅助作用。
低度鳞状上皮内病变与阴道微生态变化之间存在一定的关联。阴道微生态是指在阴道内存在的各种微生物的群落,包括细菌、真菌和其他微生物。研究表明[12],阴道微生态的改变可以影响宫颈上皮细胞的健康和功能。阴道微生态失衡可引发局部内分泌、免疫异常,导致局部免疫抑制状态,宫颈局部免疫力下降,进而可能导致宫颈上皮细胞的异常变化,引发低度鳞状上皮内病变的发生。一些研究发现[13-15],阴道微生态失衡可导致HPV感染持续时间延长,从而增加低度鳞状上皮内病变的风险。阴道微生态失衡可能导致阴道炎症的发生,进而引发炎性反应。炎性反应可促进宫颈上皮细胞的异常变化,进一步增加低度鳞状上皮内病变的风险。本研究中,LSIL患者HPV阴性组和HPV阳性组菌群密度、菌群多样性、滴虫、乳酸杆菌、加德纳菌、pH值、孢子、SNA阳性、LE阳性、阴道清洁度、Nugent评分、Donders评分异常比例比较,差异具有统计学意义。提示LSIL患者阴道微生态失衡与高危型HPV持续感染存在关联。同时,HPV阳性组慢性宫颈炎及LSIL患者较阴性组血清25(OH)D均出现不同程度下降,提示高危型HPV持续感染促使LSIL患者血清25(OH)D降低。回归分析结果表明阴道微生态异常、高危型HPV感染和25(OH)D降低为LSIL的风险因素。因此,本研究推测阴道微生态失衡及HPV感染导致宫颈病变乃至LSIL的发生发展,引发患者血清25(OH)D进一步降低,形成恶性循环,使得宫颈癌的发生风险升高。综上所述,血清25(OH)D降低、阴道微生态变化及HPV感染与宫颈病变关系密切,可能是LSIL患者HPV持续感染的发生发展的危险因素。
1 文天萌,赵爽,赵雪莲,等.不同级别宫颈上皮内病变治疗妇女的生命质量调查.中国妇产科临床杂志,2023,24:144-148.
2 Major AL,Mayboroda I,Riger A.Successful Preventive Treatment of Oncogenic Transforming HPV Infections in Low-Grade Cytology(ASC-US/LSIL) Patients with an Adsorptive and Antioxidant Vaginal Gel.J Clin Med,2023,12:4142.
3 Yetian R,Hui L,Min L,et al.A retrospective analysis of human papillomavirus(HPV) prevalence and genotype distribution among 25,238 women in Shanghai,China revealed the limitations of current HPV-based screening and HPV vaccine.Cancer Epidemiol,2023,84:102372.
4 张立晶,吴萍,骆婷婷.不同级别宫颈鳞状上皮内病变患者子宫颈分泌物的微生态观察.中国妇幼保健,2023,38:2755-2758.
5 Li D,Liu Y,Kong D,et al.Vitamin D Receptor Gene Polymorphisms and the Risk of CIN2+ in Shanxi Population.Biomed Res Int,2022,2022:6875996.
6 吴晨晨,徐静.微量元素锌、硒、铜、铁及抗氧化维生素在宫颈病变及宫颈癌中的作用.中国医药科学,2022,12:64-67.
7 钟辉,化金金,曹颖,等.多肿瘤抑制基因、细胞增殖标志指数及表皮生长因子受体与宫颈鳞状上皮内病变患者分级的相关性.中国性科学,2021,30:55-59.
8 李靖,刘慧玲,郑胜英.阴道微环境和HPV感染与宫颈上皮内瘤变的相关性分析.中南医学科学杂志,2022,50:926-929.
9 尹俊杨,叶元.维生素D及其受体在妇科癌症中的研究进展.现代肿瘤医学,2022,30:1129-1133.
10 Phuthong S,Settheetham-Ishida W,Natphopsuk S,et al.Genetic Polymorphisms of Vitamin D Receptor Gene are Associated with Cervical Cancer Risk in Northeastern Thailand.Asian Pac J Cancer Prev,2020,21:2935-2939.
11 Avila E,Noriega-Mejía BJ,González-Macías J,et al.The Preventive Role of the Vitamin D Endocrine System in Cervical Cancer.Int J Mol Sci,2023,24:8665.
12 郭瑞霞,陈俊杰,杜文君,等.外阴鳞状上皮内病变患者合并宫颈阴道上皮内病变及HPV感染的临床特点.郑州大学学报(医学版),2020,55:454-458.
13 宋丽娟,杨文翠,狄晓鸿,等.子宫颈鳞状上皮内病变中BAG-1、MCM2表达及其与p16、HR-HPV的关系.临床与实验病理学杂志,2019,35:1036-1041.
14 Chen L,Zhu K,Chen H,et al.Correlation of immediate prevalence of cervical squamous cell precancers and cancers with HPV genotype and age in women with LSIL cytology:A retrospective analysis of 1617 cases.Diagn Cytopathol,2024,52:10-15.
15 黄聪.阴道微生态环境、阴道免疫状态和人乳头状瘤病毒感染与宫颈病变的相关性.慢性病学杂志,2020,21:1845-1848.