病例资料
家系1:先证者为女性,现4岁,于2019年1月8日孕37周2天顺产出生,出生史无异常,出生时体重3 250 kg,身长52 cm。父母体健,非近亲结婚,其母孕期无特殊用药史,无污染物和放射线接触史。查体:患儿体重15 kg,身高115 cm,现全面性发育迟缓,语言发育落后,只能单字发音如“ba、ma”,能听懂简单指令但不能交流。19个月能够独立行走,但双下肢肌张力高,膝盖无法弯曲,现行走时喜上举上肢,左右摇摆走路。逗之可引发大笑,行为活跃,注意力不集中,喜欢玩水,对热的敏感性增加,出生后偶有眼角和手指的震颤,入睡困难并且睡眠质量差,予口服左乙拉西坦治疗,睡眠状态有所好转。辅助检查:肝肾功能、电解质未见异常,血尿代谢筛查无明显异常,头颅核磁平扫未见明显异常。
经孕妇及其家属知情同意,抽取患儿外周血2 mL送检,行全外显子测序分析提示NM_000462.3;UBE3A c.1365_1377del(p.Asn455LysfsTer11)突变,为移码突变(见图1),UBE3A c.1365_1377del(p.Asn455LysfsTer11),gnomAD数据库人群频率未见,gnomAD_EAS人群数据库东亚人群频率未见,依据美国医学遗传学和基因组学会(ACMG)标准[1]对其进行致病性分析,其变异性质为PS2+PM2+PM4+PP1+PP4,为致病性变异;抽取父母外周血2 mL送检,其母亲基因结果提示NM_000462.3;UBE3A c.1365_1377del(p.Asn455LysfsTer11)杂合突变,其父亲该位点为野生型。患儿母亲再次怀孕,孕19周于本院生殖遗传科行羊膜腔穿刺术,取羊水标本进行基因检测,结果示胎儿UBE3A c.1365_1377位点未见异常(见图1),STR遗传位点分析显示无母体细胞污染,出生后新生儿未进一步进行基因验证。
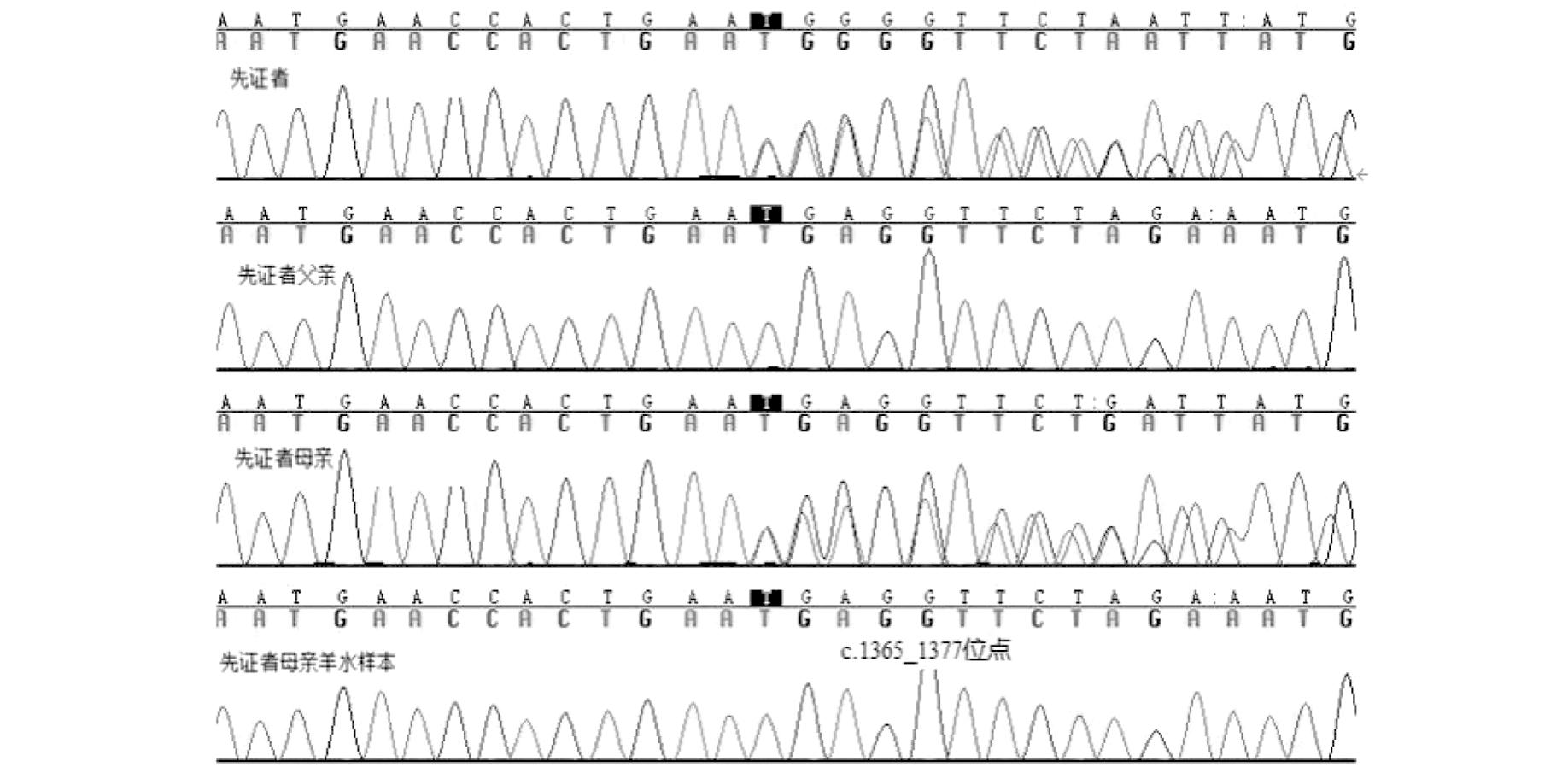
图1 家系1先证者、先证者父亲、先证者母亲、先证者母亲羊水样本UBE3A基因c.1365_1377位点Sanger测序结果
家系2:先证者为男性,现9岁3个月,于2015年10月12日顺产出生,出生史无异常,父母体健,非近亲结婚,其母孕期无特殊用药史,无污染物和放射线接触史,患儿出生后,1岁左右会坐,2岁左右会走但步态不稳,4岁左右癫疒间发作,主要表现为玩耍时突然跌倒,意识丧失、双眼紧闭、头后仰,持续约1 min左右。患儿语言系统发育落后,不能交流只能用简单的手势及表情来表达意愿。查体:体重21 kg,身高121 cm,双眼斜视,常无原因的笑,容易兴奋,走路左右摇摆,步态不稳,心肺腹查体未见异常,四肢肌力及肌张力尚可,病理征均阴性。辅助检查:肝肾功能、电解质、血氨、血同型半胱氨酸和甲状腺功能均未见异常,血尿代谢筛查无异常,头颅核磁平扫未见异常,脑电图提示疒间样放电。
经孕妇及家属知情同意,抽取患儿外周血2 mL送检,行全外显子测序分析提示NM_130838; UBE3A c.1866_1867insA(Ile623Alafs*4),为移码突变(见图2),该突变在ClinVar数据库中暂无报道,也未检索到关于该位点突变致病的相关文献,在千人数据库、gnomAD数据库和ExAC数据库中人群频率为无,依据美国医学遗传学和基因组学会(ACMG)标准[1]对其进行致病性分析,其变异性质为PS2+PM2+PM4+PP1+PP4,为致病性变异,并抽取患儿母亲、父亲、外公、外婆外周血2 mL送检,其母亲和外公基因检测结果提示UBE3A基因c.1866_1867insA(Ile623Alafs*4),为移码突变,其父亲和外婆该基因位点未见异常。先证者母亲再次怀孕,孕12+4周于本院生殖遗传科行绒毛膜穿刺术,取胎儿胎盘绒毛标本进行基因检测,结果提示UBE3A基因c.1866_1867位点未见异常(见图2),STR遗传位点分析显示无母体细胞污染,出生后新生儿未进一步进行基因验证。
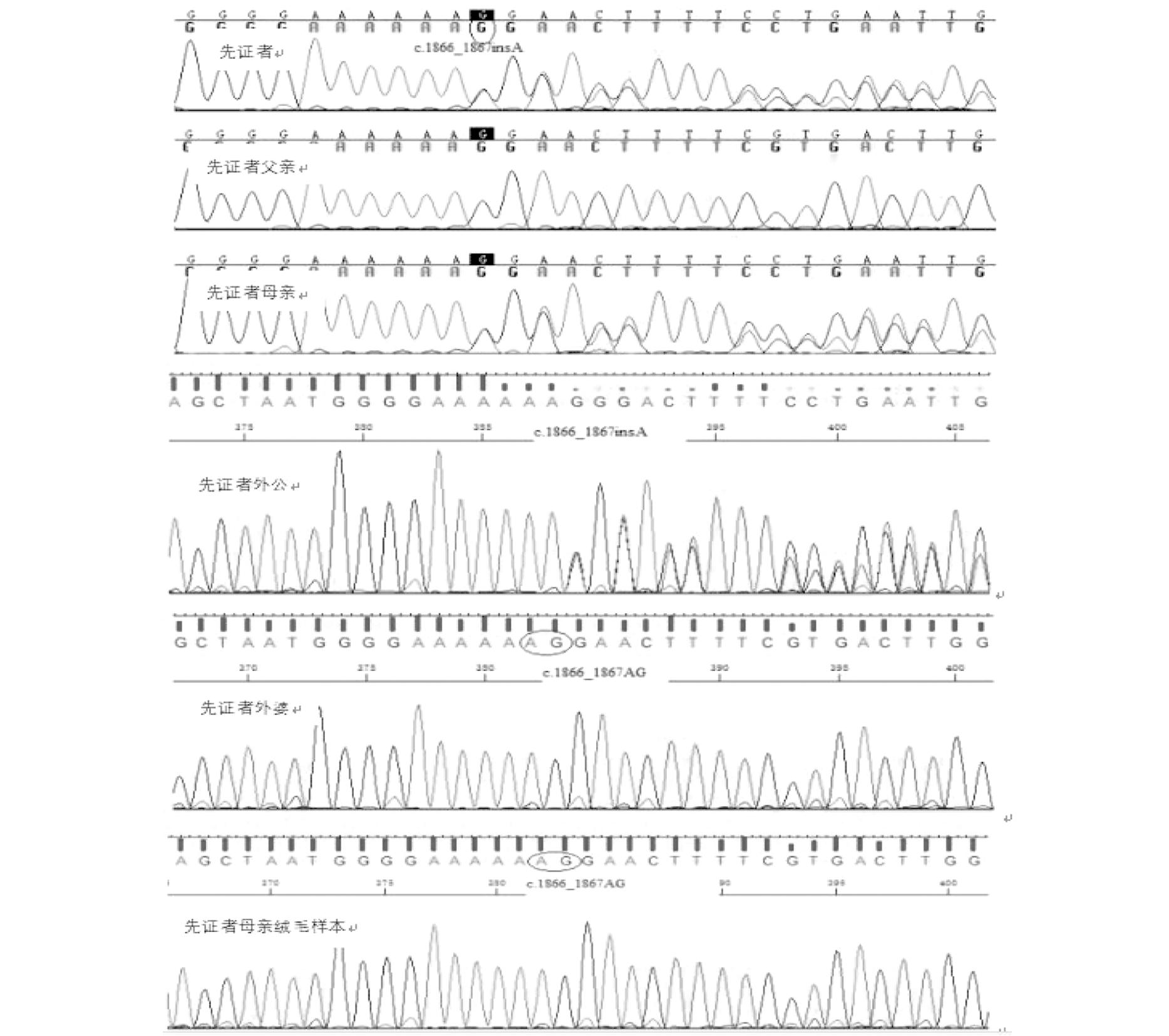
图2 家系2先证者、先证者父亲、先证者母亲、先证者外公、先证者外婆和先证者母亲绒毛样本UBE3A基因c.1866_1867位点Sanger测序结果
本研究经过了河北省人民医院伦理委员会的审核通过(伦理号:2024-LW-009)。
讨论
AS是一种罕见的神经系统发育障碍的遗传性疾病,由Harry Angelman 1965年首次报道,发病率为1/15 000,以精神发育迟滞、语言障碍、运动及平衡障碍、快乐行为、小头畸形、癫疒间等为主要的临床表现[2]。AS的致病基因是UBE3A基因,该基因编码的蛋白被称为E6-AP蛋白,其属于E3泛素连接酶的HECT结构域超家族,它可以通过其C端HECT结构域(第518-875位氨基酸)催化泛素与各种底物共价附着,对目标蛋白进行泛素化修饰,通过蛋白酶体的降解作用调节蛋白表达水平;其次也可以作为甾醇类激素受体的共激活因子来调节下游基因的转录水平[3]。E6-AP在脑组织中被广泛表达,主要分布于神经元的轴突和树突[4],在神经系统的发育和成熟过程中充当转录激活因子,参与调控细胞周期、突触传递及突触可塑性等过程[5-6],说明E6-AP蛋白可以维持神经元的正常功能。AS常见的分子缺陷机制主要包括四种,分别为染色体15q11-13区域缺失、染色体15q11-13区域父源性单亲二体印记中心的缺陷和UBE3A基因变异。其中母源性染色体15q11.2-q13区域5-7Mb的缺失是与AS相关的最常见的遗传机制,约75%的患者是由该区段缺失所致,UBE3A基因突变比较少见,仅占10%左右[7]。
UBE3A基因位于人类染色体15q11.2-13区域,该区域存在一组印记基因,UBE3A基因在印记基因的调控下差异性表达,在印记区域结构中基因的甲基化修饰和表达是由位于小分子核糖蛋白多肽N(SNRPN)上游区域的顺式元件调控的[8],小核仁RNA宿主基因14(SNHG14)位于SNRPN启动子处,该基因能够表达一种非编码反义转录物,SNHG14的转录延伸到UBE3A基因并干扰其在父系染色体上的转录,所以父系UBE3A基因沉默,由于母系该基因区域能够被甲基化修饰而影响了SNHG14基因的表达,该基因编码的反义转录物无法干扰母源性UBE3A基因,所以母源性UBE3A基因能够正常转录[9]。上述遗传方式一般仅存在于脑组织中,在人成纤维细胞及淋巴细胞中,UBE3A基因呈双等位基因表达模式[10-11]。本次研究中两个家系患儿UBE3A基因杂合变异,变异均来源于母亲,但母亲没有AS相关临床表现,母亲的UBE3A基因变异遗传其父亲但是父系UBE3A基因沉默,无法转录,所以母亲表型正常,符合母系印记基因遗传特点。
本次研究中涉及到的两个AS家系均为UBE3A基因突变所致,家系1患儿2岁左右全面发育迟缓,语言和运动系统发育落后,抽取外周血进行全外显子测序分析提示UBE3Ac.1365_1377del(p.Asn455LysfsTer11)杂合突变,为移码突变,使第455位的天冬酰胺变为赖氨酸,并且提前引入了一个终止密码子,将UBE3A基因表达产物由876个氨基酸减少到465个氨基酸。家系1针对该基因位点抽取患儿父亲和患儿母亲外周血进行Sanger测序验证,一代验证结果显示先证者携带杂合变异,变异来源于母亲,父亲未携带。家系2患儿1岁会坐,2岁左右会走但步态不稳,4岁后主要表现为癫疒间发作,抽取外周血进行全外显子测序分析提示UBE3A c.1866_1867insA(Ile623Alafs*4),为移码突变,使第623位的异亮氨酸变成丙氨酸,之后的第四个氨基酸变成了终止密码子。家系2针对该基因位点抽取患儿父亲、母亲、外公、外婆的外周血进行Sanger测序验证,验证结果显示患儿母亲和外公该基因位点为杂合突变,患儿父亲和外婆该基因位点未见异常。上述两个家系UBE3A基因突变均导致了终止密码子的提前引入,终止密码子的提前引入会导致UBE3A基因编码的E6-AP蛋白减少甚至消失,从而整体上影响患者的神经精神系统。研究者在约5%~10%的AS患者中发现了UBE3A基因突变,目前已经报道了73种影响UBE3A基因的不同致病性突变,大多数突变影响了HECT连接酶结构域,至今没有发现热点突变[12-13]。
目前没有针对AS患者的特异性基因治疗方法,主要是侧重于患儿护理、康复和抗癫疒间治疗。Du等[14]研究表明约49.75%的AS患儿需要一名家长全程陪同,这不仅给AS患者家庭带来沉重的精神压力也影响了家庭的生活水平。UBE3A基因突变型AS患儿大多数是新发突变导致,也存在家系遗传[15]。新发突变再发风险很低约<1%,如果基因检测结果提示变异遗传自母亲,那么AS患儿的再发风险可以达到50%[16],所以对于已经发现UBE3A基因突变并且母亲是突变携带者,如果有生育要求建议进行产前诊断或植入前遗传学诊断[17]。
综上所述,本文在2例AS家系中检测到了UBE3A基因位点移码突变,分别为UBE3Ac.1365_1377del(p.Asn455LysfsTer11)和UBE3Ac.1866_1867insA(Ile623Alafs*4),导致E6-AP蛋白功能缺失,出现了典型的AS症状。上述发现丰富了UBE3A基因的变异谱,也为相关家系的遗传咨询和产前诊断提供了线索。
利益冲突:所有作者均声明不存在利益冲突
志谢:北京航空医学研究所附属医院分子病理中心
1 Richards S,Aziz N,Bale S,et al.Standards and guidelines for the interpretation of sequence variants:a joint consensus recommendation of the American College of Medical Genetics and Genomics and the Association for Molecular Pathology.Genet Med,2015,17:405-424.
2 Yang L,Shu X,Mao S,et al.Genotype-Phenotype Correlations in Angelman Syndrome.Genes (Basel),2021,12:987.
3 Sen D,Voulgaropoulos A,Drobna Z,et al.Human Cerebral Organoids Reveal Early Spatiotemporal Dynamics and Pharmacological Responses of UBE3A.Stem Cell Reports,2020,15:845-854.
4 Meng L,Person RE,Beaudet AL.Ube3a-ATS is an atypical RNA polymerase II transcript that represses the paternal expression of Ube3a.Hum Mol Genet,2012,21:3001-3012.
5 Beasley SA,Kellum CE,Orlomoski RJ,et al.An Angelman syndrome substitution in the HECT E3 ubiquitin ligase C-terminal Lobe of E6AP affects protein stability and activity.PLoS One,2020,15:e0235925.
6 Ronchi VP,Klein JM,Haas AL.E6AP/UBE3A ubiquitin ligase harbors two E2~ubiquitin binding sites.J Biol Chem,2013,288:10349-10360.
7 LaSalle JM,Reiter LT,Chamberlain SJ.Epigenetic regulation of UBE3A and roles in human neurodevelopmental disorders.Epigenomics,2015,7:1213-1228.
8 Nakao M,Sutcliffe JS,Durtschi B,et al.Imprinting analysis of three genes in the Prader-Willi/Angelman region:SNRPN,E6-associated protein,and PAR-2 (D15S225E).Hum Mol Genet,1994,3:309-315.
9 Georgieva B,Atemin S,Todorova A,et al.Molecular-Genetic Diagnostics of Angelman Syndrome—The Bulgarian Experience.Acta Med Bulg,2020,47:9-16.
10 Samanta D.Epilepsy in Angelman syndrome:A scoping review.Brain Dev,2021,43:32-44.
11 Buiting K,Williams C,Horsthemke B.Angelman syndrome - insights into a rare neurogenetic disorder.Nat Rev Neurol,2016,12:584-593.
12 Luk H,Lo IF.Angelman syndrome in Hong Kong Chinese:A 20 years′ experience.Eur J Med Genet,2016,59:315-319.
13 Keute M,Miller MT,Krishnan ML,et al.Angelman syndrome genotypes manifest varying degrees of clinical severity and developmental impairment.Mol Psychiatry,2021,26:3625-3633.
14 Du X,Wang J,Li S,et al.An Analysis of Phenotype and Genotype in a Large Cohort of Chinese Children with Angelman Syndrome.Genes (Basel),2022,13:1447.
15 Keute M,Miller MT,Krishnan ML,et al.Angelman syndrome genotypes manifest varying degrees of clinical severity and developmental impairment.Mol Psychiatry,2021,26:3625-3633.
16 Clayton-Smith J,Laan L.Angelman syndrome:a review of the clinical and genetic aspects.J Med Genet,2003,40:87-95.
17 Markati T,Duis J,Servais L.Therapies in preclinical and clinical development for Angelman syndrome.Expert Opin Investig Drugs,2021,30:709-720.