□normal male; normal female;■male patient with mutation;●female patient with mutation;The arrow represents the proband; Slash represents deceased
normal female;■male patient with mutation;●female patient with mutation;The arrow represents the proband; Slash represents deceased
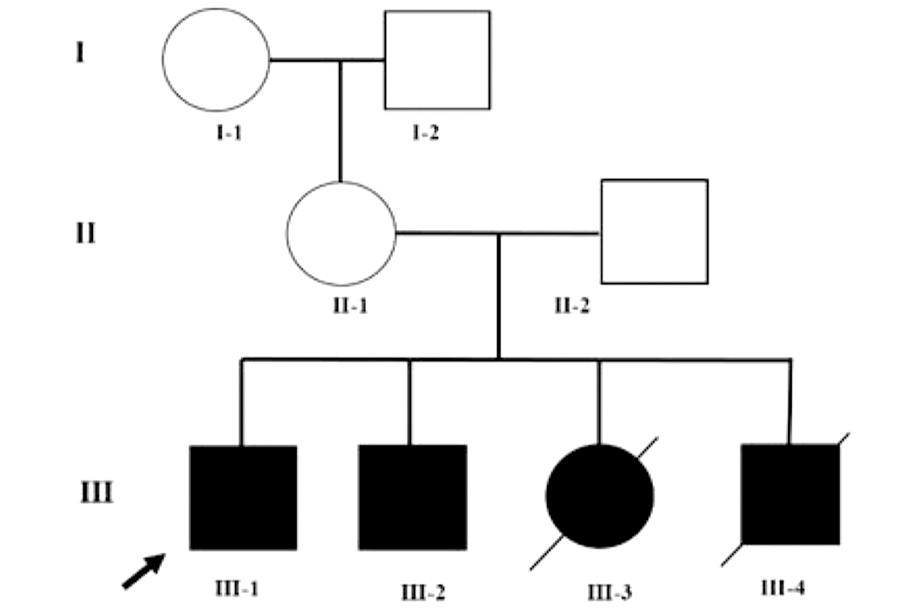
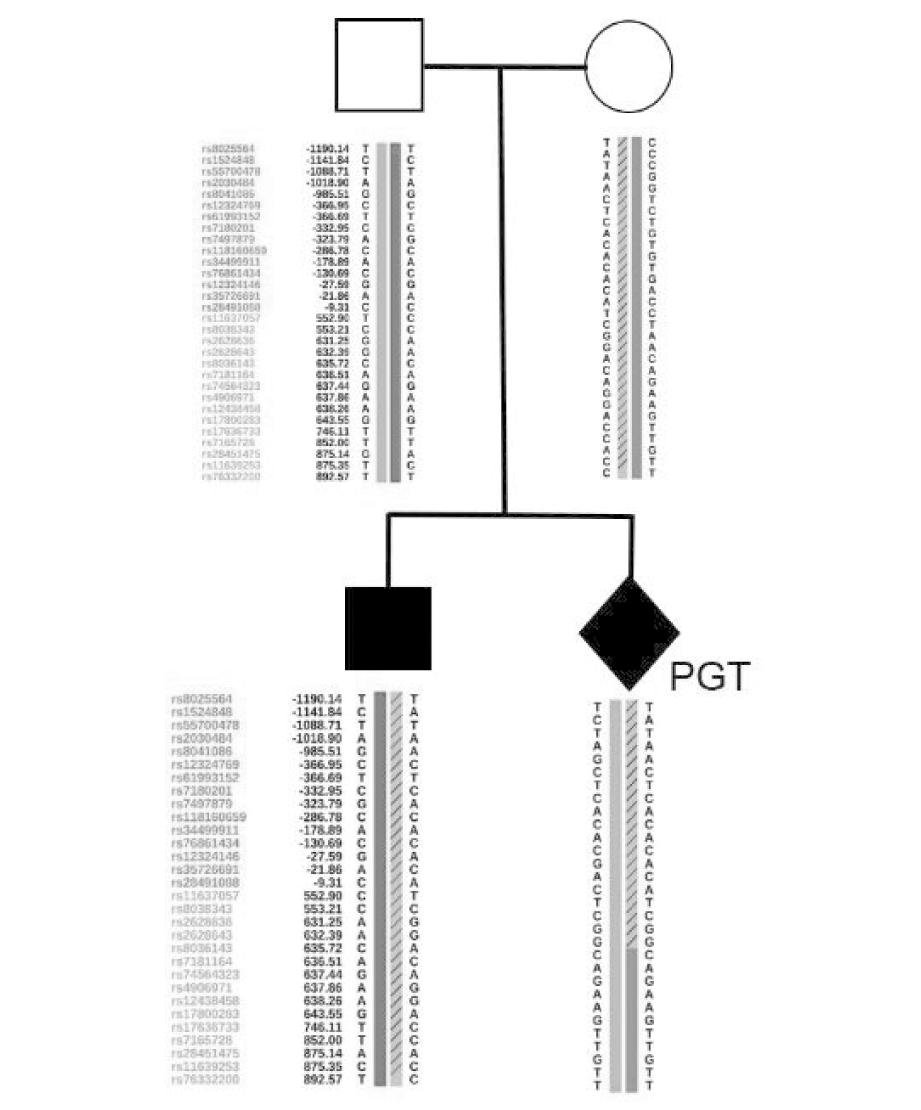
图1 Angelman综合征患者家系图谱
Figure 1 Genealogy of Angelman syndrome patients
·论著·
Angelman综合征(Angelman syndrome, OMIM 105830)又叫快乐木偶综合征,是一种罕见的遗传性疾病,自1965年Angelman综合征开始被认识后,临床病例报道不断增多[1-2]。其主要发表机制是由于15号染色体15q11.2-q13区域母源性缺失、印记异常、父源性单亲二倍体或者泛素蛋白连接酶 E3A(biguitinprotein ligase E3A,UBE3A)基因突变引起[3]。Angelman综合征通常在婴儿期就开始出现临床症状,表现为语言和运动能力发育落后、智力低下和快乐表情等,对患者的神经发育和认知能力产生重大影响。目前对于Angelman综合征还没有治愈方法,一般是通过综合性的治疗,包括物理治疗、语言治疗、药物治疗以及特殊教育和康复计划来改善患者的生活质量[4]。因此对于有Angelman综合征生育史的家庭,评估其再发风险,如果存在遗传因素给予生殖干预是非常必要的。
单基因病胚胎植入前遗传学检测(preimplantation genetic testing for monogenic disorders, PGT-M)作为一项辅助生殖与遗传诊断相结合的技术,通过对卵裂期或囊胚期的胚胎进行活检和遗传物质的检测,选择不携带特定基因变异的胚胎进行移植,可以有效的防止有遗传性疾病患儿的出生,是阻断致病变异垂直传递的有效方法[5]。本研究为一个有4例Angelman综合征患儿的家系进行了遗传学分析,并通过 PGT-M 的方法,避免了再次生育患儿的风险。
选取2023年4月就诊于复旦大学附属中山医院生殖医学中心的一个Angelman 综合征家系。家系中共有 4例智力障碍患者(见图1)。先证者,男,17岁,系第 1胎顺产。其母诉患者幼年运动和语言发育迟缓,坐、站、爬等运动发育均迟于正常同龄儿,3岁学会走路,现走路仍步态不稳,姿势不协调。语言障碍,仅能说日常2~3字的常用简单词汇。平时常不自觉频繁大笑,有明显的兴奋动作,多动,表现为经常性地拍手或者拍打物品,大叫。智力发育障碍,无法进行正常学习。睡眠障碍,表现为经常性夜间觉醒后难以入睡。脑电图未显示明显异常。其父母否认患儿有癫痫发作、惊厥或抽搐病史。

□normal male; normal female;■male patient with mutation;●female patient with mutation;The arrow represents the proband; Slash represents deceased
normal female;■male patient with mutation;●female patient with mutation;The arrow represents the proband; Slash represents deceased
图1 Angelman综合征患者家系图谱
Figure 1 Genealogy of Angelman syndrome patients
先证者弟弟,11岁,第2胎顺产,临床表现与先证者类似。先证者妹妹及弟弟,第3胎和第4胎顺产,同样表现为智力障碍和发育迟缓,快乐面容,分别于6岁和3岁时因意外死亡。家系其他成员无智力障碍、发育异常及癫痫等疾病。
2022年10月患者于外院就诊时对先证者,先证者弟弟,其父母及外祖父母检测提示先证者及弟弟15q11.2-q13印记中心部位存在小核核糖核蛋白相关蛋白N(small nuclear ribonucleoprotein-associated protein N,SNRPN),u5拷贝数缺失和甲基化异常(去甲基化状态,甲基化比值小于0.05),拷贝数缺失遗传自母亲。母亲15q11.2-q13印记中心部位存在相同的拷贝数缺失,但甲基化状态正常(正常甲基化状态:甲基化比值0.40~0.65)。先证者的父亲、外祖父及外祖母该区域均未发现基因缺失和甲基化状态异常(见表1、图2)。提示该家族先证者及弟弟15q11.2-q13 区域SNRPN u5基因拷贝数缺失遗传自母亲,外祖父及外祖母均正常,提示母亲或者系新发变异,或者存在外祖父生殖腺嵌合的可能。先证者及父母行家系全外显子检测,未见UBE3A基因突变。
表1 家系成员15q11-q13Angelman综合征印记区域检测结果
Table 1 The detection results about imprinting areas of 15q11-q13 Angelman syndrome in family members

RelationshipPhenotypeSNRPN u5region mutationSource of mutaionProbandPatientCopy Number Deletion Maternal OriginBrotherPatientCopy Number DeletionMaternal OriginMotherNormalCopy Number DeletionPaternal OriginFatherNormalNo mutation/GrandfatherNormalNo mutation/GrandmotherNormalNo mutation/
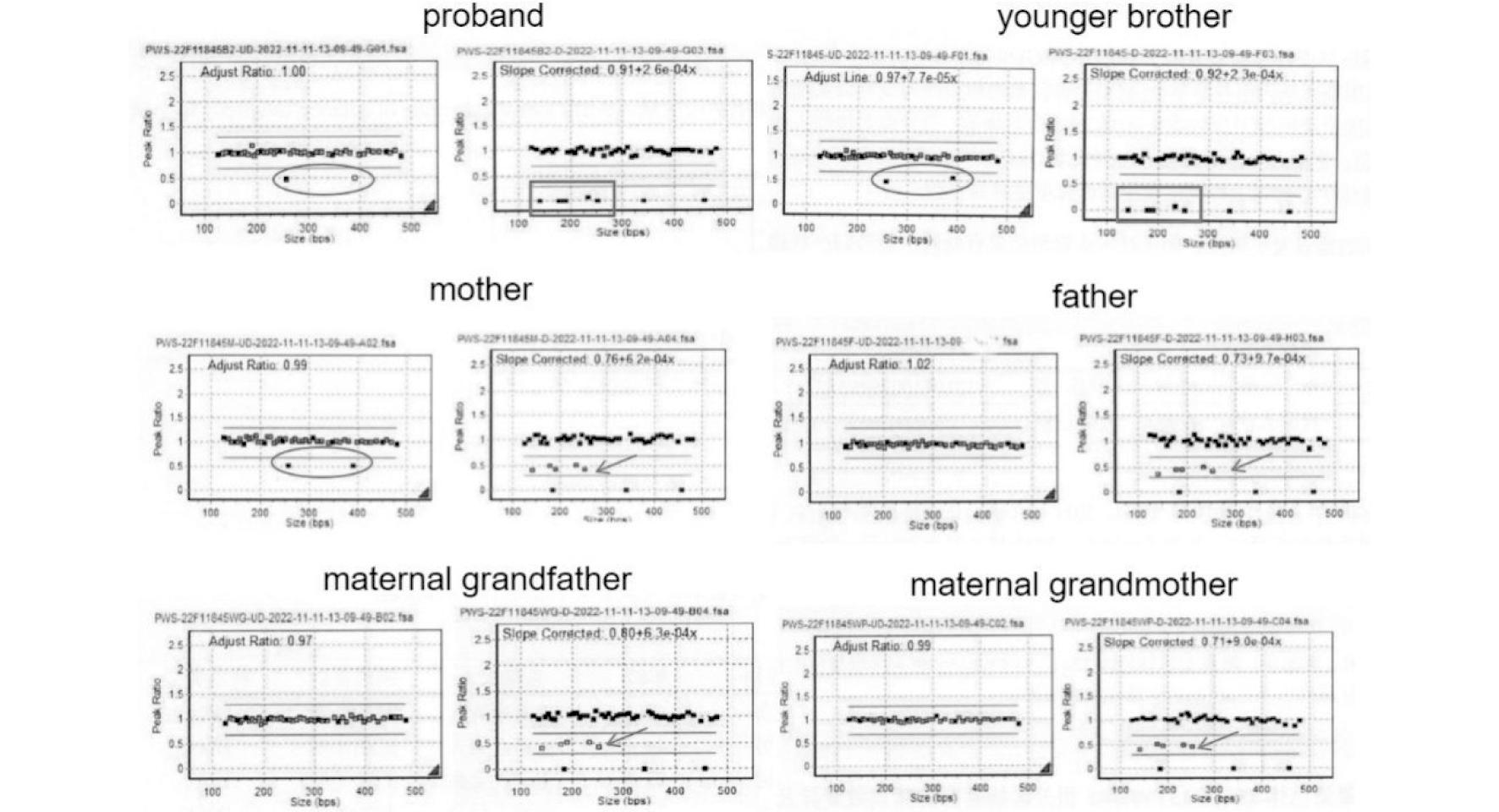
The oval shape indicates that the proband, younger brother, and mother have copy number deletions in the 15q11.2-q13 region of the gene, while the rectangular shape indicates that the proband and younger brother have abnormal methylation status in this region(demethylation status:methylation ratio less than 0.05); The arrow indicates that the methylation detection of the proband′s parents and maternal grandparents in this area is within the normal range(normal methylation status:methylation ratio 0.40-0.65).
图2 家系成员15q11.2-q13Angelman综合征印记区域检测报告
Figure 2 The detection report about 15q11.2-q13 Angelman syndrome imprinting area in family members
1. 血样采集及基因组 DNA 提取:抽取先证者及其家系成员静脉血2~5 mL,置于 EDTA抗凝管中。使用EX-DNA 全血基因组(3.0)试剂盒(货号:T146, 天隆公司,中国),按照天隆NP968-C磁珠法核酸提取的操作流程,对血液样本DNA进行自动化提取。提取后的DNA样本,使用 Qubit© dsDNA HS Assay Kit(货号:Q32851,Thermo Fisher Scientific)进行定量。
2. 甲基化特异性多重连接探针扩增技术(methylation sensitive multiplex ligation dependent probe amplification,MS-MLPA):对先证者及家系成员再次进行SNRPN u5区域变异位点验证,使用 Prader-Willi/Angelman 综合征 MS-MLPA 试剂盒(产品编号ME028-D1,荷兰 MRC-Holland 公司)检测 15q11.2-q13 印记区域的基因拷贝数(copy number variation,CNV)及甲基化。具体实验流程包括DNA变性,探针与DNA样本杂交,杂交探针的连接(分为两个PCR管中,管 1为拷贝数检测;管 2为甲基化检测,分别加入对应的连接缓冲液和连接探针),连接探针的PCR扩增,毛细管电泳分离扩增产物(扩增后的产物通过ABI-3730xl测序仪的毛细管电泳进行分离),用Coffalyser.NET分析软件进行数据分析,获得相关基因的CNV变异和甲基化信息。
3.单体型构建:根据欧洲人类生殖及胚胎学会发布的指南以及胚胎植入前遗传学诊断筛查技术的专家共识的要求, PGT-M胚胎基因检测应同时进行突变位点的直接分析和遗传多态位点连锁分析,并建议在突变基因的上下游1 Mb范围内,选择至少2个可分析位点进行分析,保证单倍体连锁分析的准确性。同时对于大片段缺失或重复难以直接进行胚胎位点检测的,建议采用基因上下游单核苷酸多态性(single nucleotide polymorphisms,SNP)连锁分析间接诊断胚胎致病携带情况[6-7]。采集夫妇双方及其先证者的外周血样,提取血液基因组 gDNA。利用Illumina公司Asian Screening Array(ASA)基因芯片对样本SNRPN u5基因所在的15号染色体11 710个SNP位点进行检测,分析SNRPN u5基因上下游 1 Mb 范围内SNP位点,选取其中可用位点进行单体型构建。可用位点定义为先证者SNP为杂合信号、父源一方为SNP信号纯合,母源一方为杂合信号,判定该位点为可用单体型构建SNP信号。
4. 胚胎活检及PGT-M 检测:门诊制定黄体期促排卵方案,获卵1枚,卵细胞胞质内单精子注射(intracytoplasmic sperminjection,ICSI)后正常受精1枚,于第3天获得可活检卵裂期胚胎1枚。采用吸取法对这枚卵裂期胚胎进行卵裂球活检。活检取得的胚胎细胞样本,运用多次退火环状循环扩增法(multiple annealing andlooping-based amplification cycles,MALBAC)进行全基因组扩增(whole genome amplification,WGA),以获取足量的 DNA。扩增过程参照基因测序通用样本处理试剂盒(ChromSwiftTM,XK-028,Yikon Genomics)进行。对扩增产物进行文库构建,染色体拷贝数变异(copy number variation,CNV)文库构建参照DNA片段化试剂盒(KT100804248,Yikon Genomics)和基因测序文库试剂盒(XK-038,Yikon Genomics)说明书进行。利用ASA基因芯片在胚胎WGA产物所在致病基因15号染色体的SNP位点进行检测。采用 NGS技术对胚胎WGA产物进行4 Mb以上的缺失或重复异常检测,同时用已构建好的家系SNP单体型对胚胎是否携带SNRPN u5缺失变异的SNP单体型进行分析。
在行单体型构建之前,再次对家系样本用MS-MLPA进行验证,验证结果显示先证者及母亲均携带SNRPN 基因 u5 区域缺失杂合突变,说明先证者的变异来源于母亲。先证者存在此区域的甲基化异常(去甲基化状态,甲基化比值小于0.05),而母亲的甲基化状态正常(甲基化比值0.40~0.65);先证者父亲15q11.2-q13 区域的拷贝数及甲基化状态均未发现异常。
通过检测变异基因SNRPN附近的SNP位点,并且进行连锁分析,构建携带该变异基因的单体型。在SNRPN基因的上下游1 M范围内筛选合适的SNP位点,结果如下:在变异基因1M范围内筛选到39个SNP位点,其中上游19个位点,下游20个位点。1 M以内的SNP数量足够用于单体型构建,表明该家系成员基因变异位点的单体型构建成功,可进行下一步的PGT-M胚胎分析。
先证者母亲42岁,系高龄女性,双侧卵巢基础窦卵泡仅1~2枚。考虑卵巢功能减退,为其制定黄体期控制性卵巢刺激方案,门诊超促排卵后,女方仅获卵1枚,其中成熟卵泡(metaphase II,MII)1枚,经 ICSI 体外受精后,获得双核受精卵(two pronuclei,2 PN)1枚,考虑1枚胚胎囊胚培养失败风险较大,故体外培养后第三天行卵裂期胚胎活检。进行PGT-M检测后,结果显示,该胚胎携带有母源性SNRPN 基因 u5 区域缺失杂合变异。其中胚胎SNP可用位点数(1 Mb范围内)26个,且胚胎的变异位点检测(见图3)和SNP单体型分析一致。同时CNV检测结果提示,胚胎存在多条染色体的拷贝数异常和嵌合异常(见图4)。经遗传咨询门诊与夫妇双方充分沟通后,不建议行胚胎移植。
□ normal male;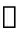 normal female;■male patient with mutation;◆PGT tested embryo with mutation;Number:Relative distance between upstream and downstream of the gene(kb); Left SNP locus represents the SNP locus upstream or downstream of the chromosome position where the gene is located; The slash inside the haplotype:The left slash represents the SNP haplotype linked to the female mutation site
normal female;■male patient with mutation;◆PGT tested embryo with mutation;Number:Relative distance between upstream and downstream of the gene(kb); Left SNP locus represents the SNP locus upstream or downstream of the chromosome position where the gene is located; The slash inside the haplotype:The left slash represents the SNP haplotype linked to the female mutation site
图3 胚胎PGT-M检测结果
Figure 3 Embryo PGT-M detection results
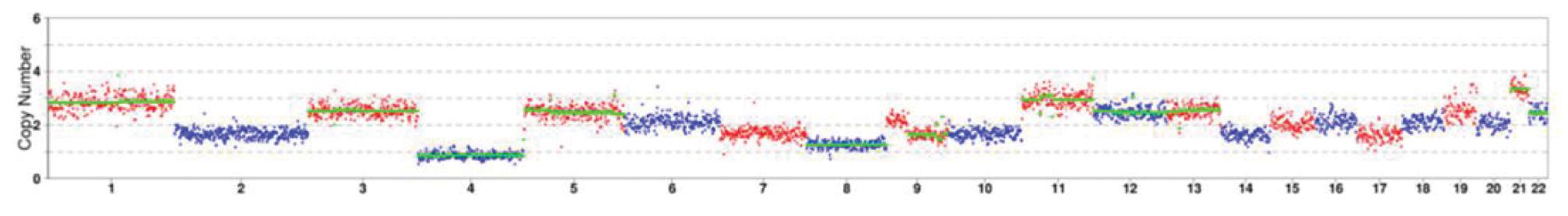
There are multiple chromosomal copy number abnormalities in the tested embryo:+1,+3(-53%),-4,+5(-50%),-8,del(9)(q21.11q34.3)(-70.40Mb, -36%), +11,+12(-48%),+13(-53%), +21, +22(-45%). Percentage represents the proportion of abnormal chromosome chimerism
图4 胚胎PGT-A检测结果图
Figure 4 Embryo PGT-A detection results
Angelman 综合征是由 15q11.2-q13 染色体区域母源印记基因的功能异常导致的神经系统发育性疾病[8]。本研究对该例Angelman综合征家系的首先进行了遗传学分析,先证者、弟弟和母亲均携带15q11.2-q13区域SNRPN 基因 u5 区域的杂合性缺失,先证者和弟弟存在15q11.2-q13区域甲基化的异常,而母亲的甲基化状态正常且表型正常,说明母亲15q11.2-q13印记中心部位的拷贝数缺失存在于父源的一条染色体上,故此区域的甲基化状态正常;而母亲的拷贝数缺失传递给两个患儿,导致了母源性染色体上述区域拷贝数缺失,从而导致甲基化状态异常,引起先证者及弟弟Angelman综合征的临床表型,其他两个孩子也有临床表型,由于现实原因无法进行验证,推测很可能携带同样的变异。
人类遗传学研究表明,Angelman综合征主要是由4种分子机制引起,不同的发病机制的临床表型和再发风险不同[9]。所以Angelman综合征患儿需完善其遗传机制分型,并且结合家系验证的结果,预测再发风险。母源染色体15q11.2-q13区域的5-7Mb新发缺失是与Angelman综合征相关的最常见的遗传机制,约75%的患者是由该区段缺失所致。包括整个印记结构域加上几个非印记基因,在大多数情况下的缺失都是新发变异;只有在极少数情况下,缺失是由于母源染色体的结构重排,如平衡易位造成的。因此,如果母亲有15号染色体的正常拷贝,家族内的复发风险很低[10]。第二种发病机制是母源染色体15q11.2-q13区域内的UBE3A的基因变异导致,约占5%~10%。Sadikovic[11]等人提供的UBE3A基因变异大数据集表明,约29%的UBE3A变异是遗传自母亲,较高的复发风险(50%),约71%是新发变异,复发风险较低。第三种分子机制是 15号染色体的父源性单亲二倍体(UPD)(1%~2%),这可能是由于母源染色体不分离和来自精子的第15号染色体的形成合子后重复所致。如果母亲有正常的核型,家庭内复发的风险很低。第四种是由于染色体15q11.2-q13内的印记缺陷(占1%~3%),改变了母源遗传的UBE3A表达。虽然各种分子机制的Angelman综合征存在差异,但一般而言,缺失型的Angelman综合征表型更严重,单亲二倍体和印记缺陷的表型相对较轻[12]。
在对本家系进行PGT流程前,进一步用MS-MLPA的方法再次验证了先证者和父母的变异位点。MS-MLPA的方法诊断Angelman综合征的机理在于SNRPN启动子的差异甲基化。位于染色体 15q11.2-q13的印记基因SNRPN受甲基化的调控,若源于母亲,则这个基因周围的CpG 二核苷酸高度甲基化(96%),而源于父亲则相同的 CpG二核酸不被甲基化。所以在Angelman综合征患者,SNRPN启动子周围的 CpG二核苷酸处于低甲基化状态。这种甲基化异常模式可以作为疾病基因诊断的标记[13]。80%~90%的Angelman综合征病例可以检测到15q11.2-q13的异常DNA甲基化,其余正常DNA甲基化病例,是由于UBE3A点突变或小的基因内重排所致。对疑似有Angelman综合征的患者的第一级临床诊断检测是DNA甲基化检测,特别是在差异甲基化的SNRPN启动子/外显子1区域内[9]。本研究在MS-MLPA验证结果中看到,先证者和弟弟均出现15q11.2-q13印记中心的去甲基化状态,说明患者存在母源性等位基因的异常,Angelman综合征诊断成立。
先证者SNRPN, u5的拷贝数缺失遗传自母亲,其发病机制可排除父源性单亲二倍体,且不存在15q11.2-q13区域的大片段缺失,甲基化状态异常,因此本例Angelman综合征家系的发病机制是由于上述中的第四种发病机制即印记缺陷导致的,属于比较罕见的病例。大约1%~3%的Angelman综合征患者可归因于印记缺陷,该缺陷可由表观遗传改变,进而影响15q11.2-q13中整个印记结构域的甲基化和基因表达。在一小部分情况下,印记缺陷是由印记中心的微小缺失引起,该中心调节整个15q11.2-q13印记结构域的印记建立和维持[14]。只有少数报道的印记中心缺失是在母源染色体新发的,或者是由于母亲生殖腺嵌合所致。在大多数情况下,这种缺失是一种家族遗传突变,可以通过父系传递,而不会产生表型效应,但通过母系传递时会导致不正确的父系印记。因此,具有印记中心缺失的女性生育患有Angelman综合征的孩子的风险为50%[15]。本病例中母亲15q11.2-q13印记中心部位存在拷贝数缺失,且已生育四个患儿,其再生育患儿的风险为50%,进行PGT-M指征明确。
由于胚胎活检所获得DNA遗传物质非常少,无法满足二代测序或 SNP array 分析所需要的最低阈值,所以需要进一步进行全基因组扩增,同时结合短串联重复序列(short tandem repeat,STR)或 SNP 建立双亲遗传标志的单体型,以避免因扩增失败、等位基因脱扣(alleledrop-out,ADO)、样本污染等因素导致的检测失误[6]。《单基因病胚胎着床前遗传学检测专家共识》中指出[5]:建议 PGT-M临床检测应同时进行基因致病变异位点的直接检测和遗传多态位点(STR或SNP)的连锁分析;同时建议采用PGT-M 联合胚胎染色体非整倍体检测(PGT for aneuploidies,PGT-A)的检测策略。相较于 STR,SNP 在人类基因组中数量更多、分布更广,具有更高的特异性,故本研究在SNRPN基因的上下游筛选合适的SNP位点,在变异基因1M范围内筛选到39个SNP位点,其中上游19个位点,下游20个位点。1M以内的SNP数量足够用于单体型构建。从而确定携带SNRPN 基因缺失变异的风险染色体,减少基因重组或ADO的发生风险。
PGT 是针对植入前胚胎进行遗传学诊断,根据活检时机的不同可分为极体活检、卵裂球活检和囊胚滋养层细胞活检[16]。采用卵裂期胚胎的卵裂球进行单细胞遗传学分析,可以同时分析来自父母双方的遗传信息,曾经是PGT最主要的取材方式;世界首例PGT婴儿即采用的卵裂期胚胎活检[17]。但是,由于可供诊断的细胞有限,且卵裂期胚胎嵌合比例较高,而囊胚的滋养层活检可获得的细胞数目较多,胚胎染色体嵌合比例低,对胚胎发育的潜能影响较小,已逐渐成为PGT-M 技术操作的主要活检方式[18-19]。但前提是要有可供活检的囊胚形成,目前体外培养的胚胎大约有40%能发育至囊胚阶段。对于卵巢功能减退的女性,促排周期获卵数低,很有可能因没有囊胚而丧失了胚胎活检和移植的机会。对于本病例患者仅获得1枚卵子,如果体外培养到第五天进行囊胚培养,很有可能没有囊胚活检。因此对于此病例,本研究选择了卵裂期胚胎活检,以减少患者无胚胎检测的风险。遗憾的是,这枚胚胎携带了母源性基因缺失,而且存在多条染色体拷贝数的异常,通过充分遗传咨询后不建议患者进行移植。虽然患者胚胎较少,没有筛选到可供移植的胚胎,但是本研究通过PGT-M技术,成功阻断了此家系中导致Angelman综合征发病的变异基因的垂直传递,避免了患儿的再次出生。
如今随着基因检测技术的快速发展,PGT技术已经广泛应用于临床实践,成为许多国家辅助生殖技术的重要组成部分,并且帮助具有遗传病家族史的家庭阻断了疾病的传递,生育了健康的后代。本研究通过深入分析这个已生育4个患儿的Angelman综合征家系的遗传机制,充分进行遗传咨询的情况下,通过PGT-M技术进行生殖干预,检测到携带母源性致病变异的胚胎,成功避免了家庭再次生育Angelman综合征后代的风险。
所有作者均声明不存在利益冲突
1 Keary CJ,McDougle CJ.Current and emerging treatment options for Angelman syndrome.Expert Rev Neurother,2023,23:835-844.
2 Ma VK,Mao R,Toth JN,et al.Prader-Willi and Angelman Syndromes:Mechanisms and Management.Appl Clin Genet,2023,16:41-52.
3 Markati T,Duis J,Servais L.Therapies in preclinical and clinical development for Angelman syndrome.Expert Opin Investig Drugs,2021,30:709-720.
4 Maranga C,Fernandes TG,Bekman E,et al.Angelman syndrome:a journey through the brain.FEBS J,2020,287:2154-2175.
5 中国医师协会生殖医学专业委员会,中国医师协会医学遗传医师分会.单基因病胚胎着床前遗传学检测专家共识.中华生殖与避孕杂志,2021,41:477-485.
6 《胚胎植入前遗传学诊断/筛查专家共识》编写组.胚胎植入前遗传学诊断/筛查技术专家共识.中华医学遗传学杂志,2018,35:151-155.
7 ESHRE PGT-M Working Group,Carvalho F,et al.ESHRE PGT Consortium good practice recommendations for the detection of monogenic disorders.Hum Reprod Open,2020:hoaa018.
8 Maranga C,Fernandes TG,Bekman E,et al.Angelman syndrome:a journey through the brain.FEBS J,2020,287:2154-2175.
9 Buiting K,Williams C,Horsthemke B.Angelman syndrome - insights into a rare neurogenetic disorder.Nat Rev Neurol,2016,12:584-593.
10 Buiting K,Saitoh S,Gross S,et al.Inherited microdeletions in the Angelman and Prader-Willi syndromes define an imprinting centre on human chromosome 15.Nat Genet,1995,9:395-400.
11 Sadikovic B,Fernandes P,Zhang VW,et al.Mutation update for UBE3A variants in Angelman syndrome.Hum Mutat,2014,35:1407-1417.
12 Yang L,Shu X,Mao S,et al.Genotype-phenotype correlations in Angelman Syndrome.Genes(Basel),2021,12:987.
13 Dikow N,Nygren AO,Schouten JP,et al.Quantification of the methylation status of the PWS/AS imprinted region:comparison of two approaches based on bisulfite sequencing and methylation-sensitive MLPA.Mol Cell Probes,2007,21:208-215.
14 Lewis MW,Brant JO,Kramer JM,et al.Angelman syndrome imprinting center encodes a transcriptional promoter.Proc Natl Acad Sci U S A,2015,112:6871-6875.
15 Buiting K,Gross S,Lich C,et al.Epimutations in Prader-Willi and Angelman syndromes:a molecular study of 136 patients with an imprinting defect.Am J Hum Genet,2003,72:571-577.
16 黄锦,刘平.胚胎活检时机和方法选择及其对植入前遗传学诊断及筛查结局影响.中国实用妇科与产科杂志,2016,32:234-237.
17 Santamonkunrot P,Samutchinda S,Niransuk P,et al.The Association between embryo development and chromosomal results from PGT-A in women of advanced age:A prospective cohort study.J Clin Med,2024,13:626.
18 Scott RT,Jr Upham KM,Forman EJ,et al.Cleavage-stagebiopsy significantly impairs human embryonic implantation potential while blastocyst biopsy does not:a randomized andpaired clinical trial.Fertil Steril,2013,100:624-30.
19 Kokkali G,Traeger-Synodinos J,Vrettou C,et al.Blastocyst biopsy versus cleavage stage biopsy and blastocyst transfer for preimplantation genetic diagnosis of beta-thalassaemia:a pilot study.Hum Reprod,2007,22:1443-1449.