·病例报告·
1例肉碱棕榈酰转移酶1A缺乏症的诊断随访并文献复习
唐玥 李璐璐 宫丽霏 杨海河 赵金琦 孔元原
【摘要】 回顾性分析1例经新生儿筛查确诊的肉碱棕榈酰转移酶1A缺乏症患儿诊断随访资料,患儿男,生后4天新生儿筛查示游离肉碱升高伴长链酰基肉碱下降,基因检测示CPT1A基因复合杂合突变,给予喂养指导,随访至24月龄未出现临床症状。肉碱棕榈酰转移酶1A缺乏症可筛可治,经早期诊断及合理随访干预总体预后较好,但该病的长期管理及远期预后仍待深入研究。
【关键词】 肉碱棕榈酰转移酶1A缺乏症; CPT1A缺乏症; CPT1A基因; 脂肪酸氧化障碍疾病; 新生儿筛查
【中图分类号】 R72
作者单位:100026,首都医科大学附属北京妇产医院北京妇幼保健院新生儿疾病筛查科
通信作者:孔元原(kongyuanyuan1971@mail.ccmu.edu.com)
肉碱棕榈酰转移酶1A(carnitine palmitoyltransferase 1A,CPT1A)缺乏症是由于CPT1A缺陷,导致长链酰基辅酶A(coenzyme A,CoA)进入线粒体进行β氧化途径受阻,引起的脂肪酸氧化障碍疾病,属于常染色体隐性遗传病。未经治疗的患者可因感染性疾病或饥饿诱发代谢危象,出现反应差、呕吐、抽搐、意识障碍,易误诊为中枢神经系统感染或其他中枢神经系统疾病导致治疗延误,严重者可致死。由于该病罕见,全球发病率约为1/500 000[1],且临床症状和常规生化改变缺乏特异性,易延误诊治造成预后不良。本文报道1例经新生儿筛查确诊的CPT1A缺乏症,结合相关文献,对中国CPT1A缺乏症患者的临床特征及基因检测结果等进行总结,旨在提高临床医师对CPT1A缺乏症的认识,从而实现对该病的早期诊断、干预,改善患者预后。
病例资料
患儿男,第一胎第一产,双胎之大,胎龄38周,因“双胎”行选择性剖宫产娩出,产程顺利,出生体重2 965 g,生后一般情况好,混合喂养,纳奶可。生后第4天行新生儿筛查,游离肉碱及酰基肉碱谱检测结果:C0:174.5 μmol/L(10-60 μmol/L),C16:0.20 μmol/L(0.5-7.4 μmol/L),C18:0.09 μmol/L(0.2-2.1 μmol/L),C0/(C16+C18) 601.72(2~50)。生后17天召回复查游离肉碱及酰基肉碱谱仍显示C0升高,C16、C18降低,C0/(C16+C18)显著升高为正常上限的16倍(详见表1)。母亲孕产史及家族史无特殊,双胞胎妹妹新生儿筛查结果正常。查体:神志清,精神反应可,发育正常,营养中等,无特殊面容,双肺未闻及干、湿啰音,心率140次/分,心音有力,律齐,腹软,肝脾不大,肌力肌张力正常。常规生化检查示:肝酶正常,血糖不低,肌酸激酶198 U/L(29~168 U/L)、肌酸激酶同工酶MB5.74 ng/mL(0~3.1ng/mL)轻度升高。影像学检查:肝胆胰脾肾超声及超声心动图均未见明显异常。
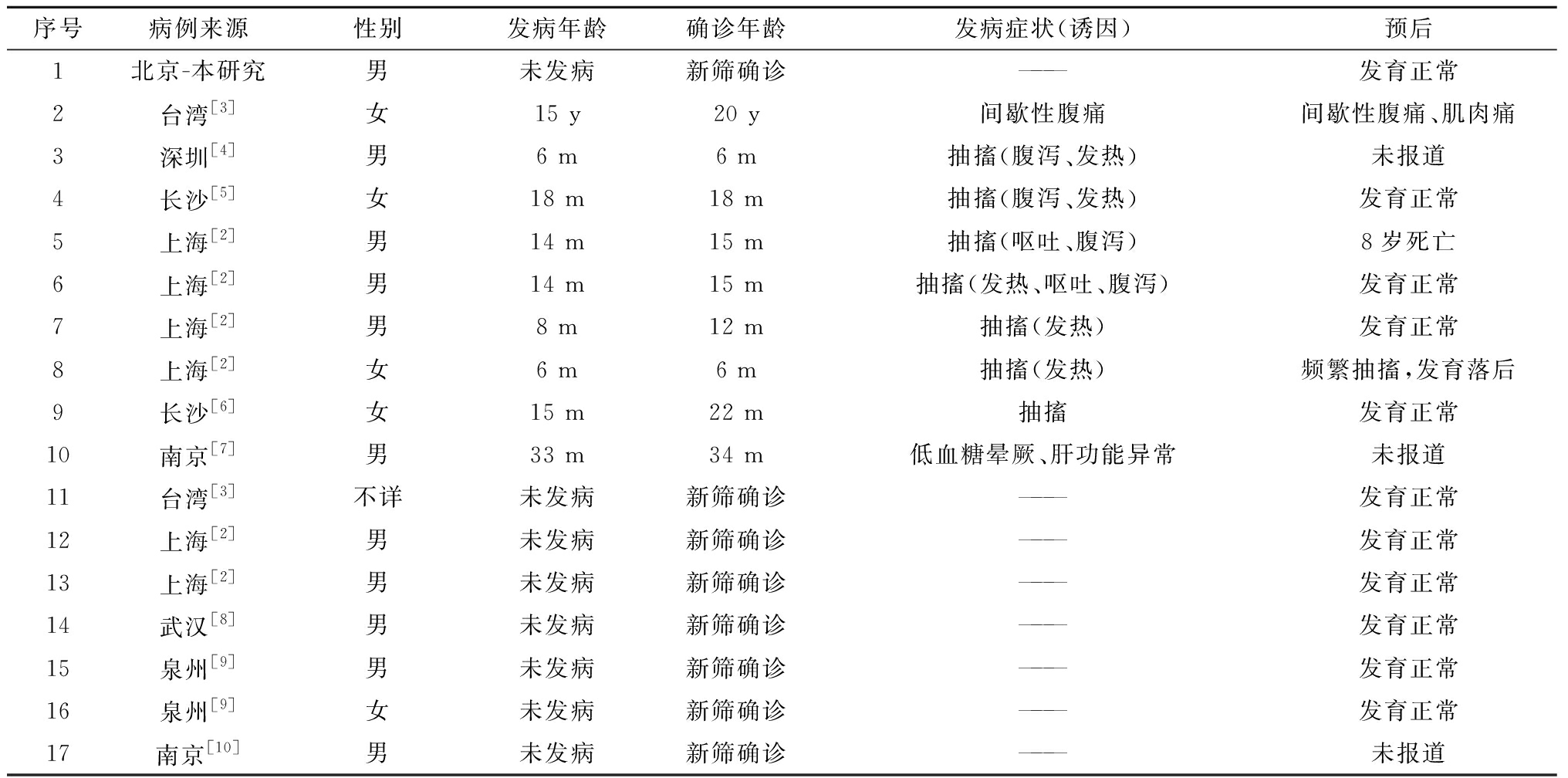
表1 17例中国CPT1A缺乏症患者基本信息及临床情况
序号病例来源性别发病年龄确诊年龄发病症状(诱因)预后1北京-本研究男未发病新筛确诊———发育正常2台湾[3]女15 y20 y间歇性腹痛间歇性腹痛、肌肉痛3深圳[4]男6 m6 m抽搐(腹泻、发热)未报道4长沙[5]女18 m18 m抽搐(腹泻、发热)发育正常5上海[2]男14 m15 m抽搐(呕吐、腹泻)8岁死亡6上海[2]男14 m15 m抽搐(发热、呕吐、腹泻)发育正常7上海[2]男8 m12 m抽搐(发热)发育正常8上海[2]女6 m6 m抽搐(发热)频繁抽搐,发育落后9长沙[6]女15 m22 m抽搐发育正常10南京[7]男33 m34 m低血糖晕厥、肝功能异常未报道11台湾[3]不详未发病新筛确诊———发育正常12上海[2]男未发病新筛确诊———发育正常13上海[2]男未发病新筛确诊———发育正常14武汉[8]男未发病新筛确诊———发育正常15泉州[9]男未发病新筛确诊———发育正常16泉州[9]女未发病新筛确诊———发育正常17南京[10]男未发病新筛确诊———未报道
征得家长知情同意后,收集患儿及其父母外周静脉血各2 mL,于4℃条件下保存,送至北京迈基诺医学检验所进行基因检测。采用Illumina高通量测序系统,针对相关基因全外显子区进行高通量测序,将过滤后的原始数据与人类基因组标准序列hg19(Genome Reference Consortium GRCh37,hg19)进行对比,同时采用CNVkit软件进行基于二代测序原始数据的拷贝数变异(Copy number variation,CNV)分析,利用同一捕获池的样本做对照进行分析,统计目标区域和非目标区域的读书深度,然后在样本内对深度进行均一化和矫正,与对照集进行比较计算得到拷贝数信息,最后用循环二次分割算法(circular binary segmentation,CBS)对区域进行分割。
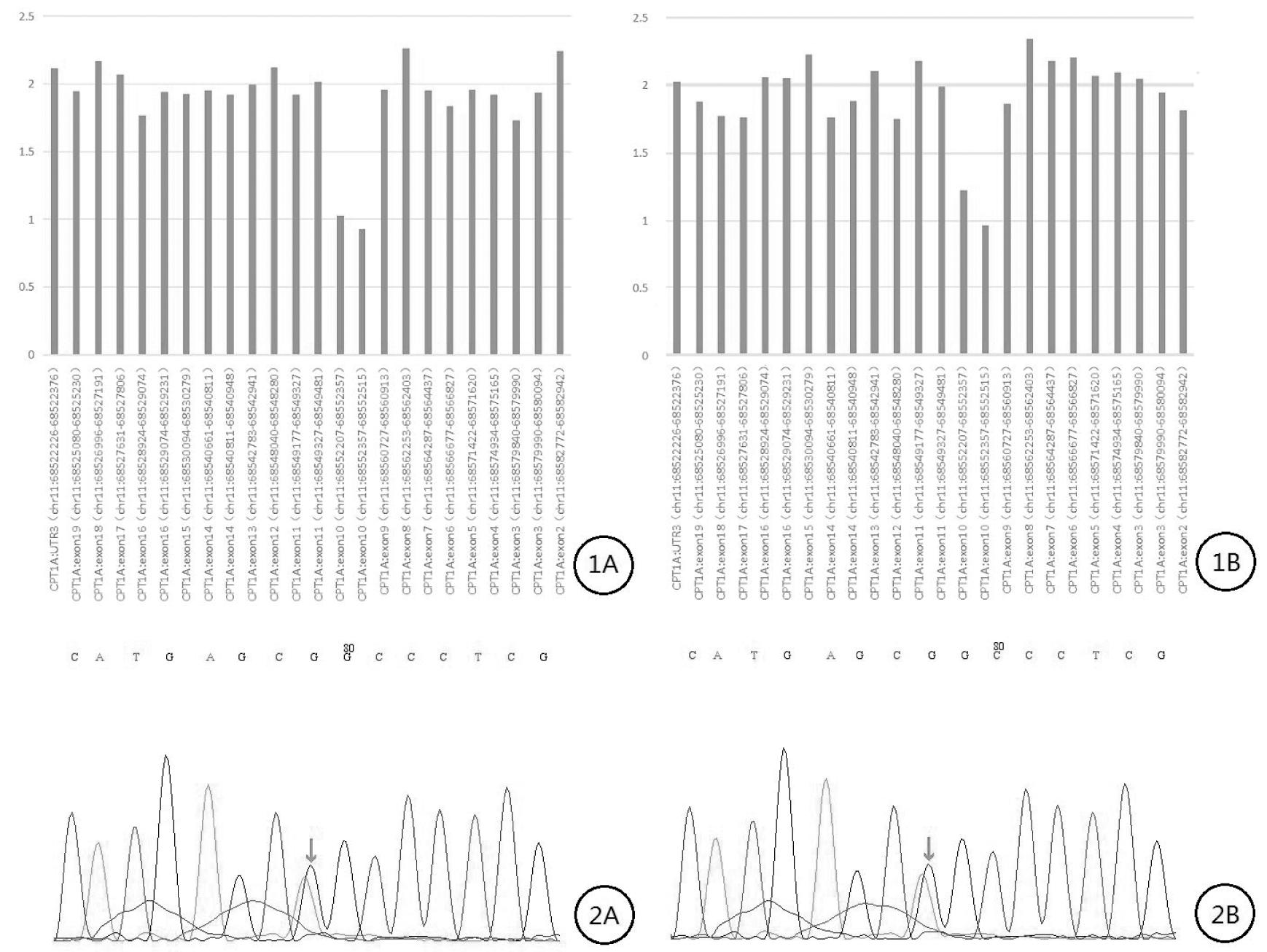
检测显示患儿CPT1A基因存在10号外显子缺失和c.740C>T(p.P247L)复合杂合突变。进一步完善父母CNV分析及Sanger测序验证突变分别来源于父母亲(见图1)。10号外显子缺失可能导致基因功能丧失(PVS1),该变异在正常人群数据库中的频率未有报道,为低频变异(PM2),根据ACMG指南,该变异判定为疑似致病性变异;c.740C>T变异为错义突变,导致第247号氨基酸由脯氨酸变为亮氨酸,该突变在正常人群数据库中的频率为0.0006418,为低频变异(PM2),该变异与已发现的疑似致病性变异10号外显子缺失呈反式分布(PM3),生物信息学蛋白功能综合性预测软件REVEL预测结果为有害,SIFT、PolyPhen_2、MutationTaster 、GERP+预测结果分别为有害、有害、有害、有害(PP3),国内已有病例报告认为该变异有致病性[2](PP5),根据ACMG指南,该变异判定为疑似致病性变异。
依据患儿游离肉碱及酰基肉碱谱特异性改变及基因检测结果,诊断“CPT1A缺乏症”明确。较为遗憾的是,患儿父母未同意对患儿孪生妹妹致病突变携带情况进行验证。
患儿自召回复查之日起即开始严格控制最长空腹时间,新生儿期喂养间隔时间不超过2~3 h;满1岁前不超过4~6 h;满1岁后不超过8 h。因生后纳奶好、体重平稳增长,继予母乳及普通婴儿配方混合喂养,早期未添加高中链甘油三酯(medium chain triglycerides,MCT)治疗配方粉;6月龄添加辅食并少量添加MCT油;积极预防失代偿,患感染性疾病期间保障充足能量供应;避免使用具有潜在肝毒性药物。末次随访时患儿24月龄,普通饮食,未严格限制膳食脂肪摄入量,鼓励增加优质蛋白摄入,避免食用油炸食品等高脂肪食物,未补充MCT油,未曾出现临床症状,监测肝脏、肾脏、心脏等器官功能正常,体格及神经心理发育同正常同龄儿。
文献复习
以“肉碱棕榈酰转移酶1A缺乏症”“肉碱棕榈酰转移酶I缺乏症”“carnitine palmitoyltransferase 1A deficiency”“carnitine palmitoyltransferase I deficiency”为中、英文关键词,在中国知网、万方数据库、web of science数据库和PubMed数据库中,对关于中国CPT1A缺乏症患者的相关文献进行检索,纳入符合CPT1A缺乏症诊断标准并进行基因检测病例,剔除临床病例资料不齐全者,共纳入病例16例,结合本研究确诊的1例患儿,共计17例[2-10]。
这17例患儿中,除1例未描述性别外,11例为男性,5例为女性,其中临床发病病例9例,新生儿筛查确诊病例8例。① 临床表现:9例临床发病病例中,7例发病年龄为6-18月,均以抽搐为首发症状,发病前多有发热、腹泻、呕吐等诱因;1例33月龄发病,以低血糖晕厥伴肝功能异常为主要表现;1例临床症状不典型,自15岁起反复出现间歇性腹痛,考虑为“复发性急性胰腺炎”,缺乏其他特异性症状,另外8例新生儿筛查确诊病例未出现临床症状。② 随访结果:9例临床发病病例中,1例患儿于8岁死亡,1例经过积极治疗仍频繁惊厥发作、发育落后,1例反复发生间歇性腹痛、肌肉痛,4例生长发育正常,2例未报道随访结果;8例新生儿筛查确诊病例除1例未报道随访结果外,其余病例随访期间生长发育正常。③ 基因检测结果:17例患儿中仅1例患儿(例10)为纯合缺失突变,其余16例均为复合杂合突变。17例患儿共检测出CPT1A基因突变25种,包括15种错义突变、4种剪切突变、1种无义突变、1种移码突变、1种整码突变及3种大片段缺失,变异谱具有高度异质性,2201T>C(p.F734S)突变频率相对较高(4/34)。
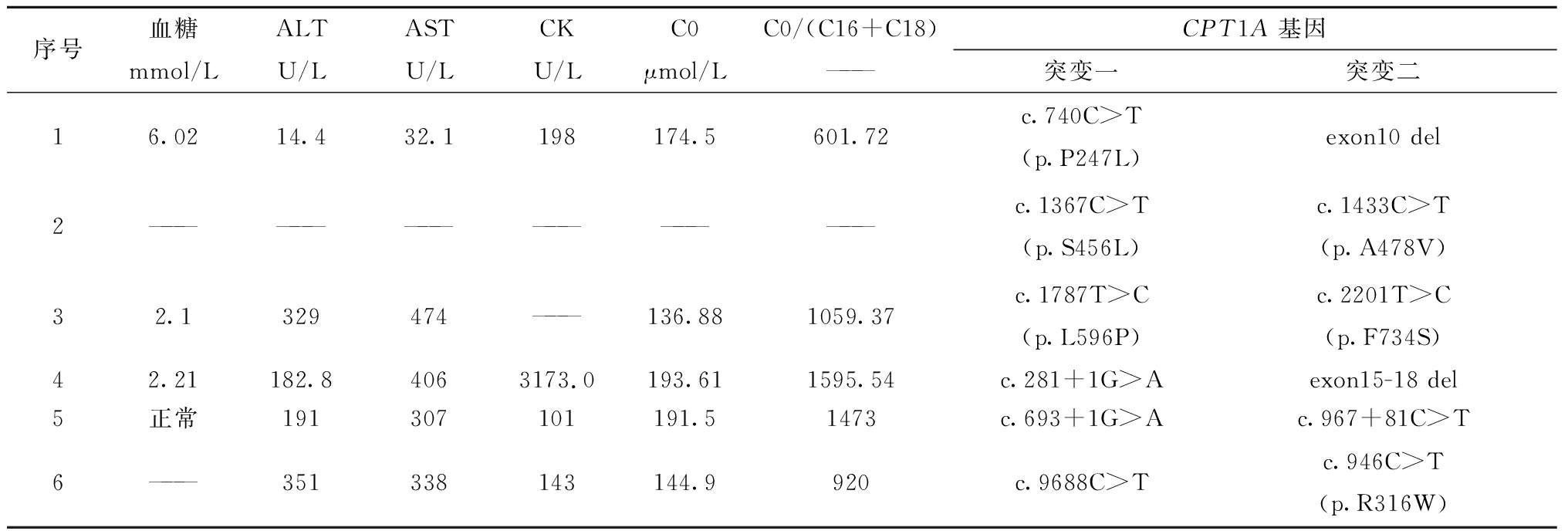
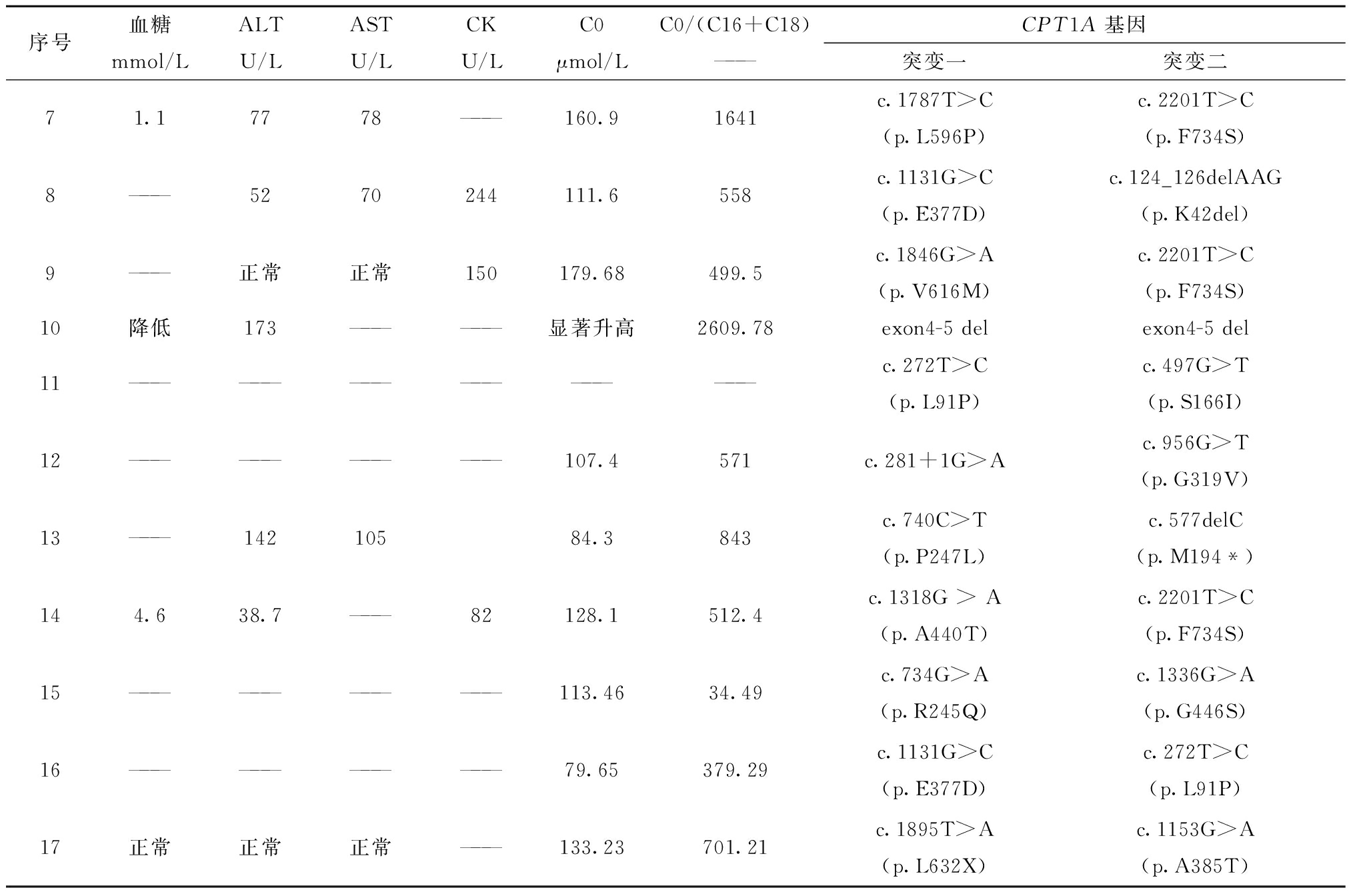
纳入研究的17例CPT1A缺乏症患儿基本信息及临床情况详见表1,生化检查及基因检测结果详见表2。
表2 17例中国CPT1A缺乏症患者生化检查及基因检测结果
序号血糖ALTASTCKC0C0/(C16+C18)mmol/LU/LU/LU/Lμmol/L———CPT1A基因突变一突变二16.0214.432.1198174.5601.72c.740C>T(p.P247L)exon10 del2——————————————————c.1367C>T(p.S456L)c.1433C>T(p.A478V)32.1329474———136.881059.37c.1787T>C(p.L596P)c.2201T>C(p.F734S)42.21182.84063173.0193.611595.54c.281+1G>Aexon15-18 del5正常191307101191.51473c.693+1G>Ac.967+81C>T6———351338143144.9920c.9688C>Tc.946C>T(p.R316W)
表2(续)
序号血糖ALTASTCKC0C0/(C16+C18)mmol/LU/LU/LU/Lμmol/L———CPT1A基因突变一突变二71.17778———160.91641c.1787T>C(p.L596P)c.2201T>C(p.F734S)8———5270244111.6558c.1131G>C(p.E377D)c.124_126delAAG(p.K42del)9———正常正常150179.68499.5c.1846G>A(p.V616M)c.2201T>C(p.F734S)10降低173——————显著升高2609.78exon4-5 delexon4-5 del11——————————————————c.272T>C(p.L91P)c.497G>T(p.S166I)12————————————107.4571c.281+1G>Ac.956G>T(p.G319V)13———14210584.3843c.740C>T(p.P247L)c.577delC(p.M194*)144.638.7———82128.1512.4c.1318G > A(p.A440T)c.2201T>C(p.F734S)15————————————113.4634.49c.734G>A(p.R245Q)c.1336G>A(p.G446S)16————————————79.65379.29c.1131G>C(p.E377D)c.272T>C(p.L91P)17正常正常正常———133.23701.21c.1895T>A(p.L632X)c.1153G>A(p.A385T)
讨论
脂肪酸β氧化是机体在禁食或能量需求增加时维持能量供应的重要途径,在肝脑等能量需求高的组织中至关重要。与短中链酰基CoA可直接通透线粒体内膜不同,长链酰基CoA必须通过肉碱穿梭方能进入线粒体进行β氧化。肉碱棕榈酰转移酶I(carnitine palmitoyltransferase I,CPTI)是一种线粒体膜蛋白,位于线粒体外膜,参与肉碱穿梭,是催化中、长链酰基CoA与肉碱合成酰基肉碱进入线粒体参与β氧化的限速酶[11],CPTI缺陷,长链酰基CoA进入线粒体进行β氧化途径受阻,乙酰CoA生成减少,长链酰基CoA蓄积。目前发现CPTI有三种亚型:CPT1A、CPT1B、CPT1C,分布具有组织特异性,CPT1A主要分布于肝脏、肾脏、胰腺;CPT1B主要分布于心脏、骨骼肌、棕色脂肪;CPT1C仅存在于神经元内质网,参与脂质代谢调控,与摄食行为和能量稳态的调控有关,不参与脂肪酸β氧化[12]。迄今为止,所报道的所有CPTI缺乏症患者实际均为CPT1A缺陷所致,尚无CPT1B缺陷相关病例报道,不除外CPT1B缺陷可能为一致死性疾病。
CPT1A缺乏症的致病基因CPT1A定位于染色体11q13.3,包含19个外显子,编码773个氨基酸。目前已报道CPT1A基因致病突变60余种,以错义突变为主。其中c.1436C>T(p.P479L)这一致病性较低的突变在纽因特人和美国阿拉斯加地区人群中携带率较高[13];c.2129G>A(p.G710E)在北美哈特莱特教派人中携带率较高[14];除此之外,其他已报道突变多为单个家系变异,突变谱具有高度异质性。国内研究报道的突变谱明显有别于欧美国家,上述2种欧美人群携带率较高的突变在国内未见报道,我国17例患儿检测出的25种变异中,除c.281+1G>A欧美国家已有报道外[15],其余24种突变目前均仅在中国人群中报道,以2201T>C(p.F734S)突变出现频率最高(4/34),可能为我国CPT1A缺乏症患者的热点突变。
文献复习结果显示,CPT1A缺乏症首次出现临床症状的年龄大多为6-18月龄,与国外报道一致[13],以感染性疾病诱发急性代谢危象,出现抽搐、意识障碍等,为典型表现,发病年龄较大者临床症状可不典型。目前报道的大部分临床发病CPT1A缺乏症患儿经积极治疗后预后良好,9例患儿中仅1例死亡,1例出现明显智能发育落后,新生儿筛查确诊病例均未出现临床症状、生长发育正常,提示CPT1A缺乏症与肉碱棕榈酰转移酶II缺乏症、极长链酰基辅酶A脱氢酶缺乏症等其他长链脂肪酸氧化障碍疾病相比,远期预后相对好,死亡率较低。CPT1A缺乏导致长链酰基CoA蓄积,而非长链酰基肉碱蓄积,前者毒性作用较后者低可能是CPT1A缺乏症预后较好的原因。另外CPT1A存在同工酶,同工酶CPT1B主要分布于骨骼肌、心脏,CPT1A缺乏症患者心肌和骨骼肌受累较其他长链脂肪酸氧化障碍患者轻,通常不发生心律失常、心肌病、横纹肌溶解等典型心肌骨骼肌损害可能与此有关。
CPT1A缺乏症的治疗原则与其他长链脂肪酸氧化障碍疾病一致,急性发作期应尽快给予足量10%葡萄糖液静脉输注以纠正低血糖并抑制脂肪分解代谢,稳定期治疗包括避免饥饿和长时间运动,低脂高碳水化合物饮食,适量补充MCT,对症处理及预防和治疗并发症。但临床实践发现,在避免饥饿和长时间运动的前提下,代谢稳定期的CPT1A缺乏症患者可能无需严格限制膳食脂肪摄入量。
新生儿筛查是早期诊断CPT1A缺乏症的有效手段。目前国内报道病例中,新生儿筛查确诊病例随访期间均未出现临床症状,可能由于此类患儿早期确诊后及时接受了生活管理及喂养指导,避免了应激状态下的代谢失衡,从而避免临床症状出现。但值得注意的是,文献复习中一例临床发病患者发病年龄晚、起病隐匿,以复发性急性胰腺炎为主要表现,类似情况在其他脂肪酸代谢障碍疾病患者中亦有报道[16]。年长儿或成人以肝脾肿大、肝功能异常、肾小管性酸中毒等为主要表现,最终确诊为CPT1A缺乏症的病例亦有数例报道[17-18],提示目前对经新生儿筛查确诊病例的随访时间尚短,管理经验有限,此类患儿日后是否会出现代谢失衡、肝肾功能损害、复发性胰腺炎及其他临床表现还需要长期随访。新生儿筛查是否使更多无症状良性患者得以确诊也需进一步评估。
综上,CPT1A缺乏症是一种可筛可治,通过恰当干预预后相对较好的疾病。新生儿筛查是早期诊断CPT1A缺乏症的有效手段,生活管理及喂养指导可有效避免应激状态下的代谢失衡,减少CPT1A缺乏症发病。但CPT1A缺乏症的长期疾病管理、治疗方案及远期预后尚待深入研究。
参考文献
1 Merritt JL 2nd,Norris M,Kanungo S.Fatty acid oxidation disorders.Ann Transl Med,2018,6:473.
2 于玥,沈凌花,邱文娟,等.肉碱棕榈酰转移酶1A缺乏症患儿六例临床特征及基因突变分析.中华医学杂志,2021,101:1041-1044.
3 Chien YH,Lee NC,Chao MC,et al.Fatty acid oxidation disorders in a chinese population in taiwan.JIMD Rep,2013,11:165-172.
4 崔冬,胡宇慧,沈丹,等.一例肉碱棕榈酰1转移酶1A缺乏症患儿的临床特点及基因突变分析.中华医学遗传学杂志,2017,34:228-231.
5 张慧,袁远宏,唐莲,等.1例肉碱棕榈酰转移酶1A缺乏症的临床特点及CPT1A基因突变分析.儿科药学杂志,2019,25:23-27.
6 周珍,杨理明,廖红梅,等.一例肉碱棕榈酰转移酶1A缺乏症患儿的临床及
7 张志华,王兰,周霄颖,等.CPT1A基因外显子纯合缺失变异导致的肉碱棕榈酰转移酶1A缺乏症1例.南京医科大学学报(自然科学版),2021,41:1707-1709.
8 Gan Y,Yu F,Fang H.Novel mutation in carnitine palmitoyltransferase 1A detected through newborn screening for a presymptomatic case in China:a case report.Ital J Pediatr,2021,47:154.
9 Zhang W,Chen Y,Lin C,et al.Three novel and one potential hotspot CPT1A variants in Chinese patients with carnitine palmitoyltransferase 1A deficiency.Front Pediatr,2021,9:771922.
10 Zhang W,Chen Y,Lin C,et al.Three Novel and One Potential Hotspot CPT1A Variants in Chinese Patients With Carnitine Palmitoyltransferase 1A Deficiency.Front Pediatr.2021,9:771922.
11 Britton CH,Schultz RA,Zhang B,et al.Human liver mitochondrial carnitine palmitoyltransferase I:characterization of its cDNA and chromosomal localization and partial analysis of the gene.Proc Natl Acad Sci U S A,1995,92:1984-1988.
12 Casals N,Zammit V,Herrero L,et al.Carnitine palmitoyltransferase 1C:From cognition to cancer.Prog Lipid Res,2016,61:134-148.
13 Dykema DM.Carnitine palmitoyltransferase-1A deficiency:a look at classic and arctic variants.Adv Neonatal Care,2012,12:23-27.
14 Prasad C,Johnson JP,Bonnefont JP,et al.Hepatic carnitine palmitoyl transferase 1(CPT1 A) deficiency in North American Hutterites(Canadian and American):evidence for a founder effect and results of a pilot study on a DNA-based newborn screening program.Mol Genet Metab,2001,73:55-63.
15 Capalbo A,Valero RA,Jimenez-Almazan J,et al.Optimizing clinical exome design and parallel gene-testing for recessive genetic conditions in preconception carrier screening:Translational research genomic data from 14,125 exomes.PLoS Genet,2019,15:e1008409.
16 Elkhateeb N,Chakrapani A,Davison J,et al.Pancreatitis in multiple acyl CoA dehydrogenase deficiency:An underdiagnosed complication.JIMD Rep,2021,57:15-22.
17 Lee BH,Kim YM,Kim JH,et al.Atypical manifestation of carnitine palmitoyltransferase 1A deficiency:hepatosplenomegaly and nephromegaly.J Pediatr Gastroenterol Nutr,2015,60:e19-22.
17 Lee BH,Kim YM,Kim JH,et al.Atypical manifestation of carnitine palmitoyltransferase 1A deficiency:hepatosplenomegaly and nephromegaly.J Pediatr Gastroenterol Nutr.2015,60:e19-22.
18 Prasit P,Kanya S,Vorasuk S.Carnitine palmitoyl transferase 1A deficiency in an adult with recurrent severe steato hepatitis aggravated by high pathologic or physiologic demands:A roller-coaster for internists.Clin Mol Hepatol.2019,25:412-416.
(收稿日期:2023-07-26)