产后出血(postpartum hemorrhage,PPH)是最常见的分娩并发症之一,也是导致全球产妇死亡的重要因素,据报告占比超过27%[1]。PPH在发展中国家,特别是低收入国家负担最重[2],且近年来全球发病率呈上升趋势[3]。在中国,PPH已成为导致产妇死亡的首要原因[4]。尽管已知多生物学和社会学的风险因素都被认为与PPH的发展相关,但是缺乏使用综合数据的预测模型[5]。一些研究试图为PPH管理建立预测模型和工具,但是大多数方法不仅预测能力有限,而且尚未在独立的孕妇队列中进行验证[6-7],或未使用PPH的共识定义[8]。所以,尽管对PPH风险因素有很好的了解,但目前在临床实践中尚无PPH的预测工具。
人工智能(artificial intelligence,AI)可以增强妇产科知识的学习并支持医疗从业者的决策[9]。AI能够处理复杂的非线性关系和多维数据,这是传统统计方法无法做到。AI目前在妇产科领域应用,AI辅助试管受精[10]AI通过检测子宫信号预测早产试验[11],AI对多普勒超声图像进行处理可提高临床诊断不同妊娠阶段疾病的能力[9],依赖于AI算法的超声技术和康复训练在产后盆腔器官脱垂恢复中的应用[12],AI准确预测卵巢癌患者预后[13]等。但是关于AI应用于产后出血风险预测方面的研究较少。本文通过探讨传统PPH风险预测的局限性,突出机器学习算法在建立PPH的预测模型中的优势。
一、产后出血的定义和传统产后出血预测的局限
《世界卫生组织关于产后出血预防和治疗的建议》中将PPH定义为出生后24 h内出血≥500 mL,无论出生方式如何,重度PPH定义为出血量≥1 000 mL/24 h。2017年美国妇产科医师学会(ACOG)在《产后出血管理》中将产后出血定义为累计失血量≥1 000 mL或在产后24 h内出现与低血容量体征/症状相关的出血[14]。在中国,PPH的定义是胎儿娩出后24 h内,阴道分娩产妇失血量≥500 mL或剖宫产术失血量≥1 000 mL,或者失血后伴有低血容量的症状或体征[15]。不同的定义可能导致不同的发生率和不同的预测结果,尤其在多中心研究中。PPH作为全球产科发病率和死亡率的主要原因,约占发展中国家孕产妇死亡的8%,占发达国家孕产妇死亡的20%[7]。但是研究表明,产后出血在临床上经常被低估,实际发生率远高于报道。由于较多的出血量估计不准确,产后出血的预测仍然具有挑战。
历史上已有许多基于逻辑回归的PPH预测模型研究。在2020年发表的一篇系统综述中,开发了14个PPH预测模型[16]。虽然基于已确定的风险因素开发了有限数量的PPH预测模型,但大多数开发的模型未能在临床实践中实施,均存在研究外部验证不足、预测因子测量模糊、临床应用场景不明确等共性问题,影响模型的实际使用。在专业文献中,机器学习(machine learning,ML)模型的验证通常是作为内部验证进行的[17],但是在医学研究中,有研究指出外部验证被认为是必要的[18]。其次在临床问题中,影响临床结果的变量多,且各变量之间的关系复杂,传统的逻辑回归,可能不适合临床事件的统计和数学表达。因此,需要一个更准确的预测模型,可能需要一个包含更多参数的非线性关系,而不是线性关系,并将该模型应用于日常临床医学[19]。
二、ML在产后出血风险评估中的应用
近年来,ML作为AI的主要子集,可以处理具有大量变量的多维数据集中的复杂关系[20-21]。ML模型在预测产科并发症(如先兆子痫、胎儿宫内生长受限等)方面表现出色[22-23]。但在PPH风险预测方面的研究较少[24]。ML模型通过大规模临床数据训练,能够检测传统统计模型无法显现的变量关系[25]。这导致了基于ML的预测模型在准确性和灵敏度方面都优于传统方法,为PPH风险评估提供更加个性化的方法[26]。ML模型可以通过大规模的临床数据进行训练,并根据输入的预测指标输出相应的出血预测[24]。
Venkatesh等[27]测试了两种逻辑回归模型和两种机器学习模型,以确定是否有一种模型能从入院时的临床数据中预测产后出血,表明ML做得更好。Man等[28]研究发现,应用的ML方法可以更好地预测PPH风险。Liu等[29]创建了一个包含850例PPH的数据集,采用的传统的统计模型和ML来评估产后出血,发现ML模型在预测PPH方面表现出较好的性能。Homa等[30]的研究发现,ML在预测PPH方面比逻辑回归具有更高的判别性。ML提供了一种创新的解决方案,从而提高早期检测和及时干预。
ML有可能准确识别PPH风险最大的女性,并提高医疗结果和产科决策[31]。ML主要有两种学习方法,即监督学习和无监督学习。监督算法使用标记数据来学习作为输入的预测变量和作为结果的目标变量之间的相互作用。在系统性文献综述(systematic literature review,SLR)结果中,所有分析的文章都采用了监督学习方法来预测PPH。而关于是否可以扩展到无监督学习,还有待进一步研究。目前对PPH的发生率预测较多,但是对PPH的定量预测研究较少。然而,与预测PPH是否发生相比,定量预测PPH的优势更为明显。首先,定量预测PPH可以直观地预测具体的出血量。为临床医生进行术前评估提供了方便。二是有利于建立分级诊疗体系。临床医生可以提前将危重孕妇转移到先进医院,避免医疗资源的浪费。第三,有利于临床医生合理分配输血资源。本次研究旨在识别和评估与出血量相关的预测指标,建立可靠的定量预测模型。
本研究将是一项前瞻性多中心研究,参与者被分为两组,即产后出血组(PPH)和对照组。PPH组进一步分为六个亚组,根据既往的相关文献,本研究将这些亚组的临床数据与对照组一起被用于开发六种机器学习,评估其预测性能。模型的建立首先需要多中心数据的收集,所有潜在的预测因子包括人口统计信息,产科、内科、外科和家族史和实验室数据。社会人口学特征包括产妇的年龄、婚姻状况、种族等。临床特点包括体质指数(body mass index,BMI)、吸烟状况(是/否)、妊娠前产妇慢性身体疾病(根据ICD-9编码),包括恶性肿瘤、糖尿病、慢性肾病病史和甲状腺疾病等。妊娠合并症包括妊娠期糖尿病、妊娠期高血压疾病、妊娠期出血、妊娠剧吐、异常胎盘、妊娠期贫血和入院后的实验室数据(包括血细胞计数、铁、促甲状腺激素、血红蛋白、纤维蛋白、APTT、离子等)。妊娠期出血包括妊娠早期点滴出血以及妊娠后期和分娩前出血。异常胎盘分为三种即胎盘植入、双胎盘或前置胎盘。在这里,孕前BMI是一个预测因子,入院BMI是另一个预测因子,然而,本研究不确定怀孕期间体重增加是否是一个预测因素。排除标准:染色体或结构性胎儿畸形、妊娠早期和中期流产、由于身体其他部位外伤导致的大出血情况、胎儿死亡等。Grobman等[32]表明,在暴露于缩宫素12 h后,产后出血增加了三倍以上。产时数据的收集更为复杂,比如潜伏期和活跃期的时间,是否使用缩宫素引产,缩宫素使用时间,产程中专科检查次数,是否镇痛分娩,是否产程中转剖宫产和羊水粪染等。
在收集数据后,本研究需要进行预处理,以确定每个变量的重要性。预处理的主要步骤是将目标(分类)变量编码为数值变量,以便于计算。最终样本中所有协变量的描述性统计量:平均值(标准差)用于总结连续变量,计数(百分比)用于分类变量。数据收集结束后,探索性数据分析(exploratory data analysis,EDA)也是预测PPH的关键。EDA帮助本研究探索出血量数据的特征,识别数据质量问题,并为进一步的数据处理和分析做准备[33]。众所周知,机器学习方法会在缺失值的情况下产生错误[34] 。为了避免这种情况,本研究按以下方式输入:具有缺失值和未知值的分类变量被分配到“未知”类别;缺失值和未知值的连续变量编码为中位数。模型使用80%的数据集进行训练,剩下的20%用于测试它们的预测准确性。模型开发后,在验证数据集上检测PPH模型。本研究在处理后的数据集上使用6个ML模型,分别是逻辑回归、线性回归、梯度增强(gradient boosting,GB)、梯度提升决策树模型(XGBoost)、多层感知器和随机森林。每个算法都经过训练,根据输入变量(如产妇病史、产科因素和分娩特征)预测产后出血的量,根据标准评价指标对每种算法的性能进行评估,包括准确性、敏感性、特异性和受试者工作特征(receiver operating characteristic cune,ROC)的曲线下面积(area under the curve,AUC),发现最适合PPH定量预测的风险指标。
三、基于ML的产后出血评估模型
各种ML技术根据对疾病诊断的临床数据进行分类,显示不同的预测性能。逻辑回归算法适用于结果是明确的问题。线性回归是预测连续结果的基础统计技术。它需要对相关指标之间的线性关系进行建模。梯度增强是一种增量构建预测模型的集成ML方法。XGBoost是梯度增强的优化实现,以其在预测建模中的效率和性能而闻名。它在回归和分类任务方面都表现出色,通常优于其他算法。多层感知器是一种具有多层相互连接节点的人工神经网络。它可以捕获数据集中的复杂模式和关系,使其适合复杂的回归任务。随机森林是一种在训练过程中构造多棵决策树的集成学习算法。它可以提高回归任务的准确性,这对于处理嘈杂的数据和避免过度拟合特别有益。XGBoost算法以其快速计算、强大的泛化能力和高预测性能而闻名。同样,随机森林算法构建了多个决策树,擅长处理大型和非线性数据集,从而提高了识别关键预测特征的准确性。
Westcott等[35]基于ML技术开发了一种PPH的预测模型,从电子病历中收集了471个变量,结果表明,XGBoost在产后出血分类方面表现最佳。Venkatesh等[27]比较了基于ML的模型(随机森林和梯度增强)和基本统计模型(使用和不使用套索正则化的逻辑回归),以预测产后出血(估计失血量大于1 000 mL)的最佳模型;结果表明,梯度增强模型表现最好(95% CI:0.92~0.93),随机森林模型也获得了令人满意的结果(95% CI:0.91~0.92),而逻辑回归较差。Homa等[30]发现,梯度增强在预测PPH方面表现最好。但是有的研究结果却不尽如此。Betts等[24]研究发现,XGB模型预测PPH的成功有限(AUC小于0.700)。Akazawa等[19] 研究发现,逻辑回归在预测PPH中表现最好,其次是随机森林。这可能归因于临床数据的使用和不同样本的预测效果不足。某些模型可能在特定类型的数据集上表现更好,而另一些模型则更适合处理非线性关系。最近的研究使用ML预测产后出血,证明了ML的潜力[36]。这些不同的发现突出了算法选择、数据集特征和模型验证在PPH预测研究中的重要性,强调了在未来的研究中需要仔细考虑这些因素。
四、挑战、限制与未来方向
ML利用具有复杂特征的大型数据集,实现高精度、预测质量和灵敏度的结合。但是,ML模型在临床应用中仍面临挑战,如数据集质量、模型过拟合、缺乏外部验证等 [20]。此外,确定疾病预测的最佳临床风险因素也是一个需要改进的具有挑战性的问题。未来研究应优先考虑高质量变量的大数据分析,并在不同人群和环境中验证模型的可靠性和通用性,发展多中心数据库、多学科合作和国际合作将加速这一领域的研究进展。
1 OBrien KL,Shainker SA,Lockhart EL.Transfusion management of obstetric hemorrhage.Transfus Med Rev,2018,32:249-255.
2 Amanuel T,Azmach D,Aregahegn D.Postpartum hemorrhage and its associated factors among women who gave birth at Yirgalem General Hospital,Sidama Regional State,Ethiopia.Health Serv Res Manag Epidemiol,2021,8:23333928211062777.
3 World Health Organization.Maternal mortality.World Health Organization [Internet],2018.
4 王霞,卡前列素氨丁三醇注射液治疗宫缩乏力性产后出血的临床疗效.中国药物与临床,2021,21:3147-3149.
5 Islam MN,Mustafina SN,Mahmud T,et al.Machine learning to predict pregnancy outcomes:a systematic review,synthesizing framework and future research agenda.BMC Pregnancy Childbirth,2022,22:348.
6 Biguzzi E,Franchi F,Ambrogi F,et al.Risk factors for postpartum hemorrhage in a cohort of 6011 Italian women.Thromb Res,2012,129:e1-7.
7 Koopmans CM,van der Tuuk K,Groen H,et al.Prediction of postpartum hemorrhage in women with gestational hypertension or mild preeclampsia at term.Acta Obstet Gynecol Scand,2014,93:399-407.
8 Rubio-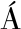 lvarez A,Molina-Alarcón M,Arias-Arias
lvarez A,Molina-Alarcón M,Arias-Arias 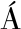 ,et al.Development and validation of a predictive model for excessive postpartum blood loss:A retrospective,cohort study.Int J Nurs Stud,2018,79:114-121.
,et al.Development and validation of a predictive model for excessive postpartum blood loss:A retrospective,cohort study.Int J Nurs Stud,2018,79:114-121.
9 Bhattad PB,Jain V,Artificial intelligence in modern medicine - the evolving necessity of the present and role in transforming the future of medical care.Cureus,2020,12:8041-8051.
10 Beam AL,Kohane IS.Big data and machine learning in health care.JAMA,2018,319:1317-1322.
11 Malani SN,Shrivastava D,Raka MS.A comprehensive review of the role of artificial intelligence in obstetrics and gynecology.Cureus,2023,15:e34891.
12 Iftikhar P,Kuijpers MV,Khayyat A,et al.Artificial intelligence:a new paradigm in obstetrics and gynecology research and clinical practice.Cureus,2020,12:7124-7130.
13 Enshaei A,Robson CN,Edmondson RJ.Artificial intelligence systems as prognostic and predictive tools in ovarian cancer.Ann Surg Oncol,2015,22:3970-3975.
14 Committee on Practice Bulletins -Obstetrics.Practice Bulletin No.183:Postpartum Hemorrhage.Obstet Gynecol,2017,130:e168-e186.
15 产后出血预防与处理指南(2023),中华妇产科杂志,2023,58:401-409.
16 Neary C,Naheed S,McLernon DJ,et al.Predicting risk of postpartum haemorrhage:a systematic review.BJOG,2021,128:46-53.
17 Jie M,Mark H,Lei M.Machine learning testing:survey,landscapes and horizons.in IEEE Trans Softw Eng,2022,48:1-36.
18 Ewout WS,Frank EH.Prediction models need appropriate internal,internal-external,and external validation.J Clin Epidemiol,2016,69:245-257.
19 Akazawa M,Hashimoto K,Katsuhiko N,et al.Machine learning approach for the prediction of postpartum hemorrhage in vaginal birth.Sci Rep,2021,11:22620.
20 Ahn KH,Lee KS.Artificial intelligence in obstetrics.Obstet Gynecol Sci,2022,65:113-124.
21 Averbuch T,Sullivan K,Sauer A,et al.Applications of artificial intelligence and machine learning in heart failure.Eur Heart J Digit Health,2022,3:311-322.
22 Vicoveanu P,Vasilache IA,Scripcariu IS,et al.Use of a Feed-Forward Back Propagation Network for the Prediction of Small for Gestational Age Newborns in a Cohort of Pregnant Patients with Thrombophilia.Diagnostics (Basel),2022,12:1009-1020.
23 Melinte PM,Vasilache IA,ocolov D,et al.Prediction of HELLP syndrome severity using machine learning algorithms-results from a retrospective study.Diagnostics,2023,13:287-297.
24 Betts KS,Kisely S,Alati R.Predicting common maternal postpartum complications:leveraging health administrative data and machine learning.BJOG,2019,126:702-709.
25 Obermeyer Z,Emanuel EJ.Predicting the future - big data,machine learning,and clinical medicine.N Engl J Med,2016,375:1216-1219.
26 Kawakita T,Mokhtari N,Huang JC,et al.Evaluation of risk-assessment tools for severe postpartum hemorrhage in women undergoing cesarean delivery.Obstet Gynecol,2019,134:1308-1316.
27 Venkatesh KK,Strauss RA,Grotegut CA,et al.Machine learning and statistical models to predict postpartum hemorrhage.Obstet Gynecol,2020,135:935-944.
28 Man Z.Comparative study of machine learning models to predict PPH.Master′s Paper.The University of North Carolina at Chapel Hill,2019.
29 Liu J,Wang C,Yan R,et al.Machine learning-based prediction of postpartum hemorrhage after vaginal delivery:combining bleeding high risk factors and uterine contraction curve.Arch Gynecol Obstet,2022,306:1015-1025.
30 Homa A,Alexa D,Mike B,et al.Machine learning for prediction of maternal hemorrhage and transfusion.Preprints,2022,3:1-4.
31 Mienye ID,Sun Y,Wang Z.An improved ensemble learning approach for the prediction of heart disease risk.Informat Med Unlocked,2020,20:100402-100412.
32 Grobman WA,Bailit J,Lai Y,et al.Defining failed induction of labor.Am J Obstet Gynecol,2018,218:122.e1-122.e8.
33 Faramarzi A,Heidarinejad M,Stephens B,et al.Equilibrium optimizer:A novel optimization algorithm.Knowl-Based Syst,2020,191:105-110.
34 Nijman S,Leeuwenberg AM,Beekers I,et al.Missing data is poorly handled and reported in prediction model studies using machine learning:a literature review.J Clin Epidemiol,2022,142:218-229.
35 Westcott JM,Hughes F,Liu W,et al.Prediction of maternal hemorrhage:using machine learning to identify patients at risk.Am J Obstet Gynecol,2020,222:407-414.
36 Zhang Y,Chen L,Zhou W,et al.Nomogram to predict postpartum hemorrhage in cesarean delivery for twin pregnancies:A retrospective cohort study in China.Front Med,2023,10:1139-1145.