多囊卵巢综合征(polycystic ovary syndrome, PCOS)是一种与内分泌失调相关的生殖功能障碍,最常见于育龄妇女[1]。PCOS患者会出现多种严重的临床后遗症,包括高雄激素血症、持续性无排卵、多囊卵巢、胰岛素抵抗和肥胖等[2-3]。“阴平阳秘”是中医基础理论的重要内容之一,指的是阴气平和、阳气固密,阴阳两者相互协调,保持相对平衡的状态[4]。这种平衡状态是人体健康的基础,故而精气血津液、脏腑经络、四肢百骸各就其位,各司其职,精(物质)、气(信息)、神(功能)皆备,达到形神统一,正气存内,邪不可干之境界[5]。阴平阳秘的失衡可能表现为阴虚火旺,导致月经不调、肥胖、多毛等症状,这些都是PCOS的典型表现[6]。近年来,昼夜节律变化在PCOS中的作用引起了相当大的关注,昼夜节律紊乱可能影响内分泌系统的正常功能,影响下丘脑-垂体-卵巢轴的协调,导致激素如促黄体生成素(luteinizing hormone, LH)和卵泡刺激素(follicle-stimulating hormone, FSH)分泌异常,这是PCOS发生的一个重要标志[7]。昼夜节律紊乱可以通过氧化应激和炎症等机制触发或加速PCOS患者体内阴阳失衡,从而加重PCOS[8]。本研究基于“阴平阳秘”理论探讨昼夜节律紊乱对PCOS模型大鼠性激素及卵巢形态的影响,以及可能的作用机制。
材料与方法
一、实验动物
40只SD雌性大鼠,21日龄,购自成都达硕实验动物有限公司,许可证编号SCXK(川)2020-0030。本动物实验经山西中医药大学医学伦理委员会审查,认为该项目符合医学伦理学要求,同意申报,项目批准号:AWE202209037。
二、实验材料及仪器
脱氢表雄酮(DHEA)(货号:D106380)购自上海阿拉丁生化科技股份有限公司。HRP标记山羊抗兔IgG(货号:GB23303)购自武汉赛维尔生物科技有限公司。Rat LH ELISA KIT(货号:ZC-36719)、Rat E2 ELISA KIT(货号:ZC-36464)、Rat T ELISA KIT(货号:ZC-36635)、Rat FSH ELISA KIT(货号:ZC-36477)购自上海茁彩生物科技有限公司。Smad1/5/9(货号:ab300164)购自Abcam。BMP6(货号:A8333)、Smad4(货号:A17116)、β-actin(货号:AC026)单克隆抗体购自Abclonal。WB试剂盒(货号:P0013)、BCA蛋白定量试剂盒(货号:P0009)购自上海碧云天生物技术有限公司。酶标仪(SpectraMAX Plus384)购自美谷分子仪器有限公司。荧光图像分析系统(5200 Multi)购自Tanon。台式高速冷冻离心机(H2050R)购自湘仪集团。超薄切片机(UC7rt)购自LEICA。透射电子显微镜(JEM-1400FLASH)购自日本电子(JEOL)。
三、方法
1.动物造模与分组:SD大鼠,21日龄,适应性饲养1周后,随机分为对照组10只、PCOS模型组30只。对照组大鼠在正常光照(光∶暗=12 h∶12 h)下饲养,并皮下注射大豆油,1次/天,连续3周。PCOS组大鼠采用脱氢表雄酮(DHEA)注射法构建PCOS模型大鼠,具体步骤:正常光照(光∶暗=12 h∶12 h)下饲养,并皮下注射DHEA 60 mg/kg(溶于注射用大豆油),1次/天,连续3周。每天观察大鼠摄食、毛发及精神一般活动情况,出现体型肥胖,体重上升,喜静不喜动,初步判定造模成功。从造模第12天开始,每日9:00取阴道冲洗液脱落细胞涂片,检测发情周期变化,连续10 d。造模结束后ELISA检测性激素水平。
2.动物分组与处理:造模成功的PCOS模型大鼠30只,随机分为PCOS组、PCOS+PL组(长光照组)、PCOS+CL组(持续光照组),各10只,PCOS组大鼠在正常光照(光∶暗=12 h∶12 h)下饲养,PCOS+PL组在长光照(光∶暗=18 h∶6 h)条件下饲养,PCOS+CL组在持续光照(光∶暗=24 h∶0 h)条件下饲养,对照组大鼠在正常光照(光∶暗=12 h∶12 h)下饲养,连续3周。
3.ELISA法检测血清LH、FSH、E2、T水平:采集全血进行离心处理,以3 000 r/min,离心5 min,-70 ℃保存,采用ELISA法检测,加入样品、对照品后37 ℃反应30 min,洗板5次,加入酶标试剂,37 ℃反应30 min,再次洗板,加入显色液,37 ℃显色10 min,加入终止液,在450 nm波长处测定各孔的OD值,计算大鼠血清LH、FSH、E2、T水平。
4. 大鼠体重及卵巢系数计算:记录各组大鼠卵巢质量与体质量,并计算卵巢系数(相对质量),卵巢系数=卵巢质量/体质量。
5. HE染色观察卵巢组织形态及有腔卵泡和囊状卵泡计数:采血结束后,脱颈处死大鼠,分离出卵巢组织。甲醛固定卵巢组织,无水乙醇脱水处理,二甲苯透明、包埋,切片机切片,苏木精染色10 min,自来水冲洗3 min,伊红染色5 min;梯度乙醇脱水,二甲苯透明,中性树胶封固,光学显微镜观察卵巢组织病理学变化,并进行有腔卵泡和囊状卵泡计数。
6. 透射电镜观察卵巢组织超微结构变化:将大鼠麻醉后断头,于冰上取卵巢组织并修成1 mm3的小块,置于4% 的戊二醛内固定2 h以上。1%四氧化锇酸再固定2 h,PBS冲洗。梯度丙酮脱水,包埋剂包埋,恒温箱内聚合。1 μm半薄切片,甲苯胺蓝染色定位,50~70 nm 超薄切片,柠檬酸铅-醋酸双氧铀双染,透射电子显微镜下观察,拍照。
7. Western blot检测BMP6、Smad4和Smad1/5/9蛋白水平:取大鼠卵巢组织研磨,提取组织中总蛋白,对蛋白定量(BCA 试剂盒),进行 SDS-PAGE 凝胶电泳分离,分离蛋白转到 PVDF 膜,封闭,加入一抗BMP6(1:2 000);Smad4(1:2 000);Smad1/5/9(1:1 000);β-actin(1:50 000),4 ℃孵育过夜;将PVDF膜放入二抗(稀释浓度为1:5 000)中,室温孵育2 h,ECL显色,测定蛋白表达情况。
四、统计学处理
采用SPSS 20.0软件进行统计学分析,计量资料以均数±标准差![]() 表示,多组间采用单因素方差检验,进一步两两比较,采用LSD-t检验,P<0.05表示差异有统计学意义。
表示,多组间采用单因素方差检验,进一步两两比较,采用LSD-t检验,P<0.05表示差异有统计学意义。
结果
一、 PCOS模型大鼠一般情况及动情周期变化结果
对照组大鼠展现出5~6 d的正常动情周期,涵盖动情前期、动情期、动情后期及动情间期。在动情前期,观察到含有细胞核的圆形上皮细胞;动情期则主要是形态不规则的、无细胞核的角化鳞状上皮细胞;动情后期,上皮细胞数量减少,白细胞增多,角化细胞含量降低;动情间期则表现为白细胞的大量出现。相较之下,PCOS组动情周期不规律,无交替变化的规律发情周期或动情周期延长,表现为持续角化的阴道上皮细胞,结果见图1。
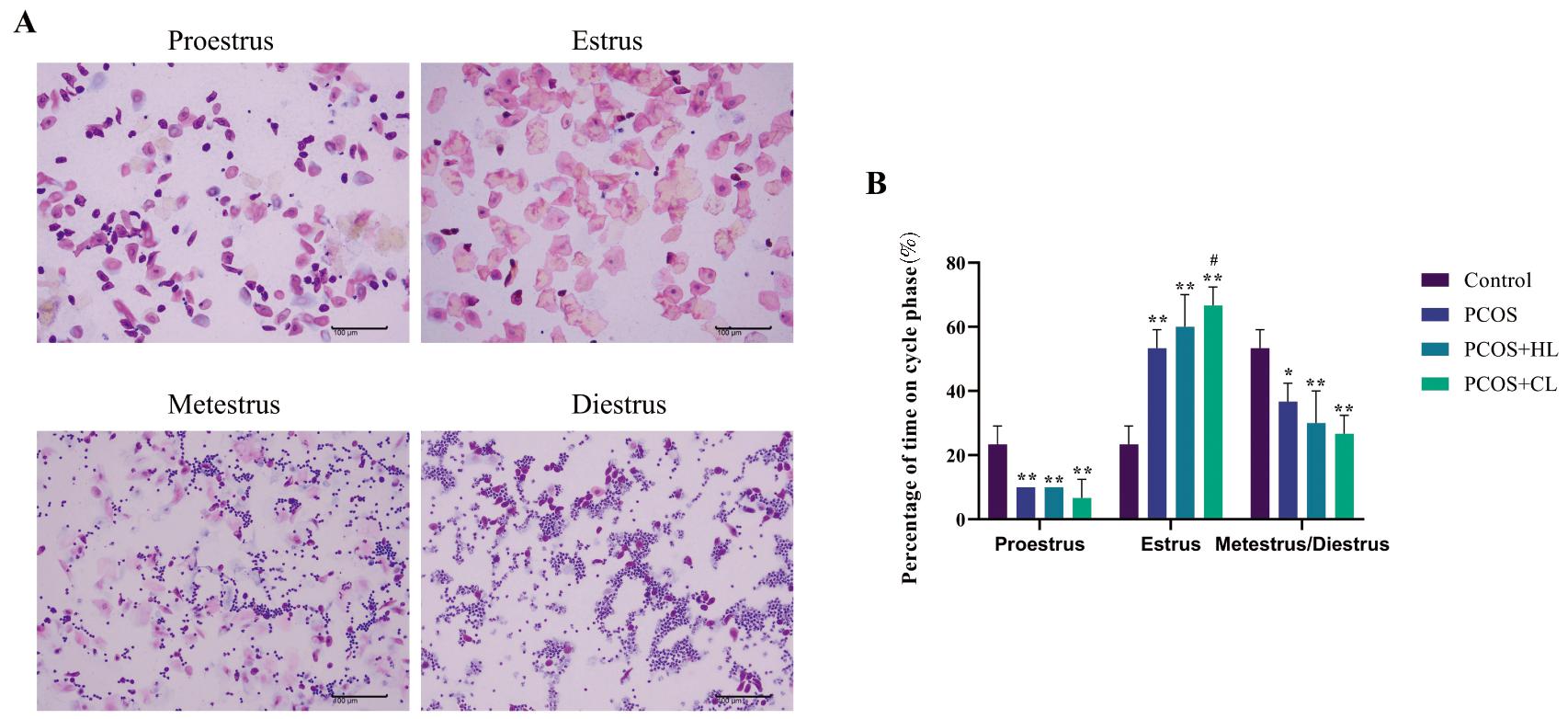
Note:Compared with Control group,*P<0.05,**P<0.01;Compared with PCOS group,#P<0.05
图1 大鼠动情周期统计(Proestrus:动情前期,Estrus:动情期;Metestrus:动情后期; Diestrus:动情间期)
A:显微镜下阴道涂片B:不同组大鼠动情周期统计柱状图
Figure 1 Estrus cycle statistics of female mice in PCOS group and control group A: Microscopic vaginal smear B: Bar chart of estrous cycle statistics of different groups of rats
二、大鼠体重及卵巢相对质量的检测结果
造模完成后,PCOS大鼠体重大于对照组,但无统计学差异。计算卵巢相对重量发现,与对照组相比,PCOS组、PCOS+PL组和PCOS+CL组大鼠卵巢系数显著升高(P<0.05);与PCOS组相比,PCOS+CL组大鼠卵巢系数显著升高(P<0.01),PCOS+HL组与PCOS组相比差异无统计学意义。结果见表1。
表1 各组大鼠体重及卵巢系数的检测结果![]()
Table 1 Results of body weight and ovarian coefficient of rats in each ![]() n=10)
n=10)
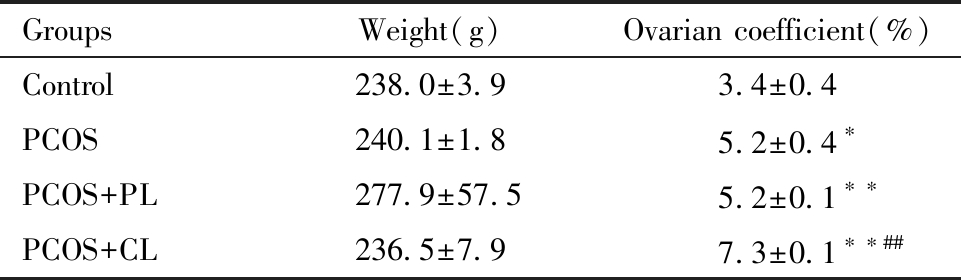
Note:Compared with Control group,*P<0.05,**P<0.01;Compared with PCOS group,##P<0.01
GroupsWeight(g)Ovarian coefficient(%)Control238.0±3.93.4±0.4PCOS240.1±1.85.2±0.4∗PCOS+PL277.9±57.55.2±0.1∗∗PCOS+CL236.5±7.97.3±0.1∗∗##
三、大鼠卵巢组织病理形态学观察及有腔卵泡和囊状卵泡计数结果
对照组卵巢被膜完整,皮质区原始卵泡、初级卵泡及次级卵泡等数量较为正常,各级卵泡发育正常;髓质区纤维结缔组织排列紧密,未见明显水肿或坏死,未见明显的炎细胞浸润及纤维组织增生。PCOS组卵巢结构发生病理性改变,卵巢内见囊状扩张卵泡并呈现多囊样病理改变,锁闭卵泡多发,潴留囊肿明显,颗粒细胞减少,卵泡膜细胞增多。PCOS组、PCOS+PL组和PCOS+CL组卵巢内见囊状扩张卵泡较多并呈现多囊样病理改变,锁闭卵泡多发,颗粒细胞层明显变薄、数量减少,卵泡膜细胞增多,且PCOS+CL组较为明显。与对照组相比,PCOS组、PCOS+PL组和PCOS+CL组有腔卵泡及囊性卵泡数量增多(P<0.01);与PCOS组相比,PCOS组+PL组有腔卵泡和囊状卵泡数量增加但差异无统计学意义,PCOS+CL组,有腔卵泡数量(P <0.05)、囊状卵泡数量(P <0.01)显著增加。结果见图2。
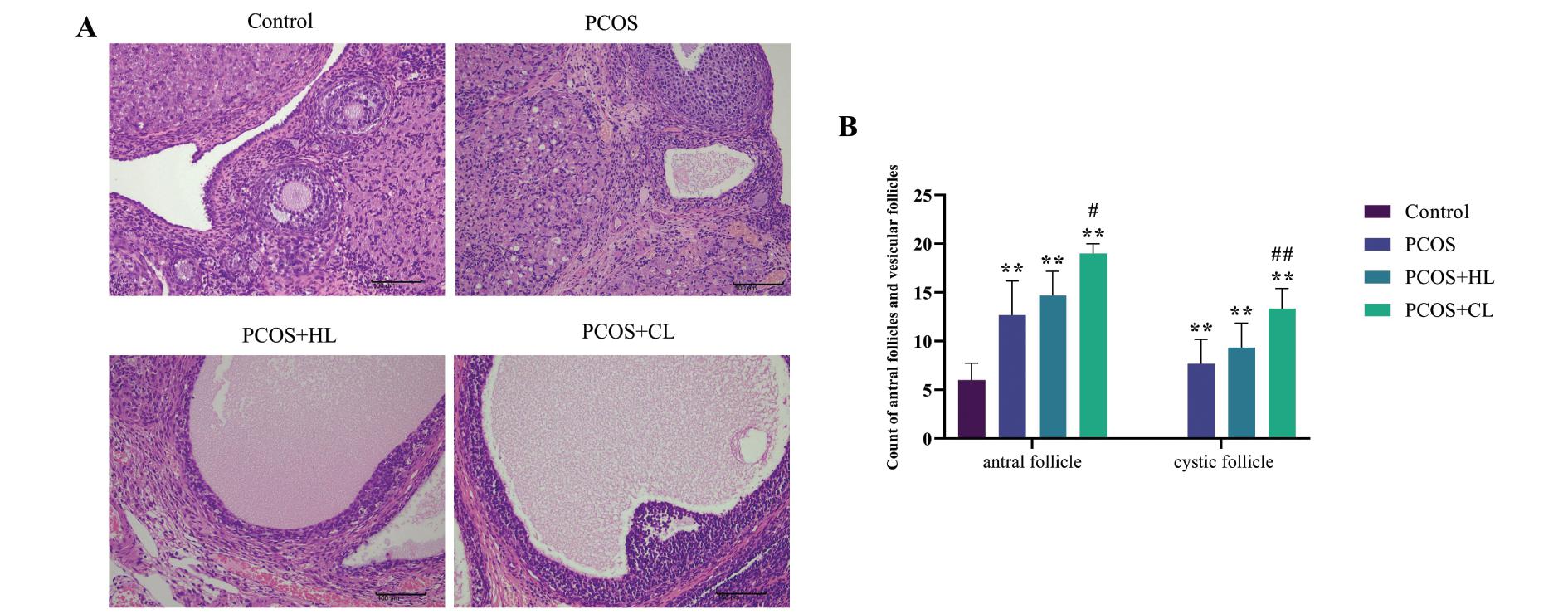
Note:Compared with Control group,**P<0.01;Compared with PCOS group,#P<0.05,##P<0.01
图2 HE染色观察各组大鼠卵巢组织病理形态学及有腔和囊状卵泡计数(×200)
A:卵巢组织HE染色病理图B:有腔和卵状囊泡数量统计柱状图
Figure 2 HE staining was used to observe the ovarian histopathology and the number of antral follicles and vesicular follicles in each group(×200)
A: HE-stained pathological image of ovarian tissue B: Bar chart of the number of antral follicles and vesicular follicles
四、大鼠卵巢组织中卵泡细胞超微结构改变情况
对照组颗粒细胞的细胞核和胞浆中细胞器均正常;PCOS组颗粒细胞的细胞核正常,胞浆中细胞器轻微异常;PCOS+PL组颗粒细胞的细胞核无明显异常,胞浆中细胞器出现较明显异常;PCOS+CL组颗粒细胞的细胞核固缩,胞浆中细胞器明显异常。结果见图3。
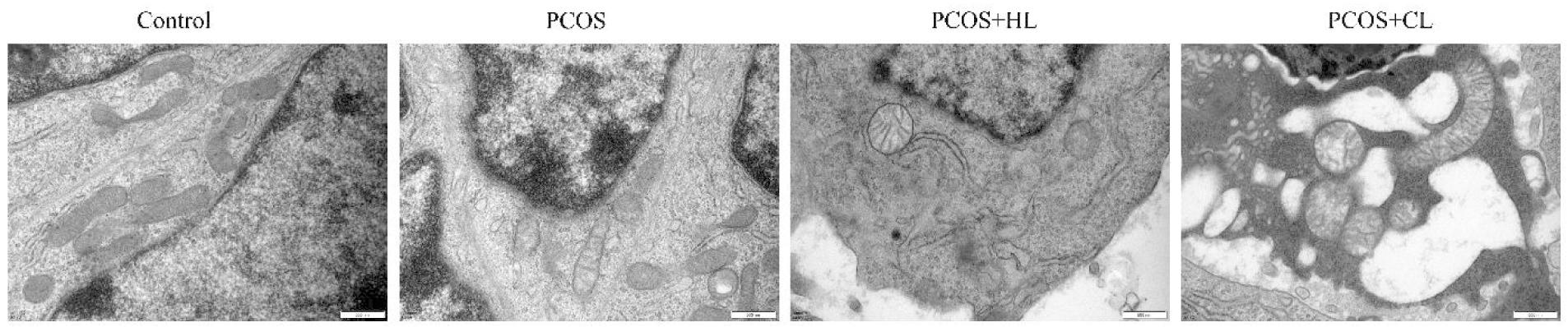
图3 各组大鼠卵巢组织细胞超微结构(×20 000,Bar=500 nm)
Figure 3 Ultrastructure of ovarian cells in each group(× 20 000, Bar=500 nm)
五、大鼠血清中LH、FSH、E2、T水平的检测结果
与对照组相比,PCOS组、PCOS+PL组和PCOS+CL组大鼠血清中LH、E2、T水平均显著升高(P<0.01),FSH水平显著降低(P<0.01);与PCOS组比较,PCOS+PL组大鼠血清中E2、T水平均显著升高(P<0.05),FSH水平显著降低(P<0.05),LH水平差异无统计学意义(P>0.05),PCOS+CL组大鼠血清中LH、E2、T水平均显著升高(P<0.01),FSH水平显著降低(P<0.01),结果见表2。
表2 各组大鼠LH、FSH、E2、T浓度的变化![]()
Table 2 Changes of LH, FSH, E2, T concentrations in each ![]() n=10)
n=10)
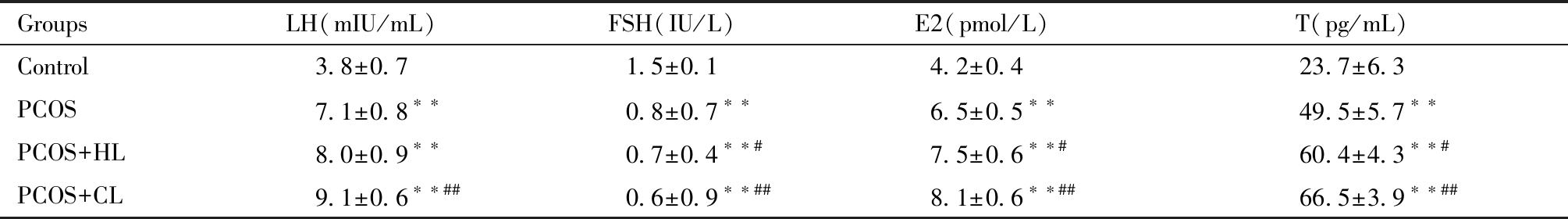
Note:Compared with Control group,**P<0.01; Compared with PCOS group,#P<0.05,##P<0.01
GroupsLH(mIU/mL)FSH(IU/L)E2(pmol/L)T(pg/mL)Control3.8±0.71.5±0.14.2±0.423.7±6.3PCOS7.1±0.8∗∗0.8±0.7∗∗6.5±0.5∗∗49.5±5.7∗∗PCOS+HL8.0±0.9∗∗0.7±0.4∗∗#7.5±0.6∗∗#60.4±4.3∗∗#PCOS+CL9.1±0.6∗∗##0.6±0.9∗∗##8.1±0.6∗∗##66.5±3.9∗∗##
六、大鼠卵巢组织中BMP6、Smad4和Smad1/5/9蛋白水平表达检测结果
通过Western blot检测各组大鼠卵巢组织BMP6、Smad4和Smad1/5/9蛋白表达水平结果如下,与对照组相比,PCOS组、PCOS+PL组和PCOS+CL组中BMP6、Smad4和Smad1/5/9蛋白表达水平均显著降低(P<0.01);与PCOS组相比,PCOS+PL组和PCOS+CL组中BMP6、Smad4和Smad1/5/9蛋白表达水平均显著降低(P<0.01)。结果见图4、表3。
表3 各组大鼠BMP6、Smad4和Smad1/5/9蛋白表达水平比较![]()
Table 3 Comparison of BMP6, Smad4 and Smad1/5/9 protein expression in each ![]() n=10)
n=10)
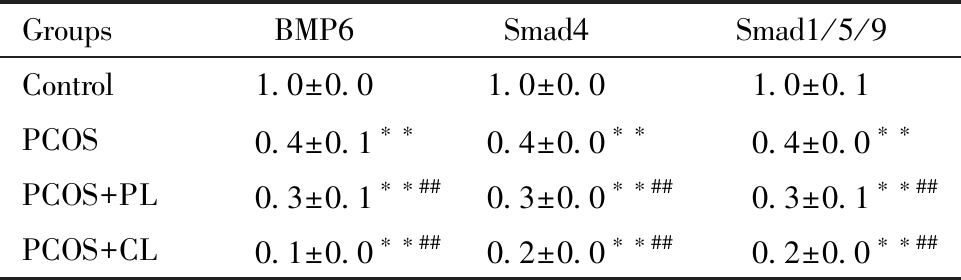
Note:Compared with Control group,**P<0.01; Compared with PCOS group,##P<0.01
GroupsBMP6Smad4Smad1/5/9Control1.0±0.01.0±0.01.0±0.1PCOS0.4±0.1∗∗0.4±0.0∗∗0.4±0.0∗∗PCOS+PL0.3±0.1∗∗##0.3±0.0∗∗##0.3±0.1∗∗##PCOS+CL0.1±0.0∗∗##0.2±0.0∗∗##0.2±0.0∗∗##
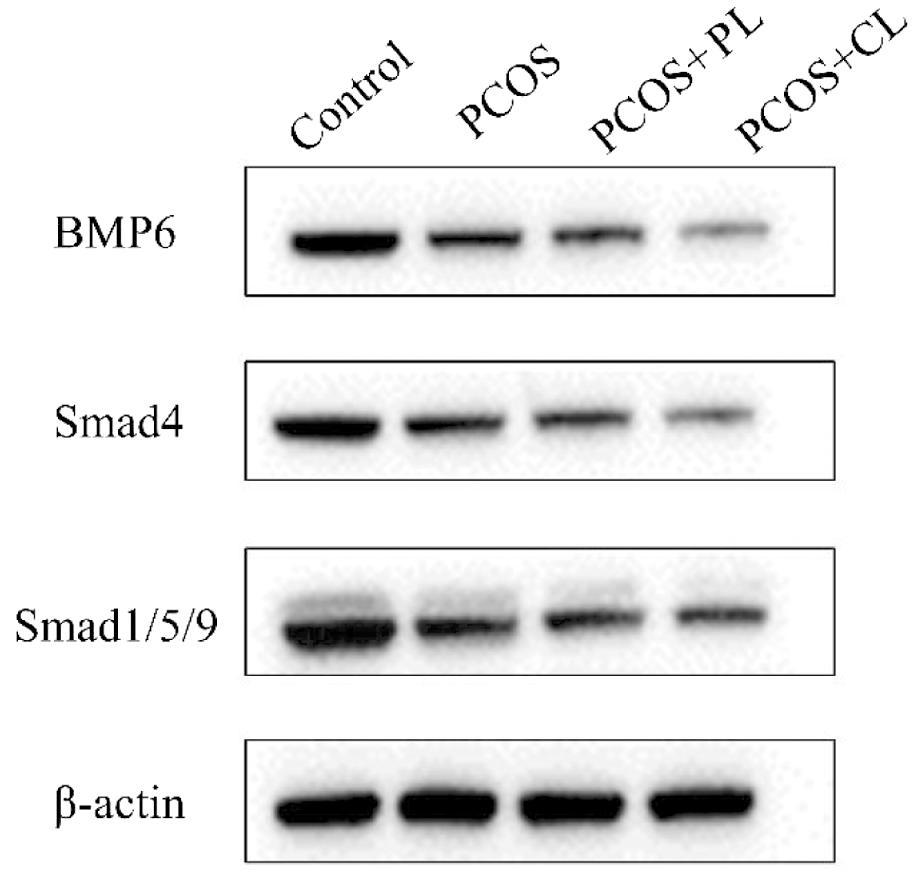
图4 各组大鼠BMP6、Smad4和Smad1/5/9蛋白表达情况
Figure 4 BMP6, Smad4 and Smad1/5/9 protein expression in each group
讨论
多卵巢综合征(PCOS)是一种复杂的内分泌疾病,其特征包括排卵不足或无排卵、雄激素水平高、多囊卵巢等[9]。育龄女性PCOS的患病率为10%~15%,已成为影响生殖和代谢最常见的综合征[10]。近年来,环境因素特别是昼夜节律紊乱在PCOS调查中引起了广泛关注[11]。昼夜节律通过位于下丘脑视交叉上核(SCN)的主要昼夜节律起搏器调控,SCN会根据环境的光/暗周期来调整内部时间顺序,以确保生理和行为节奏与昼夜节律、睡眠和清醒、体温、进食等在24 h周期内协调进行[12-13]。迄今为止,一些研究已经揭示了昼夜节律与PCOS之间的密切关系。患有PCOS的青春期女孩经历了昼夜节律紊乱,另一项研究表明,PCOS患者似乎更容易受到昼夜节律紊乱的影响,可能是由于异常的褪黑激素水平参与神经内分泌病理过程[14-15]。“阴平阳秘”学术理论最早出自《黄帝内经》,不仅是中医预防医学的精粹,也是治疗疾病的指导思想[16]。昼为阳,夜为阴,不同的时间段,阴阳的盛衰也随之变化,人体阴阳失衡时,也可能会影响身体内部的调节机制,进而影响正常的昼夜节律[17]。而长期的昼夜节律紊乱可能会损耗人体的阴气和阳气,使得阴阳之间的相互制约和相互依存关系失衡。本实验成功制备PCOS模型大鼠,研究结果显示昼夜节律紊乱会增加大鼠体重、卵巢系数降低,卵巢组织形态较PCOS组加重,有腔卵泡和囊状卵泡数量增加,表明昼夜节律紊乱加速PCOS发生发展。
LH、FSH、E2 以及相应的激素受体共同对卵巢发挥作用,对雌孕激素的分泌予以调控,从而对雌性机体的动情周期、卵泡发育以及排卵进程产生影响[18]。PCOS 患者存在 LH、FSH 分泌的不均衡状况,表现为 LH 水平上升,FSH 水平降低;LH 水平的增高会进一步促使卵泡膜细胞大量合成 T,于卵巢中营造出高雄激素的环境,进而对优势卵泡的发育造成阻碍[19-20]。PCOS患者卵巢和血液中E2水平通常会升高,反映了颗粒细胞功能障碍和雌激素生成增加[21]。研究表明,持续光照会刺激LH的分泌,引起啮齿类动物卵巢形态的变化和高雄激素血症,表明昼夜节律的变化可能引发PCOS[22-23]。此外还有研究发现,人类和动物持续暴露在光照下也会导致FSH和E2水平升高[24]。本研究结果发现,昼夜节律紊乱可升高LH、E2和T水平,可降低FSH水平,且光照时间越长激素分泌越紊乱。
骨形态发生蛋白(BMP)属于转化生长因子β(TGF-β)超家族,对于维持女性生殖健康非常重要[25]。先前的研究发现,BMP2、BMP4、BMP6和BMP7等多种BMP蛋白能够调节人类颗粒细胞中透明质酸的合成,进而影响排卵[26-27]。这些蛋白通过与TGF-β的I型和II型受体结合,在细胞膜上发生磷酸化,激活胞内信号传导介质SMAD1/5/9[28]。尤其是BMP6,已被证实通过调节卵巢间细胞通讯,对哺乳动物的卵泡功能、卵母细胞成熟和黄体功能发挥调控作用[29]。临床研究表明,卵巢中BMP6信号传导的异常与多囊卵巢综合征及排卵障碍的发病机制密切相关[30]。综上所述,BMP6是维持正常卵泡发育的关键内源性调节因子。Smad4是经典 BMP/Smad信号通路的最终信号分子且可以通过正反馈调节经典 BMP/Smad信号通路[31]。研究表明,Smad4是BMP6诱导的下游信号通路中不可或缺的介质[32]。由此推测昼夜节律紊乱可能通过调节BMP/Smad信号通路来诱发或加速PCOS发展。本研究结果发现,PCOS模型大鼠卵巢组织中BMP6、Smad4和Smad1/5/9表达水平显著降低,即BMP/Smad信号轴被抑制。持续光照后,大鼠卵巢组织中BMP6、Smad4和Smad1/5/9表达水平显著降低,可见昼夜节律紊乱可通过下调BMP/Smad信号通路来加重PCOS。
综上所述,昼夜节律紊乱破坏体内阴阳平衡,加重PCOS大鼠性激素分泌失常,影响卵巢正常功能和形态,其作用机制可能与下调BMP/Smad信号通路有关。本研究为理解昼夜节律紊乱与PCOS之间的关系提供了新的视角,也为探索基于“阴平阳秘”理论的干预策略提供了科学依据,为PCOS的治疗提供新的思路和方法。
1 Chen WH,Huang QY,Wang ZY,et al.Therapeutic potential of exosomes/miRNAs in polycystic ovary syndrome induced by the alteration of circadian rhythms.Front Endocrinol(Lausanne),2022,13:918805.
2 Velez LM,Seldin M,Motta AB.Inflammation and reproductive function in women with polycystic ovary syndrome.Biol Reprod,2021,104:1205-1217.
3 Sadeghi HM,Adeli I,Calina D,et al.Polycystic ovary syndrome:a comprehensive review of pathogenesis,management,and drug repurposing.Int J Mol Sci,2022,23:583.
4 郝燕,王鹏."阴平阳秘,精神乃治"的内涵探究.广西中医药大学学报,2024,27:70-72.
5 陆黎娟,曾薇薇,张婷婷,等.基于“阴平阳秘”思想的子宫内膜异位症免疫稳态相关研究进展.中华中医药学刊,2022,40:24-28.
6 魏春花,李海艳,朱淑平.阿司匹林联合地屈孕酮对肥胖型PCOS患者子宫内膜容受性及胰岛素抵抗的影响观察.哈尔滨医药,2023,43:56-58.
7 程冉,方晓红,朱颖,等.加味桂枝甘草龙骨牡蛎汤治疗多囊卵巢综合征合并昼夜节律紊乱疗效观察.浙江中西医结合杂志,2024,34:348-351.
8 Richards JS,Ren YA,Candelaria N,et al.Ovarian follicular theca cell recruitment,differentiation,and impact on fertility:2017 update.Endocr Rev,2018,39:1-20.
9 Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group.Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome.Fertil Steril,2004,81:19-25.
10 Azziz R,Carmina E,Chen Z,et al.Polycystic ovary syndrome.Nat rev Dis Primers,2016,2:16057.
11 Simon SL,McWhirter L,Diniz Behn C,et al.Morning circadian misalignment is associated with insulin resistance in girls with obesity and polycystic ovarian syndrome.J Clin Endocrinol Metab,2019,104:3525-3534.
12 Zheng X,Zhang K,Zhao Y,et al.Environmental chemicals affect circadian rhythms:An underexplored effect influencing health and fitness in animals and humans.Environ Int,2021,149:106159.
13 Zisapel N.New perspectives on the role of melatonin in human sleep,circadian rhythms and their regulation.Br J Pharmacol,2018,175:3190-3199.
14 Barron ML.Light exposure,melatonin secretion,and menstrual cycle parameters:an integrative review.Biol Res Nurs,2007,9:49-69.
15 Basheer M,Rai S,Ghosh H,et al.Therapeutic efficacy of melatonin against polycystic ovary syndrome(PCOS) induced by letrozole in Wistar rat.Pak J Biol Sci,2018,21:340-347.
16 刘梨会,姜大庆.基于"阴平阳秘"和"稳态"理论探讨中西医防治乳腺癌.中国民族民间医药,2024,33:1-6.
17 李瑾瑜,丘余良.从阴平阳秘浅谈免疫平衡.光明中医,2023,38:2837-2841.
18 Wu L,Zhang H,Fan M,et al.Efficacy and safety of Cangfu Daotan decoction in patients with polycystic ovary syndrome:a systematic review and meta-analysis.Evid Based Complement Alternat Med,2022,2022:4395612.
19 李珍,乔鹏艳,康丽荣.奥利司他联合达英-35治疗肥胖型多囊卵巢综合征疗效及对患者血清性激素水平的影响.陕西医学杂志,2024,53:247-251.
20 马丽亚,杜婧雯,张童,等.金匮肾气丸对多囊卵巢综合征模型大鼠的改善作用及机制研究.中国药房,2022,33:2869-2873.
21 Zhang C,Ma J,Wang W,et al.Lysyl oxidase blockade ameliorates anovulation in polycystic ovary syndrome.Hum Reprod,2018,33:2096-2106.
22 Zhang L,Liu Y,Li M,et al.Effect of a high-calorie diet and constant light exposure on female reproduction,metabolism and immune inflammation:A comparative study of different mouse models.Am J Reprod Immunol,2021,86:e13479.
23 Chu W,Zhai J,Xu J,et al.Continuous light-induced PCOS-like changes in reproduction,metabolism,and gut microbiota in Sprague-Dawley rats.Front Microbiol,2019,10:3145.
24 Li Y,Cheng S,Li L,et al.Light-exposure at night impairs mouse ovary development via cell apoptosis and DNA damage.Biosci Rep,2019,39:BSR20181464.
25 Nallasamy S,Kaya Okur HS,Bhurke A,et al.Msx homeobox genes act downstream of BMP2 to regulate endometrial decidualization in mice and in humans.Endocrinology,2019,160:1631-1644.
26 Chang HM,Bai L,Zhu YM,et al.Connective tissue growth factor mediates bone morphogenetic protein 2-induced increase in hyaluronan production in luteinized human granulosa cells.Reprod Biol Endocrinol,2022,20:65.
27 Zhang XY,Chang HM,Yi Y,et al.BMP6 increases CD68 expression by up-regulating CTGF expression in human granulosa-lutein cells.Mol Cell Endocrinol,2021,536:111414.
28 Szilágyi SS,Amsalem-Zafran AR,Shapira KE,et al.Competition between type I activin and BMP receptors for binding to ACVR2A regulates signaling to distinct Smad pathways.BMC Biol,2022,20:50.
29 Liu Y,Chen M,Zhao X,et al.Bone morphogenetic protein 6 expression in cumulus cells is negatively associated with oocyte maturation.Hum Fertil(Camb),2021,24:290-297.
30 Khalaf M,Morera J,Bourret A,et al.BMP system expression in GCs from polycystic ovary syndrome women and the in vitro effects of BMP4,BMP6,and BMP7 on GC steroidogenesis.Eur J Endocrinol,2013,168:437-444.
31 Abdurahman A,Du X,Yao Y,et al.Smad4 feedback enhances BMPR1B transcription in ovine granulosa cells.Int J Mol Sci,2019,20:2732.
32 Xin X,Chang HM,Leung P,et al.Bone morphogenetic protein 6 induces downregulation of pentraxin 3 expression in human granulosa lutein cells in women with polycystic ovary syndrome.J Assist Reprod Genet,2024,41:31-48.