妊娠期糖尿病(gestational diabetes mellitus,GDM)指妊娠期首次发生或发现的不同程度的糖耐量异常[1]。GDM可以导致不良妊娠结局,威胁母胎安全,包括早产、流产、死产等,还可以导致泌尿生殖系统感染、酮症酸中毒、妊娠高血压等并发症的产生,甚至对胎儿也产生一定的不良影响,增加了胎儿畸形、新生儿代谢异常的风险,是产后发生2型糖尿病和心血管疾病的危险因素[2-3]。因此发现GDM患者产后糖代谢异常危险因素,及时进行干预,对预后改善至关重要。T细胞免疫球蛋白及粘蛋白结构域分子3(T cell immunoglobulin and mucin domain 3,TIM-3)是一种在T细胞上表达的免疫调节分子,属于免疫检查点家族[4]。TIM-3主要在活化的T细胞、树突状细胞和某些类型的肿瘤细胞上表达,具有免疫球蛋白样结构和粘蛋白样结构,参与细胞间的相互作用[5]。TIM-3作为免疫检查点,调节T细胞的活性和功能,抑制过度的免疫反应,防止自身免疫病的发生[6]。可溶性TIM-3来源于TIM-3的剪接或分解,可能通过细胞外酶的作用释放到血液中[7]。相关研究表明,在肿瘤微环境中,可溶性TIM-3的水平升高,抑制T细胞的抗肿瘤活性,导致肿瘤细胞的免疫逃逸[8]。高水平的可溶性TIM-3可能与结核性脑膜炎病情严重程度关系密切相关[9]。而且国外研究表明,可溶性TIM-3与腰高比和体重指数呈正相关[10],但目前尚未发现可溶性 TIM-3与GDM 产后糖代谢异常的相关研究报道,因此本研究探讨可溶性TIM-3与GDM及其产后糖代谢异常的相关性,为临床寻找预防和阻断 GDM 产后糖代谢异常提供新的思路和策略。
对象与方法
1.研究对象:取2023年8月—2024年12月入本院治疗的妊娠期糖尿病患者159例,所有患者均于产后6周进行门诊复查,采用口服葡萄糖耐量试验(oral glucose tolerance test,OGTT)评估糖代谢状态,空腹血糖< 5.1 mmol/L,1 h血糖<10.5 mmol/L,2 h血糖< 8.5 mmol/L为糖代谢正常孕妇;空腹血糖≥ 5.1 mmol/L,1 h血糖≥ 10.5 mmol/L,2 h血糖≥ 8.5 mmol/L为糖代谢异常孕妇。依据糖代谢情况进行分组,分为糖代谢正常组(n=128)和糖代谢异常组(n=31)。纳入标准:(1)符合妊娠期糖尿病的诊断标准[11];(2)年龄18~45岁;(3)单胎妊娠;(4)孕妇知情同意,并签订知情同意书。排除标准:(1)合并精神疾病患者;(2)多胎妊娠和合并感染者;(3)妊娠前有代谢综合征、甲状腺疾病、心血管疾病、多囊卵巢综合征及血液疾病者;(4)肝肾功能严重异常者;(5)合并结核、传染性疾病者。本研究通过本单位医学伦理委员会审核,批号:20230507。
2.方法:(1)临床资料收集。收集孕妇的临床资料,包括孕妇的年龄、孕前体质指数(BMI)、孕次、糖尿病家族史、产次、产检次数、收缩压、舒张压、使用胰岛素治疗等。(2)孕妇生化指标检测。所有受试者在孕24~28周禁食8 h抽取肘静脉血6 mL,采用日立7600系列全自动生化分析仪检测甘油三酯(triglyceride,TG)、高密度脂蛋白(high-density lipoprotein,HDL)、γ-谷氨酰转肽酶(gamma-glutamyl transpeptidase,GGT)、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、碱性磷酸酶(alkaline phosphatase,ALP)、白蛋白(albumin,ALB)、胆固醇(cholesterol,CHOL)水平,贝克曼库尔特AU-5800全自动生化分析仪测定中性粒细胞(neutrophilicgranulocyte,Neu)、低密度脂蛋白(low density lipoprotein,LDL)、淋巴细胞(lymphocyte,LYM)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)、血红蛋白(hemoglobin,Hb)水平;采用日立 7600 P 模块上检测葡萄糖(glucose,GLU)(包括0 h、1 h、2 h)水平。(3)孕妇血清中可溶性TIM-3水平检测。在诊断GDM时,取肘静脉血 3 mL,注入干燥试管,4 ℃离心3500 rpm×10 min,分离血清,采用酶联免疫吸附试验(ELISA)检测血清可溶性TIM-3水平。TIM-3 ELISA试剂盒购自于上海生工生物工程有限公司。
3.统计学方法:采用SPSS 22.0软件进行数据处理,计数成比或率(%)表示,比较用χ2检验;符合正态分布采用![]() 表示,组间采用t检验,Logistic 回归分析GDM孕妇产后危险因素,ROC曲线分析可溶性TIM-3预测GDM患者产后糖代谢异常的价值,P<0.05 为差异有统计学意义。
表示,组间采用t检验,Logistic 回归分析GDM孕妇产后危险因素,ROC曲线分析可溶性TIM-3预测GDM患者产后糖代谢异常的价值,P<0.05 为差异有统计学意义。
结果
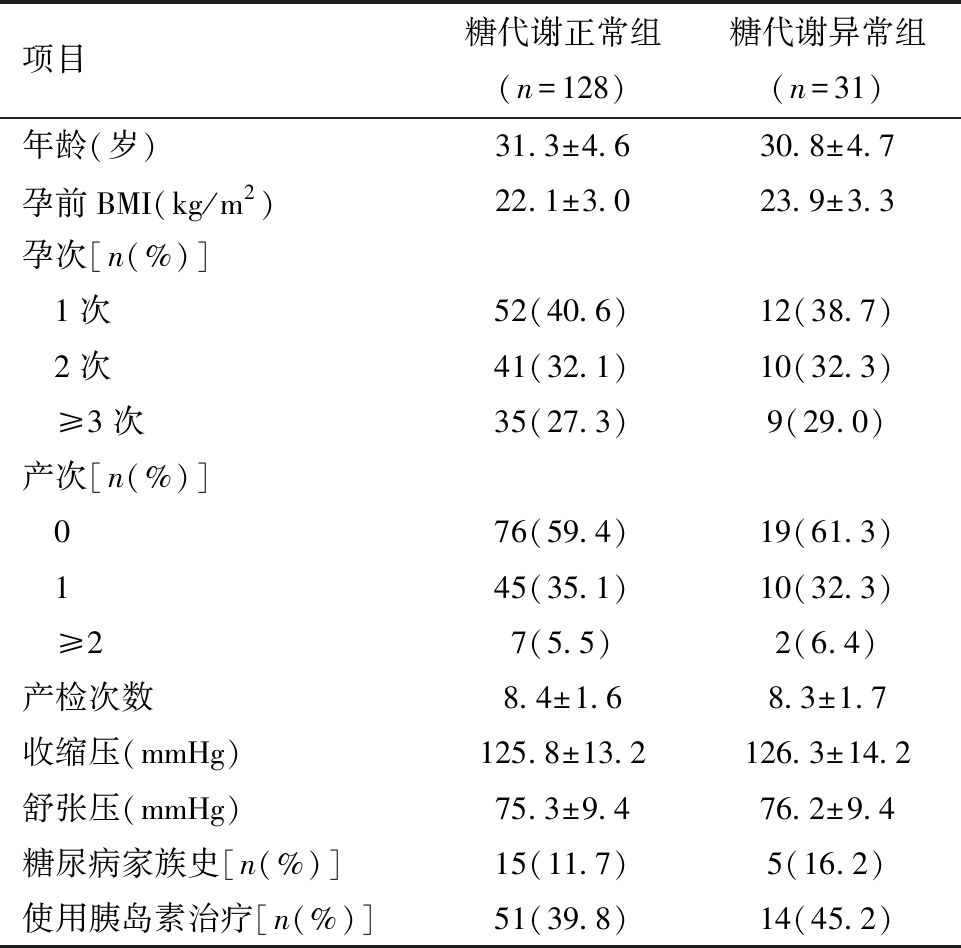
1.两组孕妇资料比较:两组孕妇的年龄、孕次、产次、产检次数、收缩压、舒张压、糖尿病家族史、使用胰岛素治疗对比无差异(P>0.05),糖代谢异常组孕前BMI高于糖代谢正常组(P<0.05)。见表1。
表1 2组孕妇的基线资料比较![]()
项目糖代谢正常组(n=128)糖代谢异常组(n=31)年龄(岁)31.3±4.630.8±4.7孕前BMI(kg/m2)22.1±3.023.9±3.3孕次[n(%)] 1次52(40.6)12(38.7) 2次41(32.1)10(32.3) ≥3次35(27.3)9(29.0)产次[n(%)] 076(59.4)19(61.3) 145(35.1)10(32.3) ≥27(5.5)2(6.4)产检次数8.4±1.68.3±1.7收缩压(mmHg)125.8±13.2126.3±14.2舒张压(mmHg)75.3±9.476.2±9.4糖尿病家族史[n(%)]15(11.7)5(16.2)使用胰岛素治疗[n(%)]51(39.8)14(45.2)
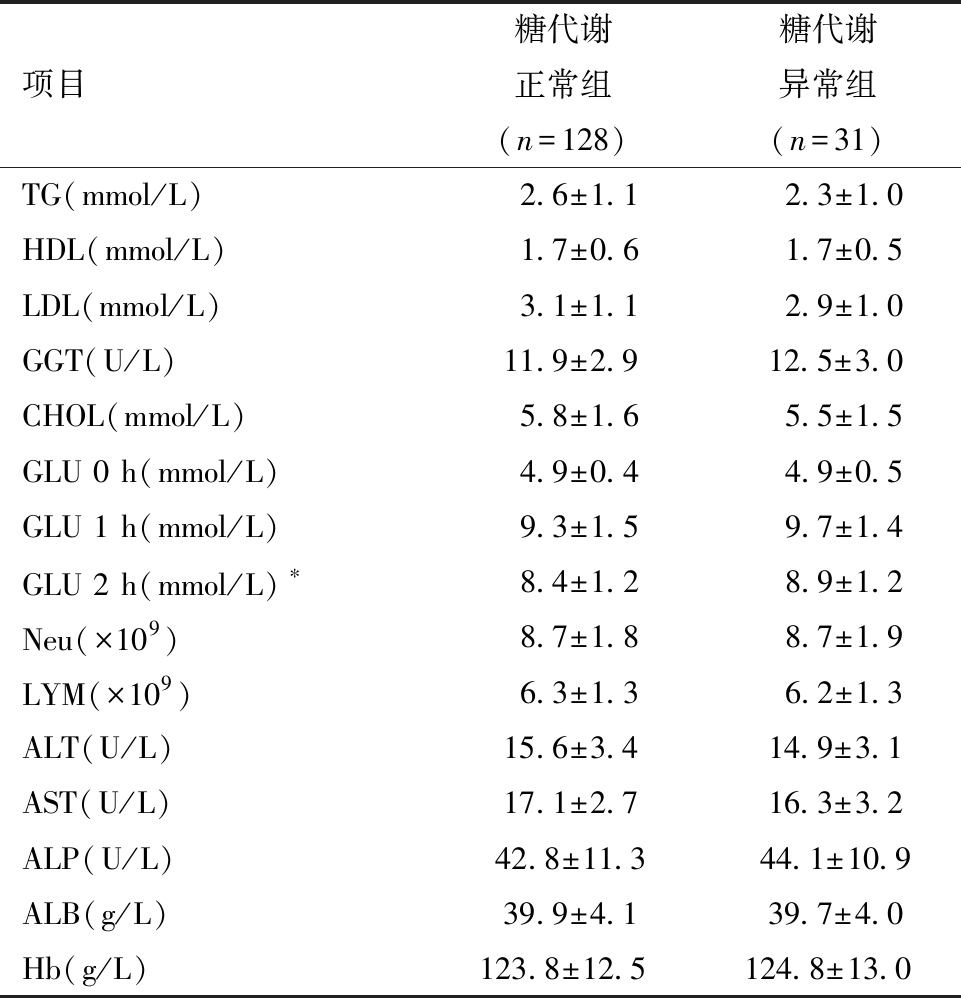
2.两组孕妇生化指标比较:糖代谢异常组的GLU 2 h高于糖代谢正常组(P<0.05),而两组孕妇的TG、HDL、LDL、GGT、CHOL、GLU 0 h、GLU 1 h、Neu、LYM、ALT、AST、ALP、ALB、Hb对比无差异(P>0.05)。见表2。
表2 两组孕妇生化指标比较分析![]()
*P<0.05
项目糖代谢正常组(n=128)糖代谢异常组(n=31)TG(mmol/L) 2.6±1.1 2.3±1.0HDL(mmol/L) 1.7±0.6 1.7±0.5LDL(mmol/L) 3.1±1.1 2.9±1.0GGT(U/L)11.9±2.912.5±3.0CHOL(mmol/L) 5.8±1.6 5.5±1.5GLU 0 h(mmol/L) 4.9±0.4 4.9±0.5GLU 1 h(mmol/L) 9.3±1.5 9.7±1.4GLU 2 h(mmol/L)∗ 8.4±1.2 8.9±1.2Neu(×109) 8.7±1.8 8.7±1.9LYM(×109) 6.3±1.3 6.2±1.3ALT(U/L)15.6±3.414.9±3.1AST(U/L)17.1±2.716.3±3.2ALP(U/L)42.8±11.344.1±10.9ALB(g/L)39.9±4.139.7±4.0Hb(g/L)123.8±12.5124.8±13.0
3.两组孕妇血清中可溶性TIM-3水平比较:糖代谢正常组患者血清中可溶性TIM-3水平为(110.7±21.7)pg/mL,糖代谢异常组患者血清中可溶性TIM-3水平为(326.8±84.8)pg/mL,糖代谢异常组患者血清中可溶性TIM-3水平明显高于糖代谢正常组,差异具有统计学意义(P<0.001)。见图1。
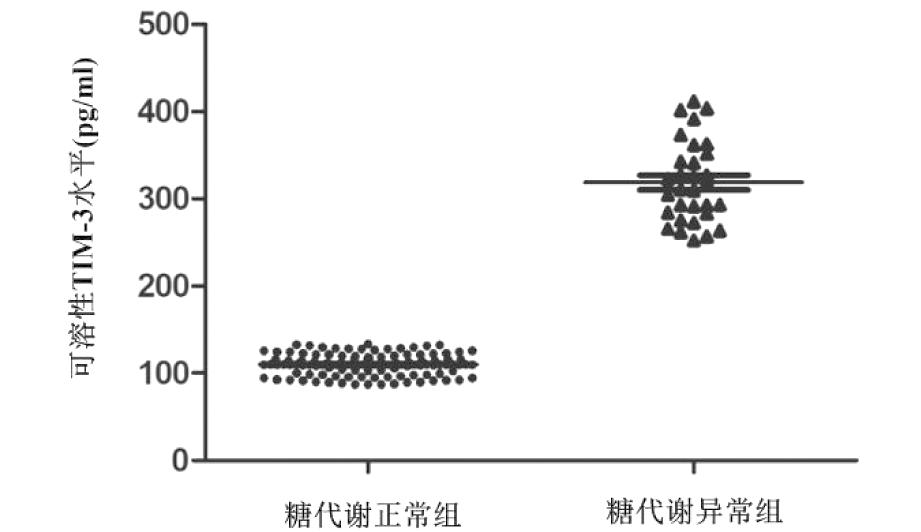
图1 两组患者血清中可溶性TIM-3水平对比
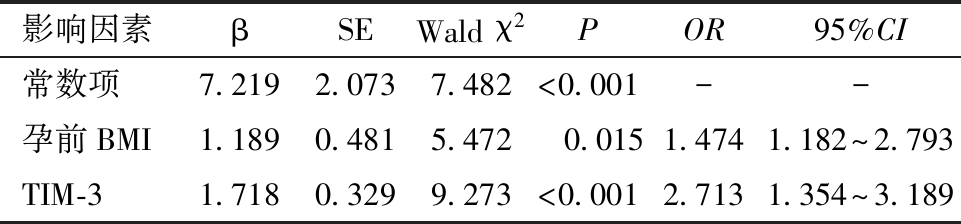
4.GDM孕妇产后糖代谢异常的危险因素:以GDM孕妇产后糖代谢异常为因变量(赋值:否=0,是=1),以孕前BMI(赋值:实际值输入)、GLU 2 h(赋值:实际值输入)和TIM-3(赋值:实际值输入)为自变量,多因素Logistics回归分析结果显示,孕前BMI和TIM-3均是GDM孕妇发生糖代谢异常的危险因素(P<0.001)。见表3。
表3 娠期糖尿病孕妇产后糖代谢异常影响因素的Logistics回归分析
影响因素βSEWald χ2POR95%CI常数项7.2192.0737.482<0.001--孕前BMI1.1890.4815.472 0.0151.4741.182~2.793TIM-31.7180.3299.273<0.0012.7131.354~3.189
5.可溶性TIM-3预测妊娠期糖尿病患者产后糖代谢异常的价值:ROC曲线分析结果显示,可溶性TIM-3对产后糖代谢异常具有较高的预测价值,AUC值为0.877,当临界值为202.7 pg/mL时,其灵敏度为83.9% ,特异度为77.3% 。见图2。
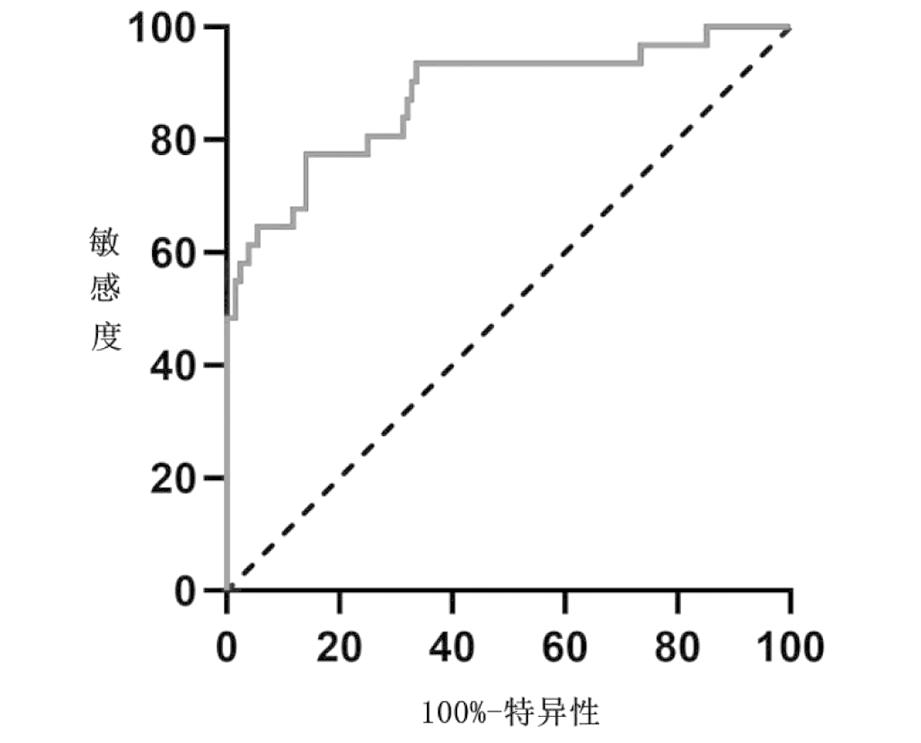
图2 血清中可溶性TIM-3预测GDM产后糖代谢异常的 ROC 曲线
讨论
妊娠期体内的糖代谢会发生一系列改变,尤其是空腹葡萄糖水平降低[12]。胎儿宫内生长发育所需的能量会导致空腹葡萄糖水平的降低;另外孕激素与雌激素增加了母体对葡萄糖的利用,也会导致空腹葡萄糖水平的降低[13];此外,孕期肾血流量及肾小球滤过率明显增加,肾糖阈降低,致使葡萄糖的排泄增加,导致孕妇的空腹葡萄糖水平降低[14]。GDM是一种严重的妊娠并发症,中国GDM患病率为14.8%~17.8%,且呈逐年上升趋势[15],成为重要公共卫生问题之一。妊娠期糖尿病的发生与多种因素相关,包括遗传易感性、体质指数、年龄、种族及孕期生活方式等。研究表明,GDM不仅会对母体的健康造成影响,如增加产后发展为2型糖尿病的风险,还可能导致胎儿的多种不良结局,包括巨大儿、早产、以及胎儿生长受限等[16]。因此,对GDM患者产后的糖代谢异常风险进行分层,从而提升对糖代谢异常的识别效率。
可溶性TIM-3是近年来生物医学研究中逐渐受到关注的免疫调节因子[17]。TIM-3作为一种免疫检查点分子,广泛表达于多种免疫细胞上,尤其是在T细胞中,其主要功能是通过与其配体结合,调节免疫反应,促进免疫耐受[18],已被证明与多种病理状态相关,如自身免疫性疾病、感染及肿瘤等。可溶性TIM-3的生成与TIM-3的剪切作用有关,它可以与TIM-3的配体结合,从而影响免疫应答的调节[19]。此外,可溶性TIM-3被认为能够通过调节炎症反应、影响细胞凋亡等途径参与疾病的发展。研究表明,可溶性TIM-3在慢性HIV感染中与T细胞的功能失调相关,提示其可能影响疾病的进程和患者的免疫状态[20]。此外,在急性胰腺炎患者中,可溶性TIM-3的表达也与疾病的严重程度有关,进一步强调了其在免疫调节中的潜在作用[21]。目前,关于妊娠糖尿病的研究主要集中在其病因、诊断标准和治疗方法等方面。近年来,越来越多的研究关注免疫检查点在GDM中的作用,可溶性TIM-3是一种重要的免疫调节因子,其在多种免疫相关疾病中表现出异常表达,可能与机体的免疫耐受和代谢状态密切相关。研究表明,TIM-3可能与代谢状态相关,影响胰岛素敏感性,GDM患者的TIM-3表达可能与炎症水平、胰岛素抵抗及妊娠结局相关[22]。本研究结果显示,糖代谢异常组孕期血清中可溶性TIM-3水平均明显高于糖代谢正常组,TIM-3是GDM孕妇发生产后糖代谢异常的危险因素,而且可溶性TIM-3对产后糖代谢异常具有较高的预测价值,说明孕期可溶性TIM-3水平升高可能提示产后糖代谢紊乱的风险,对临床预防产后糖代谢异常具有积极意义,以期揭示可溶性TIM-3在产后糖代谢异常中的生物学意义及其作为潜在生物标志物的可能性。可溶性TIM-3参与GDM产后糖代谢异常的机制尚不清楚,可能原因是可溶性TIM-3高表达可以促进炎症因子的分泌,导致Th1/Th2、Treg/Th17 细胞失衡,从而诱导或加重胰岛β细胞损伤,参与糖尿病的发生发展[23]。另有研究报道,可溶性TIM-3与代谢性炎症标志物白细胞介素-6、C反应蛋白和瘦素之间存在显著相关性,而且可溶性TIM-3的水平显著升高,可能与胰岛素抵抗和炎症反应有关[24]。本研究通过检测GDM孕妇孕期血清中可溶性TIM-3的水平可以更好地识别产后糖代谢异常的GDM患者,进而采取更为个性化的干预措施,降低母婴并发症的风险。此外,可溶性TIM-3的水平也可能为监测GDM孕妇糖代谢异常的治疗反应提供新的指标,帮助制定更合理的治疗方案,提升患者的预后。
综上所述,GDM患者产后糖代谢异常孕妇孕期可溶性TIM-3水平升高,高水平的可溶性TIM-3是产后糖代谢异的危险因素,对产后糖代谢异常具有较高的预测价值,值得临床推广和应用。但本研究仍存在一定的不足,首先,样本量相对较小,且主要集中在单一医疗中心进行,可能影响结果的普适性。未来的研究需要扩大样本量,并在多中心进行,以验证可溶性TIM-3的临床应用价值,并探讨其在GDM的病理生理机制中的具体作用,这将为GDM的早期诊断和干预策略提供更为坚实的理论基础。
1 舒心宇,隽娟,杨慧霞.妊娠期糖尿病:诊断进展及存在争议.中华围产医学杂志,2025,28:12-16.
2 de Oliveira Araújo ME,de Lucena AML,Fontes IL,et al.Nutritional strategies prescribed during pregnancy and weight gain in women with gestational diabetes mellitus:a systematic review of observational studies.Nutrients,2024,17.
3 Randall D,Ibiebele I,Nippita T,et al.StUdy of gestational diabetes and risk using electronic data(SUGARED):a population-based cohort study-study protocol.BMJ Open,2024,14:e087248.
4 赵彤,郭海平,郑勤.TIM-3表达对肝癌细胞的作用及其机制研究.肝脏,2024,29:671-675,718.
5 Zhang J,Wang L,Guo H,et al.The role of Tim-3 blockade in the tumor immune microenvironment beyond T cells.Pharmacol Res,2024,209:107458.
6 Ariolli A,Agolini E,Mazza T,et al.The putative role of TIM-3 variants in polyendocrine autoimmunity:insights from a WES investigation.Int J Mol Sci,2024,25:10994.
7 Zhao D,Li C,Yang X,et al.Elevated soluble Tim-3 correlates with disease activity of systemic lupus erythematosus.Autoimmunity,2021,54:97-103.
8 汪可,刘丽娟,崔现平,等.可溶性T细胞免疫球蛋白黏蛋白结构域在胰腺癌患者外周血中的表达及与血清糖链抗原19-9的联合诊断价值.中华内分泌外科杂志,2023,17:278-281.
9 孙霞,王丽,李庭毅.可溶性Tim-3及Galectin-9在结核性脑膜炎患者脑脊液中的表达及意义.国际检验医学杂志,2020,41:2721-2724,2731.
10 Lin M,Huang J,Huang J,et al.Level of serum soluble Tim-3 expression in early-phase acute pancreatitis.Turk J Gastroenterol,2019,30:188-191.
11 张溪竹,湛浩然,孙若宁,等.妊娠期糖尿病诊断标准的研究进展及发展趋势.中国糖尿病杂志,2023,31:555-560.
12 韦肖慧,傅桂芬,黄小知,等.妊娠期糖尿病患者产后糖代谢异常的孕期预测因子的研究进展.中国计划生育和妇产科,2022,14:35-38.
13 林晶,陈蕾,沈梦尘,等.妊娠期糖尿病孕前体质量指数对糖代谢及妊娠结局的影响.实用妇产科杂志,2021,37:466-470.
14 郑凯,袁晶.脂肪因子与妊娠期糖尿病及糖脂代谢.国际生殖健康/计划生育杂志,2021,40:431-435.
15 王爱爱,刘彩琴,张力,等.妊娠期糖尿病患者血清Lp-PLA2、SDF-1α、FGF-21水平变化及与产后糖代谢异常的关系.中国计划生育学杂志,2020,28:1396-1401.
16 王欢,钱秋萍,赵绍杰,等.妊娠期糖尿病孕妇产后2年糖代谢转归失败风险因素分析.中国计划生育学杂志,2021,29:2326-2331.
17 Yan L,Yang Y,Li YM,et al.Soluble Tim-3/Gal-9 as predictors of adverse outcomes after kidney transplantation:A cohort study.Clin Biochem,2022,102:19-25.
18 李强,陈明,黄飚,等.重组人可溶性TIM-3稳转细胞株的构建及其分泌蛋白的表达.中国细胞生物学学报,2020,42:1194-1200.
19 Yan L,Yang Y,Li YM,et al.Soluble Tim-3/Gal-9 as predictors of adverse outcomes after kidney transplantation:A cohort study.Clin Biochem,2022,102:19-25.
20 Hu Y,Hu P,Peng X.TIM-3 blockade:immune and targeted therapy in DIPG.Trends Mol Med,2024,30:110-112.
21 陈曙蓓,林影,叶勇.急性胰腺炎患者血清可溶性Tim-3、炎症因子及RAAS分子检测的临床意义.中国现代医学杂志,2020,30:81-85.
22 Grannes H,Sharma A,Suntharalingam A,et al.Plasma soluble TIM-3 is increased in normoglycemic South Asian women compared to Nordic women after gestational diabetes mellitus and associated with markers of metaflammation.Heliyon,2024,10:e40339.
23 Bailly C,Thuru X,Goossens L,et al.Soluble TIM-3 as a biomarker of progression and therapeutic response in cancers and other of human diseases.Biochem Pharmacol,2023,209:115445.
24 Huang S,Liu D,Sun J,et al.Tim-3 regulates sepsis-induced immunosuppression by inhibiting the NF-κB signaling pathway in CD4 T cells.Mol Ther.2022,30:1227-1238.