妊娠期糖尿病(gestational diabetes mellitus,GDM)是妊娠期最常见的并发症之一。中国患病率为14.8%[1],随着饮食、生活习惯的改变,以及“三胎政策”的开放,高龄产妇数量明显增加,GDM的发病率上升。大量的研究已经证明GDM是不良妊娠结局发生的危险因素[2-4]。从长远来看,GDM 孕妇及子女未来患糖尿病、肥胖和心血管疾病的风险也明显增高[5-6]。因此,研究GDM的发病机制,早期识别和预防其发生发展,为临床诊治GDM寻找新方法有重要的意义和价值。
研究发现补体Clq/肿瘤坏死因子相关蛋白与脂联素具有高度同源性,其多个成员在糖脂代谢、胰岛素抵抗、氧化应激、调节炎症等方面发挥不同的病理生理作用[7]。补体C1q/肿瘤坏死因子相关蛋白7(C1q/tumor necrosis factor-related protein7,CTRP7)是CTRP家族成员之一,在全身广泛表达。Holmes[8]等人首次发现肥胖人群血清以及肝脏CTRP7的表达水平明显高于对照组,其中空腹血糖>5.6 mmol/L的人群血清CTRP7水平高于空腹血糖<5.6 mmol/L者。另外,研究[8]中还发现CTRP7基因缺失小鼠在高脂饮食后,表现出明显的胰岛素抵抗减轻和葡萄糖耐量增强。Hu[9]等人研究发现代谢综合征和胰岛素抵抗人群血清CTRP7水平明显升高,并且血清CTRP7与葡萄糖和脂质代谢相关的基因和信号通路相关。Li[10]等人研究发现糖耐量减退(impaired glucose tolerance,IGT)和2型糖尿病人群血清CTRP7水平明显升高,血清CTRP7是2型糖尿病的独立危险因素。但是到目前为止,尚未见CTRP7与GDM的相关研究报道。基于此,本研究通过检测GDM孕妇与糖耐量正常(normal glucose tolerance,NGT)孕妇血清CTRP7、血糖、血脂、空腹胰岛素、新生儿体重水平,研究血清CTRP7与GDM、胰岛素抵抗、新生儿体重之间的关系。
对象与方法
1.研究对象:选取2022年6月—2023年6月期间至郑州大学第二附属医院住院分娩的80例妊娠期糖尿病患者例纳入GDM组,另外选取同期于本院规律产检并分娩的糖耐量正常孕妇80例纳入NGT组;GDM诊断标准参考《妊娠合并糖尿病诊治指南(2014)》[11]:(1)空腹血糖≥5.1 mmol/L;(2)口服75 g葡萄糖耐量实验(75 g oral glucose tolerance test,75 g OGTT)后1 h血糖≥10.0 mmol/L;(3)75 g OGTT后2h血糖≥8.5 mmol/L;于妊娠24~28周行口服葡萄糖耐量实验,结果任何一项达到或超过以上标准即可明确诊断为GDM。
2.纳入标准:(1)初产妇,自然单胎妊娠;(2)无妊娠前糖尿病史、糖尿病家族史、既往不良妊娠史;(3)无心血管疾病、肝肾功能障碍等重要脏器功能损伤;(4)无妊娠期高血压、甲状腺疾病、多囊卵巢综合征等妊娠合并症。
3.排除标准:(1)临床资料收集不全、孕前资料不详;(2)精神状态差,不能正常沟通交流;(3)服用影响糖脂代谢的药物(如降压药、激素、抗生素等);(4)孕期有烟酒嗜好史。
4.一般资料收集:在研究对象首次入院检查时收集其年龄、孕周、身高、孕前及产前的体质量,于胎儿分娩后记录新生儿出生体重,计算孕前及产前的体质量指数(Body mess index,BMI),BMI=体质量(kg)/身高2(m2)。
5.生化和实验室指标收集:所有研究对象于分娩前清晨空腹(禁食8 h后)采集肘静脉血进行相关检测,由检验科全自动生化分析仪检测血清空腹血糖(fasting plasma glucose,FPG)、餐后2 h血糖(2-hour postprandial blood glucose,2 h PG)、糖化血红蛋白(glycated hemoglobin,HbA1c)、总胆固醇(total cholesterol,TC)、甘油三酯(Triglyceride,TG)、低密度脂蛋白胆固醇(low density lipoprotein-cholesterol,LDL-C)、高密度脂蛋白胆固醇(high density lipoprotein-cholesterol,HDL-C)、空腹胰岛素(fasting insulin,FINS)水平,计算胰岛素抵抗指数(homeostasis model assessment of insulin resistance,HOMA-IR)=FPG×FINS/22.5;血清CTRP7水平通过酶联免疫吸附双抗体夹心法检测。试剂盒来自上海仁捷生物科技有限公司,实验步骤严格遵守试剂盒说明书。
6.统计学方法:采用SPSS 25.0软件进行统计分析。对于计量资料采用![]() 表示,使用t检验;采用Pearson相关性分析对CTRP7与各变量之间的相关性进行分析,CTRP7与其他变量的线性关系采用多元逐步回归(进入和剔除模型的标准分别是≤0.05和≥0.1)分析;通过二元Logistic回归模型分析CTRP7对GDM和胰岛素抵抗的影响。以P<0.05为差异有统计学意义。
表示,使用t检验;采用Pearson相关性分析对CTRP7与各变量之间的相关性进行分析,CTRP7与其他变量的线性关系采用多元逐步回归(进入和剔除模型的标准分别是≤0.05和≥0.1)分析;通过二元Logistic回归模型分析CTRP7对GDM和胰岛素抵抗的影响。以P<0.05为差异有统计学意义。
结果
1.两组的一般资料及实验室指标比较:
(1)两组孕妇年龄和孕周的差异无统计学意义(P值均>0.05),见表1。
表1 两组孕妇一般资料和实验室指标比较![]()
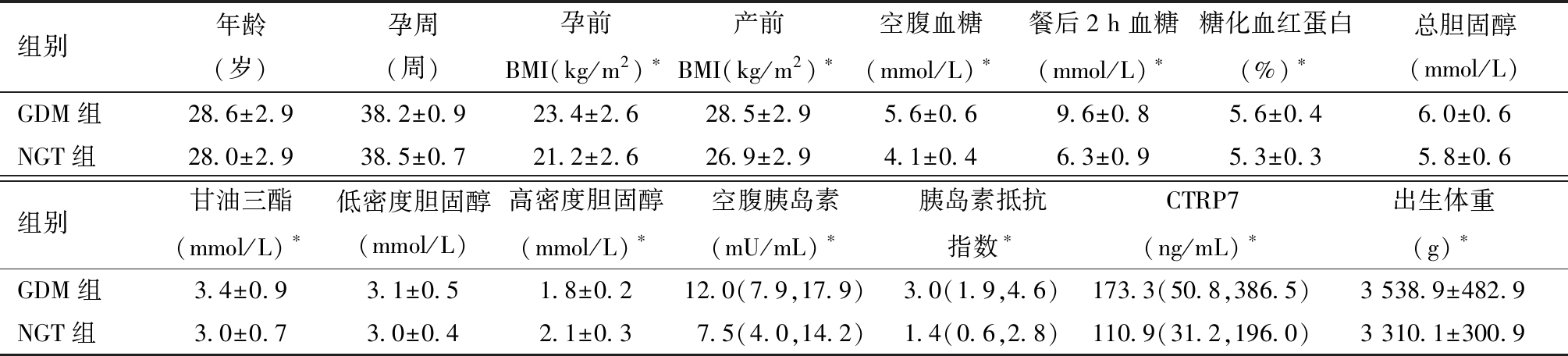
注:两组比较,*P<0.05。
组别年龄(岁)孕周(周)孕前BMI(kg/m2)∗产前BMI(kg/m2)∗空腹血糖(mmol/L)∗餐后2 h血糖(mmol/L)∗糖化血红蛋白(%)∗总胆固醇(mmol/L)GDM组28.6±2.938.2±0.923.4±2.628.5±2.95.6±0.69.6±0.85.6±0.46.0±0.6NGT组28.0±2.938.5±0.721.2±2.626.9±2.94.1±0.46.3±0.95.3±0.35.8±0.6组别甘油三酯(mmol/L)∗低密度胆固醇(mmol/L)高密度胆固醇(mmol/L)∗空腹胰岛素(mU/mL)∗胰岛素抵抗指数∗CTRP7(ng/mL)∗出生体重(g)∗GDM组3.4±0.93.1±0.51.8±0.212.0(7.9,17.9)3.0(1.9,4.6)173.3(50.8,386.5)3 538.9±482.9NGT组3.0±0.73.0±0.42.1±0.37.5(4.0,14.2)1.4(0.6,2.8)110.9(31.2,196.0)3 310.1±300.9
(2)GDM组孕妇的孕前BMI、产前BMI、FPG、2hPG、HbA1c、FINS、HOMA-IR、TG、新生儿出生体重、CTRP7均高于 NGT 组,HDL-C水平低于NGT组,差异均有统计学意义( P值均<0.05),见表1。
2.GDM患者CTRP7水平与机体各参数指标以及新生儿体重的相关性分析:
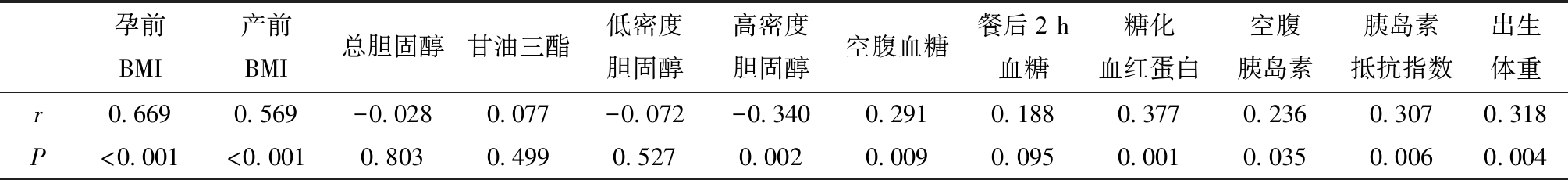
(1)GDM孕妇血清 CTRP7浓度与孕前BMI、产前BMI、FPG、HbA1c、FINS、HOMA-IR 呈正相关,与HDL-C呈负相关,(P值均< 0.05),见表2。
表2 GDM患者CTRP7水平与机体各参数指标的相关性分析
孕前BMI产前BMI总胆固醇甘油三酯低密度胆固醇高密度胆固醇空腹血糖餐后2 h血糖糖化血红蛋白空腹胰岛素胰岛素抵抗指数出生体重r0.6690.569-0.0280.077-0.072-0.3400.2910.1880.3770.2360.3070.318P<0.001<0.0010.8030.4990.5270.0020.0090.0950.0010.0350.0060.004
(2)GDM孕妇血清CTRP7浓度与新生儿体重呈正相关( P<0.05),见表2。
3.多重线性逐步回归分析GDM血清中CTRP7水平与临床指标之间的关系:以GDM患者血清CTRP7浓度为因变量,孕前BMI、产前BMI以及产前的FPG、HbA1c、FINS、HOMA-IR、HDL-C为自变量,进行多元逐步回归分析,结果提示孕前BMI、HOMA-IR、HDL-C为GDM患者血清CTRP7水平的影响因素,见表3。
表3 GDM患者血清CTRP7水平的影响因素分析

自变量βP孕前BMI(kg/m2)0.531<0.001胰岛素抵抗指数0.2330.009高密度脂蛋白胆固醇(mmol/L)-0.1830.034
4.二元Logistic回归分析血清CTRP7水平对胰岛素抵抗及GDM的影响:分别以HOMA-IR(HOMA-IR≥2.23为胰岛素抵抗[12])、GDM为因变量进行二元Logistic回归分析,校正孕前BMI、产前BMI、TG、HDL-C后,血清CTRP7水平仍与胰岛素抵抗及GDM相关(OR值分别为1.01和1.01,95%CI分别为1.01~1.02和1.00~1.01。
讨论
既往研究发现,GDM的发生与多种原因导致的胰岛素抵抗、血脂代谢异常、炎症反应密切相关[13-14]。正常妊娠过程中,为了满足胎儿的快速生长发育所需的以葡萄糖为主要形式的能量,母体一方面会通过减少对葡萄糖的利用,使机体处于轻度的生理性胰岛素抵抗状态;另一方面随着孕周的增加,胎盘的大小和功能逐渐成熟,胎盘会分泌人胎盘催乳素、人胎盘生长激素、雌激素、孕激素等大量拮抗胰岛素的激素,从而使母体对胰岛素的敏感性下降,以孕晚期最明显,进一步加重胰岛素抵抗。正常情况下,大部分母体会通过胰岛β细胞的肥大和增生来代偿性增加胰岛素的分泌,维持血糖始终在正常范围内;只有小部分孕妇体内胰岛素的分泌不足以代偿胰岛素抵抗的程度,最终导致妊娠期糖尿病的发生[15-16]。Wang[17]等人研究发现GDM患者HOMA-IR曲线呈上升趋势,混合胰岛素敏感度曲线呈下降趋势,表明GDM患者的胰岛素抵抗随着妊娠的进展而增强、胰岛素敏感性随着妊娠的进展而降低。与上述研究结果一致,本研究发现与正常孕妇相比,GDM患者孕晚期的FPG、2hPG、HbA1c、FINS、HOMA-IR均明显升高,表明孕晚期GDM患者血糖代谢紊乱,存在显著的病理性胰岛素抵抗。
CTRP7是CTRPs家族成员之一,与脂联素具有高度同源性,广泛表达于脂肪、子宫内膜、胆囊、肺等组织[8]。既往研究表明,GDM患者存在慢性低度炎症反应,炎症因子(例如TNF-α、IL-6、PTX-3、Cd11c等)可能通过多种途径影响糖尿病的发生和发展[18],Holmes[8]等人通过构建基因敲除小鼠模型发现,CTRP7缺失小鼠的脂肪组织抗炎细胞因子(CD206、IL-1R)表达明显增加,促炎细胞因子(CCR2和CCR7)的表达减少。Holmes[8]等人还发现CTRP7缺失导致脂肪组织促炎因子CD11c水平明显升高。促炎因子Cd11c是由M l型巨噬细胞分泌的,其表达增加可能会加剧脂肪组织中巨噬细胞的积聚和活化,加重脂肪组织炎症,增加胰岛素抵抗[19]。提示CTRP7可能通过调节多种炎症因子的分泌,参与机体葡萄糖代谢和胰岛素敏感性的调节。国内研究[10]发现肥胖、IGT、T2DM人群血清CTRP7水平均显著增高,且从IGT进展至T2DM呈逐渐升高,通过体内和体外实验证实CTRP7可能通过使糖异生和糖原分解相关基因mRNA表达增加、糖酵解和糖原合成相关基因mRNA表达下降以及胰岛素信号分子磷酸化水平显著降低,从而加重葡萄糖代谢紊乱和胰岛素抵抗;与上述结果一致,本研究结果显示,GDM患者血清CTRP7水平明显高于正常糖耐量患者,且与孕前BMI、产前BMI呈中等程度相关,与FPG、HbA1c、FINS、HOMA-IR 呈弱相关性。推测GDM血清CTRP7水平升高与妊娠期糖脂代谢异常、胰岛素抵抗相关,尤其是与孕前超重和肥胖密切相关。这可能与肥胖患者尤其是腹部脂肪增加,分泌大量瘦素、脂肪酸等脂肪因子,通过影响胰岛素受体和受体后信号转导,降低胰岛素的敏感性,促进胰岛素抵抗的发生、发展。多重线性回归分析提示孕前BMI、HOMA-IR、HDL-C为血清CTRP7水平的影响因素,说明妊娠妇女血清CTRP7水平主要受孕前BMI、胰岛素抵抗程度以及HDL-C水平的影响。血清CTRP7水平与胰岛素抵抗和GDM明显相关,提示血清CTRP7水平的升高可能与GDM有一定的相关性。
研究发现GDM患者母体血糖明显升高时,血糖可以通过胎盘屏障进入胎儿体内,刺激胎儿分泌胰岛素增加,使胎儿在宫内快速生长,从而增加巨大儿发生的可能性[20]。本研究发现GDM组的新生儿出生体重明显高于NGT组,相关性分析显示新生儿出生体重与GDM患者母体血清CTRP7水平呈正相关。提示GDM患者血清CTRP7与新生儿体重相关,但具体的作用机制仍需继续深入研究。
综上所述,GDM患者血清CTRP7水平明显高于正常孕妇,且与BMI、血糖、血脂、胰岛素抵抗密切相关,提示CTRP7可能参与GDM患者妊娠晚期的糖脂代谢紊乱,为妊娠期糖尿病的临床防治提供新思路。
1 Ye W,Luo C,Huang J,et al.Gestational diabetes mellitus and adverse pregnancy outcomes:systematic review and meta-analysis.BMJ,2022,377:e067946.
2 null,Metzger BE,Lowe LP,et al.Hyperglycemia and adverse pregnancy outcomes.N Engl J Med,2008,358:1991-2002.
3 Filardi T,Tavaglione F,Stasio MD,et al.Impact of risk factors for gestational diabetes(GDM) on pregnancy outcomes in women with GDM.J Endocrinol Invest,2018,41:671-676.
4 于成华,张硕.妊娠期糖尿病患者产后胰岛素抵抗及胰岛β细胞功能变化及其影响因素.中国生育健康杂志,2020,31:215-218.
5 Zeng J,Shen F,Zou Z,et al.Association of maternal obesity and gestational diabetes mellitus with overweight/obesity and fatty liver risk in offspring.World J Gastroenterol,2022,28:1681-1691.
6 Moon JH,Jang HC.Gestational diabetes mellitus:diagnostic approaches and maternal-offspring complications.Diabetes Metab J,2022,46:3-14.
7 Zhang H,Zhang-Sun Z,Xue C,et al.CTRP family in diseases associated with inflammation and metabolism:molecular mechanisms and clinical implication.Acta Pharmacol Sin,2023,44:710-725.
8 Holmes TH.Ten categories of statistical errors:a guide for research in endocrinology and metabolism.Am J Physiol Endocrinol Metab,2004,286:E495-501.
9 Hu W,Zhan B,Li Q,et al.Circulating CTRP7 is a potential predictor for metabolic syndrome.Front Endocrinol(Lausanne),2021,12:774309.
10 Li K,Liang Z,Xu W,et al.CTRP7 Is a biomarker related to insulin resistance and oxidative stress:cross-sectional and intervention studies in vivo and in vitro.Oxid Med Cell Longev,2022,2022:6877609.
11 郭小芳,王国举,曾涛.医学营养治疗对妊娠期糖尿病孕妇剖宫产、新生儿并发症等妊娠结局影响的前瞻性研究.当代医药论丛,2022,20:68-71.
12 金芳,宋文琪,彭亚光,等.北京地区儿童网织红细胞参数参考区间的建立及验证[J].中华检验医学杂志,2024,47:554-560.
13 Sharma AK,Singh S,Singh H,et al.Deep insight of the pathophysiology of gestational diabetes mellitus.Cells,2022,11.
14 de Gennaro G,Palla G,Battini L,et al.The role of adipokines in the pathogenesis of gestational diabetes mellitus.Gynecol Endocrinol,2019,35:737-751.
15 Baeyens L,Hindi S,Sorenson RL,et al.β-Cell adaptation in pregnancy.Diabetes Obes Metab,2016,18 Suppl 1:63-70.
16 Plows JF,Stanley JL,Baker PN,et al.The Pathophysiology of Gestational Diabetes Mellitus.Int J Mol Sci,2018,19:3342.
17 Wang Y,Wu H,Ding H,et al.Changes of insulin resistance and β-cell function in women with gestational diabetes mellitus and normal pregnant women during mid- and late pregnant period:a case-control study.J Obstet Gynaecol Res,2013,39:647-652.
18 Pantham P,Aye ILMH,Powell TL.Inflammation in maternal obesity and gestational diabetes mellitus.Placenta,2015,36:709-715.
19 Wu H,Perrard XD,Wang Q,et al.CD11c expression in adipose tissue and blood and its role in diet-induced obesity.Arterioscler Thromb Vasc Biol,2010,30:186-192.
20 颜彦,柳洲,刘大庆.妊娠期糖尿病患者血糖代谢表现异质性的分析.中国临床医学,2014,21:682-685.