宫颈癌是全球范围内严重危害女性健康的公共卫生问题[1]。持续感染的人乳头瘤病毒(human papillomavirus,HPV)是导致宫颈癌的主要病因[2]。从HPV感染到宫颈癌通常需要长达十余年之久,这一漫长的癌前阶段使得提早筛查、干预成为可能[3]。目前临床筛查宫颈癌的方式主要为液基细胞学检测(thinprep cytology test,TCT)和HPV检测,高危HPV检测具有较高的灵敏度而特异度较低,TCT的特异度较高而灵敏度低,因此,目前大多采用高危HPV检测与TCT联合筛查,提高诊断的准确性[4-5]。对于高风险人群建议进行阴道镜转诊,根据病变情况定位活检。然而,并非所有初筛异常患者的组织病理学结果均为阳性,而且阴道镜活检为有创检查,增加患者心理负担与身体创伤。因此,临床上需要一种能降低阴道镜转诊的无创且精确的检测方式。基因甲基化是调控基因转录的一种至关重要的表观遗传机制,已是目前肿瘤领域与精准医学研究的热点[6-7]。Septin9是抑癌基因,可参与多种生物过程,该基因启动子区域的CpG岛高甲基化导致该基因表达减少或沉默,降低了该基因的转录活性,从而促进宫颈癌细胞的增殖、侵袭和迁移[8]。研究表明,Septin9甲基化检测可作为多种肿瘤的有力筛查、诊断工具,但在宫颈癌中的应用较少[9-10]。因此,本文对Septin9甲基化检测用于宫颈癌筛查的诊断效能分析,以探讨Septin9甲基化检测在宫颈癌筛查中的临床价值。
对象与方法
1.研究对象:选择2019年10月至2022年10月在青海红十字医院及本院的全省医联体医院行宫颈癌筛查(高危HPV和TCT)的女性患者,筛查结果符合《中国子宫颈癌筛查及异常管理相关问题专家共识》[11]中转诊阴道镜活检指征者,并行Septin9基因甲基化检测与阴道镜活检组织病理学检测。所有患者知情同意且获得青海红十字医院伦理委员会批准(KY-2020-20)。
2.纳入标准:(1)均行高危HPV检测、TCT、Septin9甲基化检测与阴道镜活检组织病理学检测。(2)有过性生活的女性患者,没有宫颈治疗史,存在完整宫颈;(3)取样时未处于月经期及孕期,取样时机选择月经干净3~5 d内取样;(4)未合并其它妇科恶性肿瘤以及其他内外科疾病;(5)绝经期行宫颈癌筛查的女性。
3.研究对象分组:以阴道镜活检组织病理学结果为金标准,将研究对象分为两组:阴性组包括组织病理学结果为阴性或宫颈炎症的患者;阳性组包括组织病理学结果为LSIL、HSIL、宫颈癌的患者。
4.HPV、TCT标本采集:两者标本采集方法相同,患者取膀胱截石位后使用阴道窥器使宫颈充分的暴露。宫颈刷置于宫颈的移行带处,刷头置于宫颈管内按照同一方向旋转刷取宫颈脱落细胞,将样本送至本院病理科分别进行HPV、TCT检测。HPV分型为:81、68、66、58、59、56、53、52、51、45、39、35、33、31、16、18判读为高危HPV阳性。TCT结果≥ASCUS判读为TCT阳性。
5.Septin9基因甲基化标本采集与检测:临床标本采集方法同HPV、TCT采集,于阴道镜活检组织病理学检测前完成标本采集。Septin9甲基化检测步骤:(1)标本和对照品的核酸提取处理:将阴性质控品和阳性质控品编号EP管中加入1mL宫颈分泌物样本,12 000 rpm离心机(iCen 24,杭州奥盛有限公司)离心2 min,弃上清留沉淀约200 μL,加入200 μL裂解液与10 μL蛋白酶K,涡旋15 s,混匀仪(Vortex dancer 111S,莱普特有限公司)混匀。加入50 μL 焦碳酸二乙酯水涡旋混匀,离心取上清备用。(2)提取核酸质量评估:使用紫外分光光度计(Nano100,杭州奥盛有限公司测量)测量DNA样本OD260/OD280在1.6~2.0内为合格,若OD260/OD230>2.0,DNA浓度则需>100 ng/μL。(3)硫酸盐转化:将融化好的基因组DNA 加洗脱液后涡旋混匀、短暂离心,加入适量亚硫酸盐溶液保护液,在恒温孵育器设置80 ℃,孵育45 min,洗涤吸去上清液后干燥沉淀。(4)加样:配制20∶1的PCR反应液(ZP-NP-001,广州奇辉生物有限公司)16 μL和0.8 μL DNA聚合酶(M150I,isher),分装至PCR反应板15 μL。(5)PCR扩增:定量荧光PCR仪(ABI7500 Thermo,isher)设置参数:扩增第一阶段,循环1次,设置94 ℃、20 min、40%的温度升降速率;扩增第二阶段,循环45次,设置62 ℃、5 s、80%的温度升降速率,55.5 ℃、35 s、80%的温度升降速率,93 ℃、30 s、40%的温度升降速率;扩增第三阶段,循环1次,设置40 ℃、5 s、80%的温度升降速率;循环45次,反应体系为30 μL。荧光通道检测选择:选用FAM和JOE通道。(6)结果分析:若内参JOE通道信号为阴性或Ct>28.5提示检测结果无效,若Ct(FAM)=45或未检出时提示无甲基化,若Ct>8提示低度甲基化,若Ct<8提示高度甲基化,若Ct<23,提示加入的样本DNA过量。
6.阴道镜活检组织病理学检测:患者取膀胱截石位后用阴道窥器使宫颈充分暴露,进行醋酸白试验和碘试验后对宫颈可疑部位进行定位活检和宫颈管搔刮,固定标本后送本院病理科作出诊断,阴道镜活检组织病理学结果≥LSIL判读为组织病理学阳性。
7.统计学方法:采用SPSS 26.0 软件进行统计分析,计量资料以![]() 表示,两组比较采用两独立样本t检验,计数资料用百分率(%)表示,组间比较用卡方检验或Fisher确切概率法,线性趋势采用Cochran-Armitage趋势检验,以组织病理学结果作为诊断金标准,使用MedCalc软件绘制ROC曲线,比较各筛查方法的受试工作曲线下面积(the area under the curve,AUC),评价各检测方式对宫颈癌筛查的诊断效能。
表示,两组比较采用两独立样本t检验,计数资料用百分率(%)表示,组间比较用卡方检验或Fisher确切概率法,线性趋势采用Cochran-Armitage趋势检验,以组织病理学结果作为诊断金标准,使用MedCalc软件绘制ROC曲线,比较各筛查方法的受试工作曲线下面积(the area under the curve,AUC),评价各检测方式对宫颈癌筛查的诊断效能。
结果
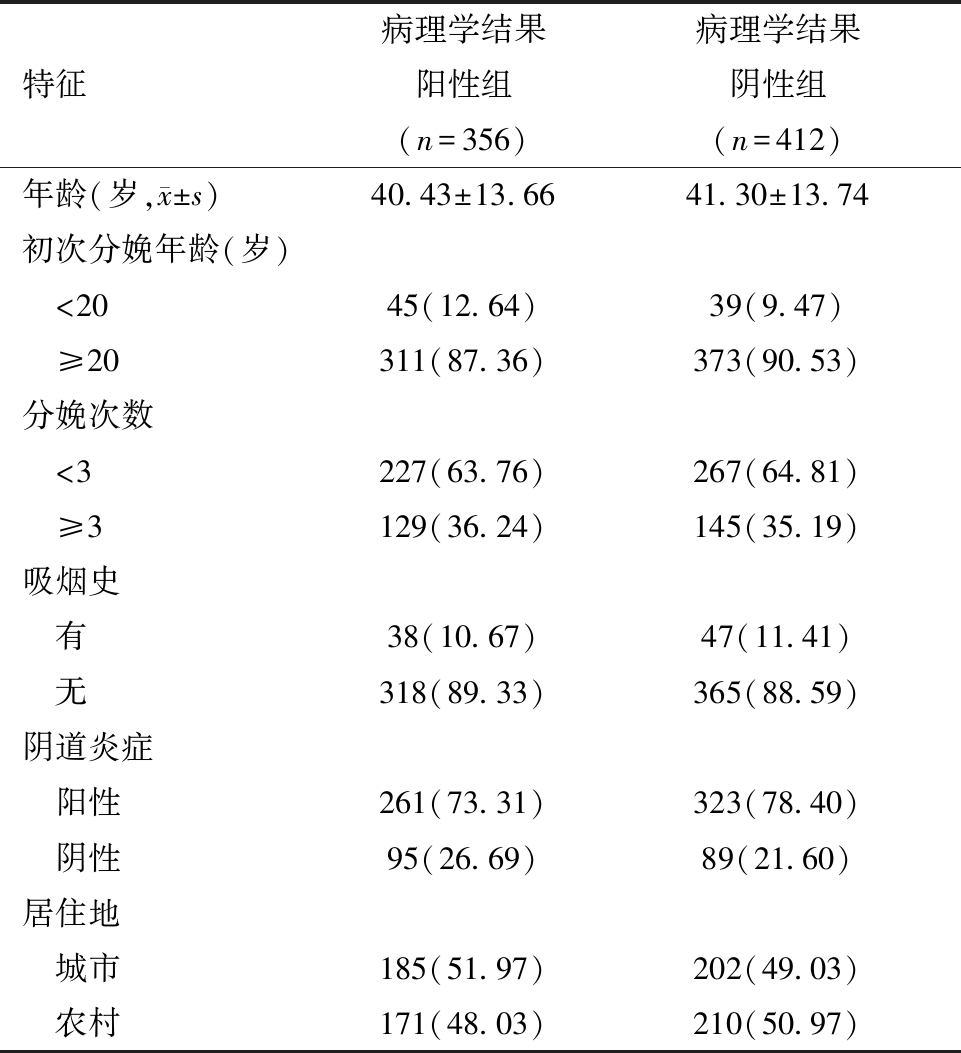
1.一般资料:共收集病例768例,根据阴道镜活检组织病理学结果分为阳性组356例、阴性组412例,两组研究对象的各基本特征比较,结果差异均无统计学意义(P均>0.05),两组具有可比性。见表1。
表1 研究对象的基本特征[例(%)]
特征病理学结果阳性组(n=356)病理学结果阴性组(n=412)年龄(岁, x±s)40.43±13.6641.30±13.74初次分娩年龄(岁) <2045(12.64)39(9.47) ≥20311(87.36)373(90.53)分娩次数 <3227(63.76)267(64.81) ≥3129(36.24)145(35.19)吸烟史 有38(10.67)47(11.41) 无318(89.33)365(88.59)阴道炎症 阳性261(73.31)323(78.40) 阴性95(26.69)89(21.60)居住地 城市185(51.97)202(49.03) 农村171(48.03)210(50.97)
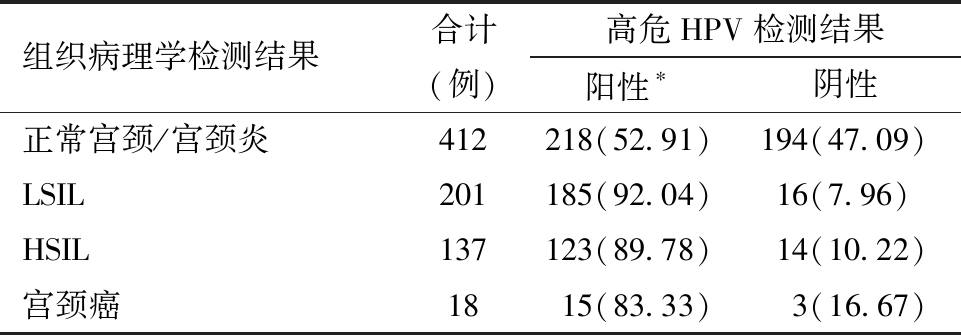
2.高危HPV检测在各组织病理学检测结果中的检出率比较:高危HPV检测在四组组织病理学检测结果中检出率的差异具有统计学意义(P<0.001),见表2。
表2 高危HPV检测在各组织病理学检测结果中的检出率比较[例(%)]
注:组间比较,*P<0.001
组织病理学检测结果合计(例)高危HPV检测结果阳性∗阴性正常宫颈/宫颈炎412218(52.91)194(47.09)LSIL201185(92.04)16(7.96)HSIL137123(89.78)14(10.22)宫颈癌1815(83.33) 3(16.67)
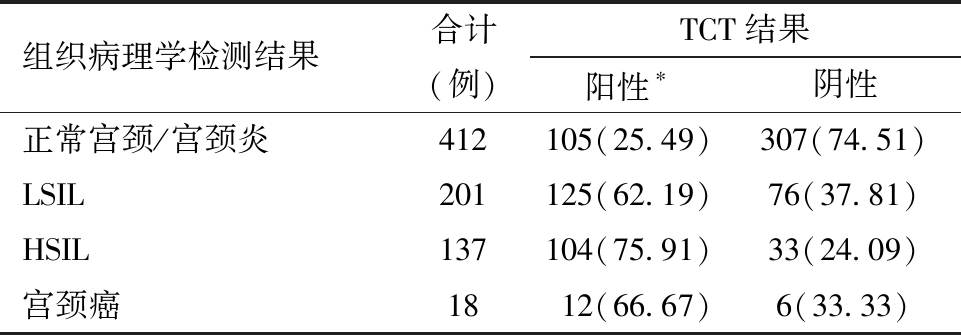
3.TCT在各组织病理学检测结果中的检出率比较:TCT在四组组织病理学检测结果中检出率的差异具有统计学意义(P<0.001),见表3。
表3 TCT在各组织病理学检测结果中的检出率比较[例(%)]
注:组间比较,*P<0.001
组织病理学检测结果合计(例)TCT结果阳性∗阴性正常宫颈/宫颈炎412105(25.49)307(74.51)LSIL201125(62.19)76(37.81)HSIL137104(75.91)33(24.09)宫颈癌1812(66.67)6(33.33)
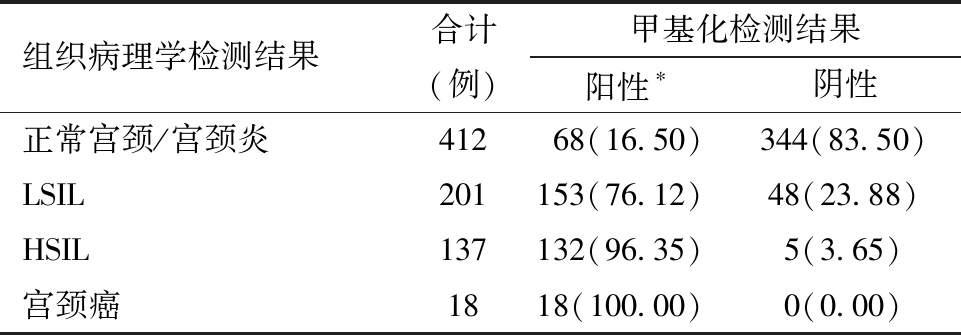
4.Septin9甲基化检测在各组织病理学结果中的检出率比较:Septin9甲基化检测在四组组织病理学检测结果中检出率的差异具有统计学意义(P<0.001),见表4。采用 Cochran-Armitage 趋势检验发现宫颈病变程度与Septin9甲基化之间存在线性趋势(P<0.05),即Septin9基因甲基化的检出率随着宫颈病变严重程度增加逐渐升高。
表4 Septin9甲基化检测在各组织病理学结果中的检出率比较[例(%)]
注:组间比较,*P<0.001
组织病理学检测结果合计(例)甲基化检测结果阳性∗阴性正常宫颈/宫颈炎41268(16.50)344(83.50)LSIL201153(76.12)48(23.88)HSIL137132(96.35)5(3.65)宫颈癌1818(100.00)0(0.00)
5.四种检测方式在宫颈病变中的诊断效能比较:与高危HPV检测相比,Septin9甲基化检测的特异度、阳性预测值、准确率及AUC较高(P均<0.05),而灵敏度与阴性预测值无统计学差异(P均>0.05);与TCT相比,Septin9甲基化检测的灵敏度、阴性预测值、准确率及AUC较高(P均<0.05);而特异度与阳性预测值无统计学差异(P均>0.05);与高危HPV联合TCT相比,Septin9基因甲基化检测的灵敏度、阴性预测值较高(P值均<0.05),而特异度、阳性预测值不及高危HPV联合TCT检测(P均<0.05),其准确率与AUC与两者联合筛查对比无统计学差异(P均>0.05)。见表5、图1。
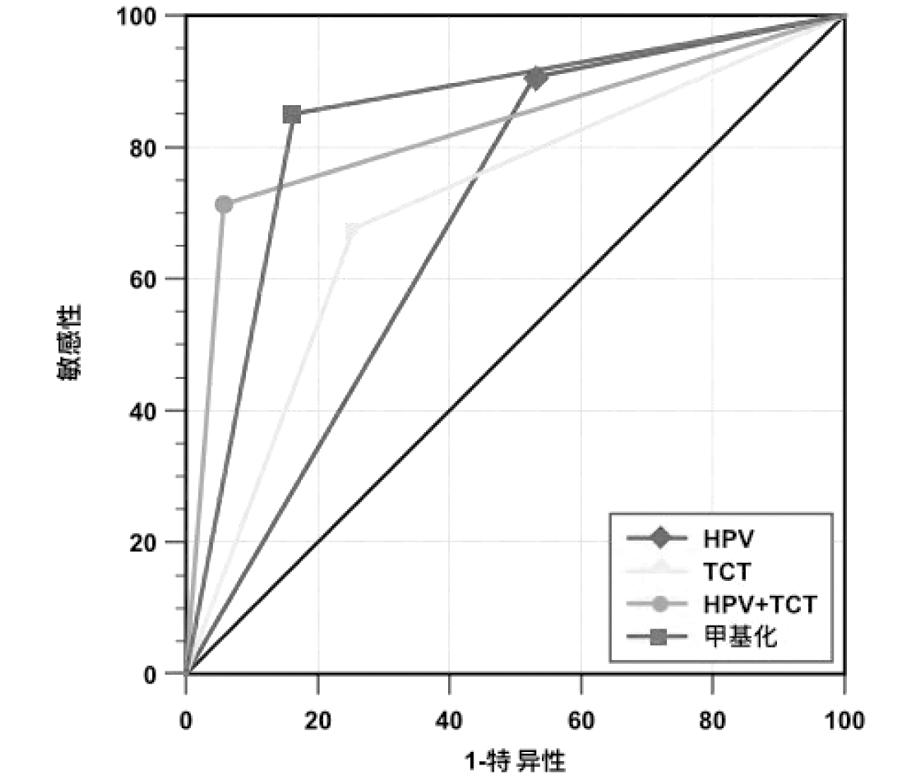
图1 四种检测方式诊断宫颈病变的ROC曲线
表5 四种检测方式在宫颈病变中的诊断效能比较
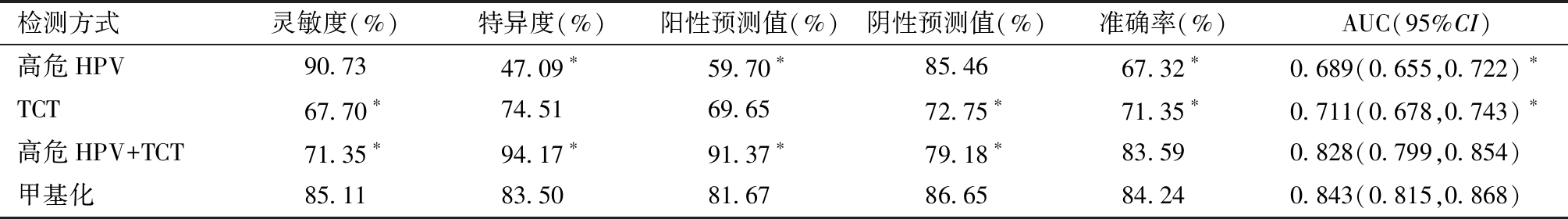
注:与甲基化组比较,*P<0.05
检测方式灵敏度(%)特异度(%)阳性预测值(%)阴性预测值(%)准确率(%)AUC(95%CI)高危HPV90.7347.09∗59.70∗85.4667.32∗0.689(0.655,0.722)∗TCT67.70∗74.5169.6572.75∗71.35∗0.711(0.678,0.743)∗高危HPV+TCT71.35∗94.17∗91.37∗79.18∗83.590.828(0.799,0.854)甲基化85.1183.5081.6786.6584.240.843(0.815,0.868)
讨论
宫颈癌是最常见而且危害极大的女性生殖道恶性肿瘤。研究已经证实了HPV感染和宫颈癌的因果关系[12]。本研究356例组织病理学阳性患者中,HPV阳性检出率高达90.73%。并非所有的HPV感染都会致癌,大多是短暂的、一过性的,能被自身免疫系统所清除[13]。本研究中,在412例组织病理学阴性结果中的高危HPV的阳性检出率高达52.91%,说明部分高危HPV阳性患者的组织病理学结果不一定为阳性,因此,部分感染高危HPV的患者是不需要治疗的。据统计,性活跃的妇女约80%感染HPV,但是在3年的时间里,几乎90%的感染可自发消除,只有10%为持续感染,持续感染的患者中只有1%发展成宫颈癌[14]。因此,宫颈癌患者预后的关键在于早筛查及早诊断。
目前,临床上常用的宫颈癌筛查方法有:高危HPV检测和TCT。TCT操作流程较复杂,在涂片、染色、镜下检测等复杂过程中,易出现细胞重叠、炎症背景杂乱等问题,受病理医师主观因素影响较大,影响检测结果的准确性,容易造成漏诊[15]。HPV检测也是宫颈癌筛查中推荐的检测方式,不仅可以检测HPV的存在,还可以确定病毒亚型,判断是高危型还是低危型感染,更容易聚焦高风险人群[16]。但HPV检测比TCT在宫颈癌筛查中具有更高的灵敏度,但其特异性较低,大多为一过性感染,容易引起患者的恐慌[17]。本研究结果也同样证实,高危HPV检测的灵敏度(90.73%)和阴性预测值(85.46%)均高于TCT的灵敏度(67.70%)和阴性预测值(72.75%),但是高危HPV检测的特异度(47.09%)和阳性预测值(59.70%)均低于TCT的特异度(74.51%)和阳性预测值(69.65%),说明采用高危HPV作为宫颈癌筛查时易造成假阳性,从而增加误诊风险;而采用TCT作为初筛,则易导致假阴性,从而增加漏诊风险。而两者联合筛查则可以弥补单独筛查的不足,因此,根据中国国情,国内专家推荐采用多元化的宫颈癌筛查方法[18]。本文高危HPV联合TCT筛查中准确率(83.59%)及AUC(0.828)较单独筛查时均明显提高,证明高危HPV联合TCT筛查较单独筛查能提高诊断效能。联合筛查异常的患者需要转诊阴道镜定位活检,然而数据显示>60%的宫颈低级别病变会自然好转,只有约10%的宫颈低级别病变在2至4年发展成宫颈高级别病变,约1%的低级别病变可进展为子宫颈癌[19-20]。本研究中因为纳入的所有患者均满足转诊阴道镜活检的指征,并且在阴道镜活检之前均行了Septin9甲基化检测,根据本研究数据表明最终的宫颈活检组织病理学结果中仍有412例为阴性,这就意味着这412例患者没有必要转诊有创的阴道镜活检和相应的临床干预治疗,以免增加初筛异常患者对疾病的恐慌以及不必要的有创伤害。
DNA甲基化是指胞嘧啶磷酸鸟嘌呤位点的5′端的碳原子在DNA甲基转移酶的催化作用下与S腺苷甲硫氨酸提供的活性甲基共价结合,形成DNA甲基化修饰[21]。Septin9是一个抑癌基因,在宫颈病变的过程中,该基因启动子区域的CpG岛高甲基化导致该基因表达减少或沉默,降低了该基因的转录活性,失去抑癌基因的保护,从而促进宫颈癌细胞的增殖、侵袭和迁移,有研究发现甲基化水平升高的趋势随着宫颈病变严重程度而增加,高 CpG 岛甲基化表型使宫颈高级别病变的风险增加 50.6 倍以及宫颈癌的风险增加 122 倍,结果表明 CpG 岛的高甲基化水平参与了宫颈癌的进展[8]。本研究采用Cochran-Armitage 趋势检验发现宫颈病变程度与Septin9甲基化之间存在线性趋势(P<0.05),即Septin9甲基化的检出率随着宫颈病变严重程度增加逐渐升高,证实Septin9甲基化水平影响宫颈病变的程度。
越来越多的研究表明,在恶性肿瘤组织中往往伴随多个抑癌基因启动子区高甲基化,使这些基因的表达下调甚至沉默,降低了该基因转录活性,最终诱导癌的发生[22]。国内外大量研究证实,基因甲基化是临床上用于宫颈癌筛查的理想生物标记物,Liang等[23]对150例宫颈癌筛查异常患者的研究中,在宫颈高级别病变和宫颈癌中,PAX1甲基化检测灵敏度为91.9%、特异度为72.8%及AUC为0.878,ZNF582甲基化检测灵敏度为97.3%、特异度为76.7%及AUC为0.900;两者的诊断价值均高于TCT与高危HPV检测,PAX1、ZNF582甲基化可作为宫颈癌筛查的重要生物标志物。Jiao等[9]证实了Septin9在宫颈癌组织中过度表达并且对Septin9甲基化在检测宫颈癌及癌前病变中的灵敏度、特异度及AUC作了分析,但是该检测在临床中用于宫颈癌筛查的效能和可行性还需要进一步评估和验证。本文对Septin9甲基化在临床中的应用价值进行研究,其准确率(84.24%)与AUC(0.843)与本研究中高危HPV联合TCT的准确率(83.59%)与AUC(0.828)对比差异无统计学意义,但准确率与AUC均高于高危HPV、TCT单独筛查。说明与已研究的PAX1、ZNF582甲基化检测的结果一致,Septin9甲基化对宫颈癌及癌前病变的诊断效能均高于高危HPV检测、TCT单独筛查,而与两者联合筛查的诊断效能相当。而且本研究还证实了Septin9甲基化阳性检出率随着宫颈病变严重程度的增加而逐渐升高,Septin9甲基化检测在HSIL中的检出率为96.35%,而在宫颈癌中的检出率高达100%,说明其对阴道镜活检组织病理学结果中宫颈低级别以上病变的阳性检出率较高,更容易聚焦到宫颈高级别病变以及宫颈癌的患者。本文数据显示组织病理学阴性结果412例中,Septin9甲基化检测阴性结果为344例,因此,若转诊阴道镜定位活检前先行Septin9甲基化检测可降低44.79%(344/768)的阴道镜转诊率。所以Septin9甲基化检测为初筛异常的患者提供一种无创且较为精准的宫颈癌筛查方法,降低了一部分患者的阴道镜转诊率,使患者受益。研究表明基因甲基化检测作为高危HPV分流可弥补TCT的不足,Pun等[24]对POU4F3、HS3ST2、AJAPI、PAX1和SOX1五个基因甲基化检测分别用于分流高危 HPV阳性患者,其中在检测宫颈高级别病变及宫颈癌中POU4F3的AUC最高为0.86,敏感度为74%,特异度为89%,均高于TCT检测,提示POU4F3甲基化检测对高危HPV阳性患者分流具有较高的诊断价值。本研究中采用Septin9甲基化检测与TCT分流高危HPV患者,Septin9 甲基化检测的灵敏度(85.11%)、阴性预测值(86.65%)、准确率(84.24%)及 AUC(0.843)均高于TCT 的灵敏度(67.70%)、阴性预测值(72.75%)、准确率(71.35%)及AUC(0.711),结果表明,作为高危HPV阳性患者的分流,Septin9 基因甲基化检测的分流效能与以往研究的 POU4F3 基因甲基化检测相近,且均高于TCT 分流。
综上所述,Septin9甲基化检测用于宫颈癌筛查及高危HPV分流具有较高的诊断价值,对宫颈高级别病变及宫颈癌的检出率较高以及对降低阴道镜的转诊具有重要意义。
1 刘文敏,付振明.宫颈癌预防与筛查研究进展.中国预防医学杂志,2022,23:713-720.
2 Al Raisi M,Al Yahyai T,Al Kindi R.Knowledge and attitude regarding cervical cancer and human papillomavirus in Oman.Sultan Qaboos Univ Med J,2022,22:493-500.
3 Kyrgiou M,Arbyn M,Bergeron C,et al.Cervical screening:ESGO-EFC position paper of the European Society of Gynaecologic Oncology(ESGO) and the European Federation of Colposcopy(EFC).Br J Cancer,2020,123:510-517.
4 Bedell SL,Goldstein LS,Goldstein AR,et al.Cervical cancer screening:past,present,and future.Sex Med Rev,2020,8:28-37.
5 王冬英,丁红辉.阴道镜联合液基细胞学检测鉴别宫颈高级别鳞状上皮病变性质的价值.中国妇幼保健,2022,37:1905-1909.
6 Dasari K,Somarelli JA,Kumar S,et al.The somatic molecular evolution of cancer:Mutation,selection,and epistasis.Prog Biophys Mol Biol,2021,165:56-65.
7 Li L,Wang Y,Mou Y,et al.KDM1A Identified as a potential oncogenic driver and prognostic biomarker via multi-omics analysis.Can J Infect Dis Med Microbiol,2021,2021:4668565.
8 Li B,Huang H,Huang R,et al.SEPT9 gene methylation as a noninvasive marker for hepatocellular carcinoma.Dis Markers,2020,2020:6289063.
9 Jiao X,Zhang S,Jiao J,et al.Promoter methylation of SEPT9 as a potential biomarker for early detection of cervical cancer and its overexpression predicts radioresistance.Clin Epigenetics,2019,11:120.
10 刘贵平.Septin9介导上皮间质转化在子宫颈鳞癌发生发展及预后中作用的初步研究.泸州:西南医科大学,2019.
11 赵昀,魏丽惠.CSCCP关于中国宫颈癌筛查及异常管理相关问题专家共识解读.实用妇产科杂志,2018,34:101-104.
12 He YH,Su RJ,Zheng J.Detection of DKK-1 gene methylation in exfoliated cells of cervical squamous cell carcinoma and its relationship with high risk HPV infection.Arch Gynecol Obstet,2021,304:743-750.
13 Chen H,Wang H,Liu J,et al.Association of the MUTYH Gln324His(CAG/CAC) variant with cervical carcinoma and HR-HPV infection in a Chinese population.Medicine(Baltimore),2019,98:e15359.
14 Chen L,Dong B,Gao H,et al.HPV-16 E2/E6 and POU5F1B as biomarkers to determine cervical high-grade squamous lesions and more.J Inflamm Res,2020,13:813-821.
15 王金玲,张燕萍,魏瑛.高危型HPV检测联合TCT检查用于宫颈癌筛查的应用探究.甘肃科技,2020,36:150-152.
16 黄丹,王紫薇,鞠梅.人乳头瘤病毒感染及诊疗新动向.中国临床新医学,2021,14:245-250.
17 刘晓旭,梁建梅,苏学艳,等.HPV DNA和HPV E6/E7 mRNA检测在宫颈病变诊治中应用价值的比较.国际妇产科学杂志,2021,48:462-466.
18 魏丽惠.面向加速消除宫颈癌的挑战.中国妇产科临床杂志,2021,22:1-2.
19 魏丽惠,赵昀.关于《子宫颈癌等人乳头瘤病毒相关疾病免疫预防专家共识》的临床要点解读.中国妇产科临床杂志,2020,21:1-2.
20 王凯怡,胡庆伟.高危人乳头瘤病毒E6/E7 mRNA以及病毒载量检测在高危人乳头瘤病毒阳性女性宫颈癌筛查分流中的应用.中国性科学,2021,30:61-65.
21 Botezatu A,Goia-Rusanu CD,Iancu IV,et al.Quantitative analysis of the relationship between microRNA-124a,-34b and -203 gene methylation and cervical oncogenesis.Mol Med Rep,2011,4:121-128.
22 Marquardt J,Chen X,Bi E.Septin assembly and remodeling at the cell division site during the cell cycle.Front Cell Dev Biol,2021,9:793920.
23 Liang H,Li GL,Liu J,et al.The application value of PAX1 and ZNF582 gene methylation in high grade intraepithelial lesion and cervical cancer.Clin Transl Oncol,2021,23:283-288.
24 Pun PB,Liao YP,Su PH,et al.Triage of high-risk human papillomavirus-positive women by methylated POU4F3.Clin Epigenetics,2015,7:85.