Mohr-Tranebjaerg综合征(Mohr-Tranebjaerg syndrome,MTS)是一种线粒体疾病,TIMM8A蛋白在线粒体内功能缺陷,从而无法形成 TIMM8A/TIMM13复合物,影响其他蛋白在线粒体内正常运送[1]。X连锁无丙种球蛋白血症(X-linkedagammaglobulinemia,XLA)是一种原发性体液免疫缺陷病。是由于Bruton酪氨酸激酶(Brutontyrosinekinase ,Btk)的信号转导分子缺陷引起,最终导致XLA。现就1例Mohr-Tranebjaerg综合征合并X连锁无丙种球蛋白血症患儿的临床特点、诊断及治疗方法结合文献进行分析探讨。
临床资料
患儿,男,4岁4月,因“跛行3周”入中山大学孙逸仙纪念医院深汕中心医院就诊,患儿系G4P4,40周经阴道分娩出生,出生体重3.15 kg,出生时有“黄疸”史,否认窒息抢救史,生后纯母乳喂养,6月龄改人工喂养,按时添加辅食。运动:8月龄会爬,13月龄会走,1岁会叫“爸爸、妈妈”,现可讲简单词汇,对大声呼唤有反应。预防接种按计划进行。3周前低热正常后出现左侧下肢疼痛,不能指出疼痛部位,拒绝行走,无关节红肿,前往海南当地医院,考虑“滑膜炎”,予制动处理后,2周前下肢疼痛自行缓解,可行走、跑步,呈跛行步态,左足背屈受限伴足下垂。既往患儿每月有多次上呼吸道感染病史。患儿出生后及1岁龄两次行听力筛查均未通过,为双侧听力异常。父母非近亲结婚,患儿父母及兄弟姐妹均体健。家中无类似病人。入院时体格检查:身高94.5 cm,体重14.1 kg。神志清楚,表情正常,反应好。耳廓无畸形,外耳道未见异常分泌物。双肺呼吸音清,未闻及干湿性啰音。心脏听诊未见异常。腹平软,未触及肿大肝脾,肠鸣音正常。脊柱生理弯曲存在,棘突无压痛、叩痛,脊柱四肢无畸形,肌肉无萎缩、无压痛,左下肢踝关节活动背屈受限伴足下垂,关节无红肿压痛、畸形、肿胀,无短肢,四肢皮温正常,肌张力正常,肌力V级。跛行步态,巴氏征、克氏征等病理征未见异常。入院实验室检查:尿、粪常规、肝肾功能、心肌酶、乳酸、甲功、致畸四项、氨基酸和酰基肉碱谱分析、尿液有机酸分析均未见异常。血常规示白细胞及CRP升高。淋巴细胞亚群示T细胞87.10%,B细胞0,淋巴细胞 7.05×109/L,NK细胞 11.30%,CD8+T细胞/淋巴细胞 35.60%,CD4+T细胞/淋巴细胞 41.80。免疫六项示免疫球蛋白A及免疫球蛋白G低于正常下限,余项正常。听性脑干诱发电位示双耳声刺激未见I、III、V波分化,极重度异常(见图1)。神经传导速度示左侧总神经传导未引出电位(图2)。腹部彩超、心电图、左侧髋关节正侧位、腰椎MRI、眼底检查未见异常。头颅核磁共振成像示双侧大脑角对称性小片状异常信号,大小各约8 mm*4 mm*3 mm,T1WI低信号,T2WI及T2-FLAIR高信号,考虑局部神经细胞损害(图3、图4)。
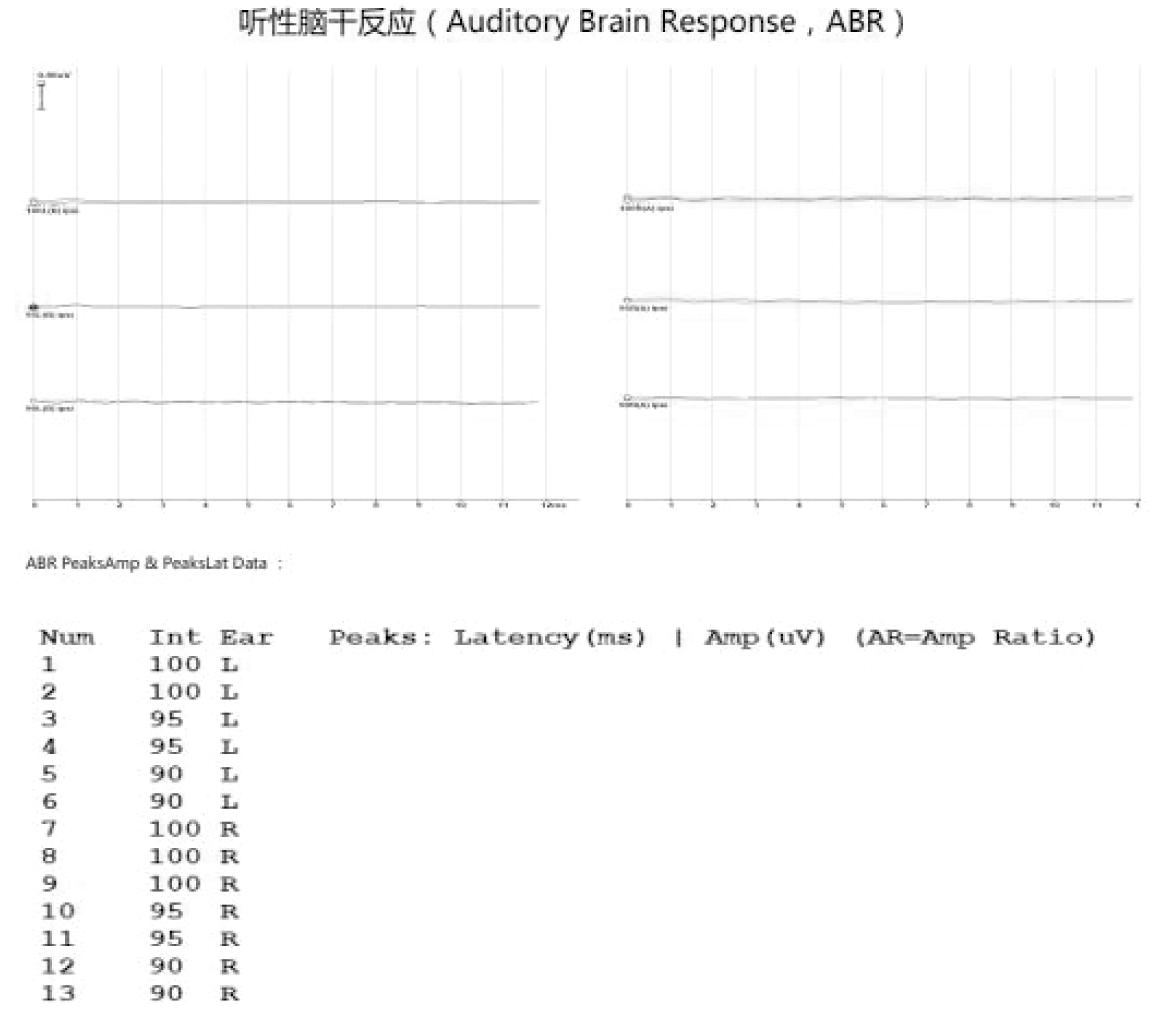
图1 听性脑干反应:ABR测试极重度异常
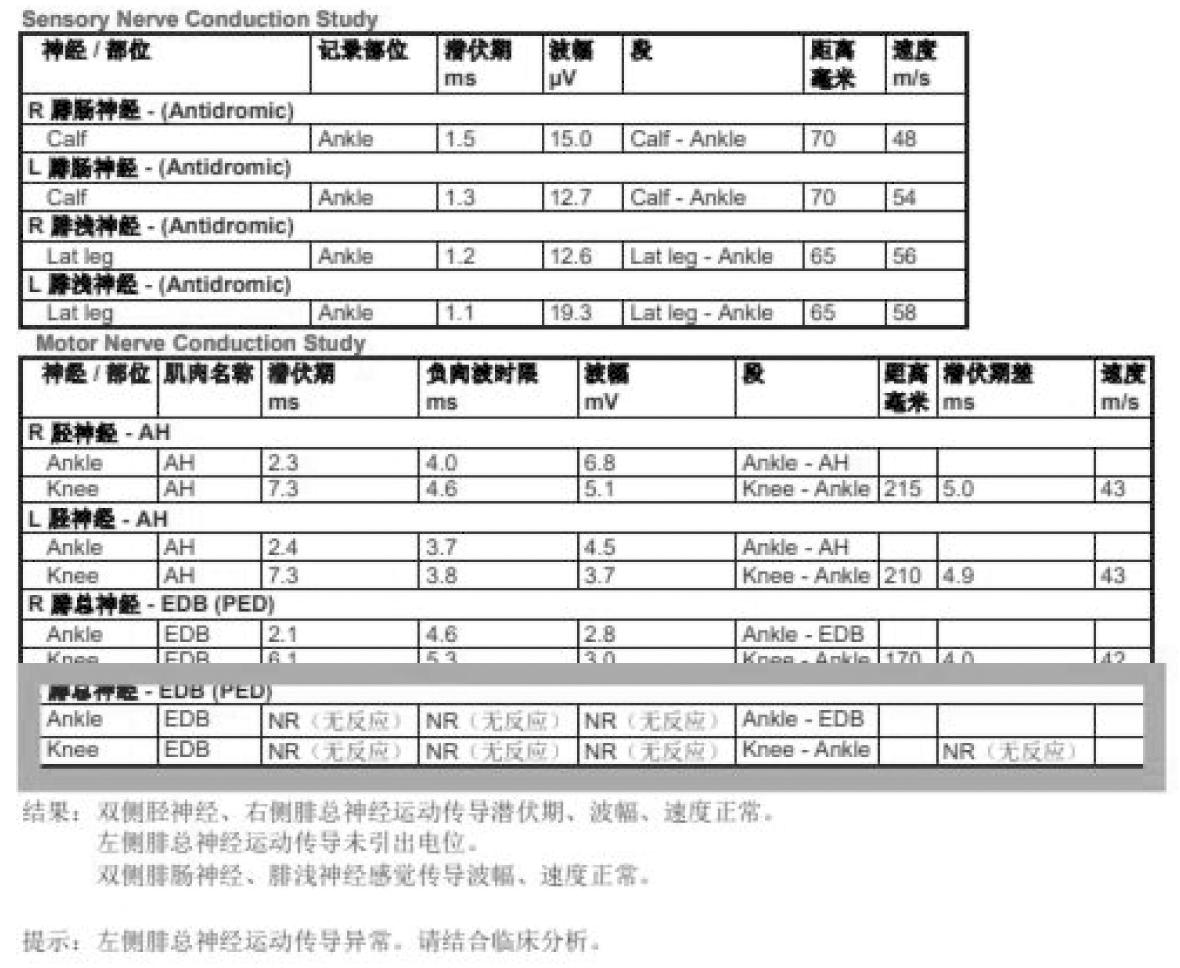
图2 神经传导速度
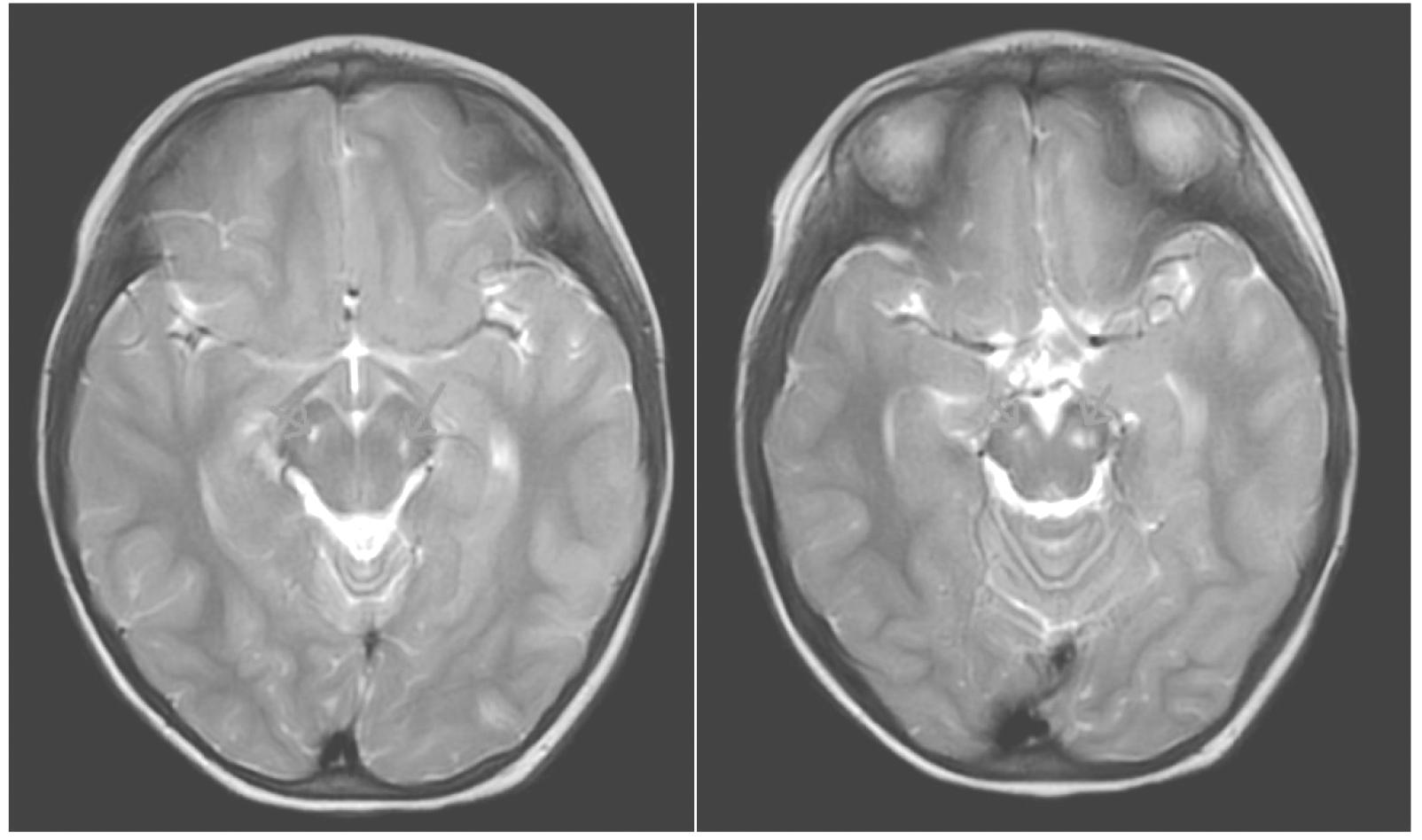
图3 颅脑MRI T2WI成像示双侧大脑角对称性小片状异常信号,大小各约8mm*4mm*3mm,T2WI高信号,增强未见强化
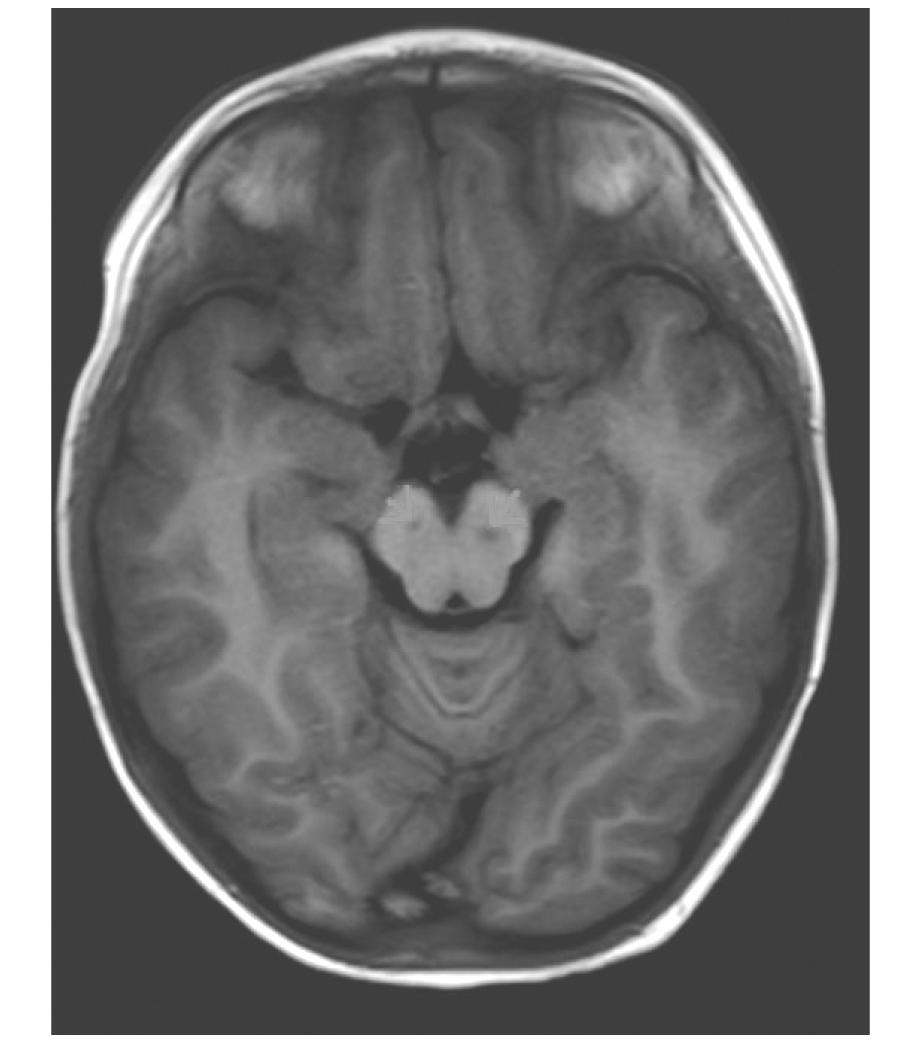
图4 颅脑MRI T1WI成像示双侧大脑角对称性小片状异常信号,大小各约8mm*4mm*3mm,T1WI低信号,增强未见强化
经患儿家属同意,收集患儿外周血4 mL,送中山大学孙逸仙纪念医院行全外显子基因测序,通过高通量测序技术,与参考序列(hg19)进行比较。全外显子测序结果分析示:(1)患儿携带 X 染色体上 chrX:100603389-100608339 约 4.95Kb 的缺失,拷贝数为 0,变异来源未知。(2)①该缺失与 DGV Gold Standard、gnomAD v2.1 不重叠,即在该数据库收录的部分普通人群中未见到类似半合子变异;②该缺失区域累及 TIMM8A 基因外显子 1(NM_004085.4),该基因总共有 2 个外显子,和 BTK 基因外显子 18-19(NM_000061.3)。ClinGen 关于该缺失区域内的 TIMM8A 基因(OMIM*300356)和 BTK 基因(OMIM*300300)的单倍剂量不足敏感性评分为 3,即目前有足够的证据表明该基因的功能缺失突变具有致病性,与患儿目前疾病的表型相符合。进一步对患儿及父母进行该CNV的鉴定及来源分析,采用PCR、gap-PCR(跨越断点区域的间隙PCR)和一代测序,发现患儿携带(hg19)chrX:100603112-100608757之间5.645kb的缺失(如图5所示)。患儿父母未检测到以上区域的缺失,提示患儿所携带缺失变异为新发变异。
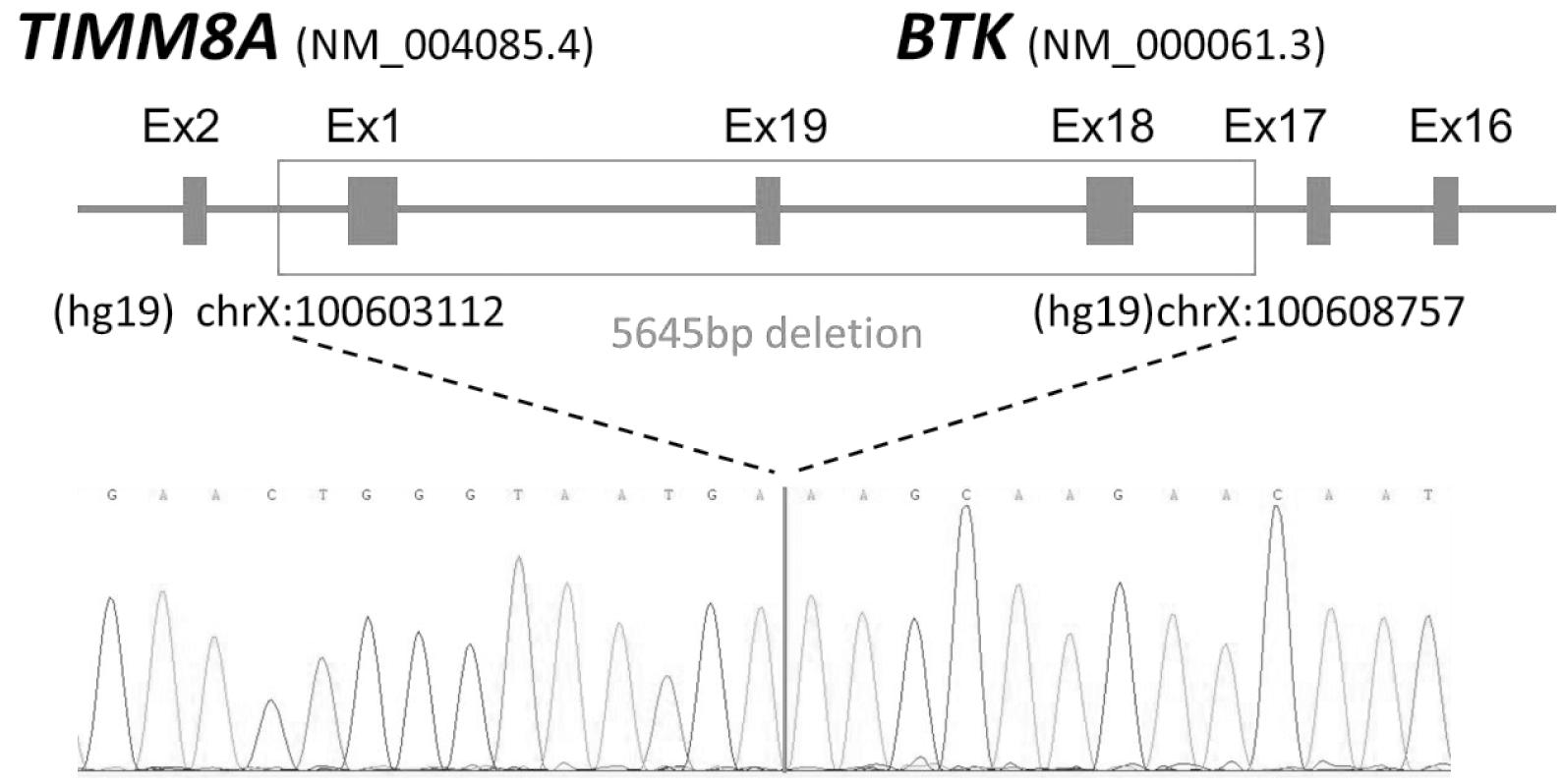
图5 一代测序
材料方法:根据全外显子组二代测序所示CNV缺失,对患儿及父母外周血DNA进行PCR、gqp-PCR和一代测序。Gap-PCR引物:Forward primer:5′-TGGGAGCCAATCCTCTCATAGC-3′,Reverse primer:5′-TGACACTCTTGTGACCGTGC-3′。Sange测序检测所扩增片段引物:Forward primer:5′-GGGCCTATGGAAACCAATGACT-3′,Reverse primer:5′-AGTTCAGCAGCAAATCTGACA-3′。
患儿入院后予头孢曲松钠抗感染、输注丙种球蛋白对症支持治疗,同时予神经康复训练,患儿症状无进行性加重,踝关节活动受限及足下垂较前改善,患儿家属要求出院,门诊随诊。患儿诊断X连锁无丙种球蛋白血症,建议每3-4周定期复查免疫球蛋白水平,定期输注免疫球蛋白0.4-0.6 g/kg,免疫球蛋白IgG维持5-6 g/L以上谷浓度。5个月后随访,患儿跛行未明显好转。对于Mohr-Tranebjaerg综合征这类罕见病无有效治疗手段。
讨论
Mohr-Tranebjaerg综合征为X染色体隐性遗传病,由Mohr和Mageroy在1960年初次报道描述了一个挪威家庭,其中4代男性患有进行性耳聋,当时报道为非综合征性X连锁隐性耳聋[8]。但Tranebjaerg等在1992年[9]和1995年[10]在重新调查初次报道中发现了眼部特征,包括近视、视力下降、视野收缩和视网膜电图异常。耳聋是进行性综合征的一种表现,同时可有皮质失明、肌张力障碍、骨折和精神缺陷的视力障碍的表现。这种综合征型耳聋目前全球报道病例数不超过70例,亚洲病例报道更少,目前文献中7例来自日本,2019年我国报道3例[3],属于极其罕见疾病。目前已报道的致病变异约15种[4]。其中存在联合Mohr- Tranebjaerg综合征及X连锁无丙种球蛋白血症中报道病例更少见。
MTS/XLA连续基因综合征存在的新特征包括:(1)XLA患者伴有感音神经性听力损失;(2)有免疫缺陷家族史或因反复感染耳聋、肌张力障碍或共济失调而导致不明原因的幼儿死亡;(3)有轻度听力障碍和局灶性肌张力障碍的老年女性家族史[6]。在相关报道中发现,其中一例MTS/XLA患者,头颅MRI和MR光谱中检测到神经退行性改变[7]。本例患儿通过全外显子测序,结合临床表型,诊断为Mohr-Tranebjaerg综合征合并X连锁无丙种球蛋白血症,符合第一及第二条发现,暂未发现患儿存在眼底病变情况。对于此后有类似临床表现患儿,需要完善全外显测序检查,明确诊断。该患儿头颅MRI提示局部神经细胞损害,可能为神经退行性改变的前期表现,可继续监测头颅MRI变化,是否能发现影像学数据为该联合缺陷的典型特征。
Mohr-Tranebjaerg综合征的临床表现为肌张力障碍、早发性耳聋和各种神经系统表现。患者一般为男性,受影响的男性在儿童早期出现感音神经性听力障碍,在青少年时期出现缓慢进行性肌张力障碍或共济失调,从约20岁开始视神经萎缩导致视力缓慢进行性下降,并在约40岁开始出现痴呆症。童年期和进展期可能出现人格改变、偏执等精神症状。但是一些女性携带者也可能有轻度听力障碍和轻度肌张力障碍。本例患儿自出生时听力筛查未通过,1岁龄时听力筛查仍未通过,4岁龄时诊断感音性耳聋,并发现左侧腓神经损伤,合并X连锁无丙种球蛋白血症。国外有报道3例Mohr-Tranebjaerg综合征合并XLA中发现TIMM8A基因的较大的连续基因缺失中涉及邻近基因BTK,导致无丙种球蛋白血症[2]。
目前MTS临床诊治包括:(1)使用助听器等辅助听力,对于听神经病助听效果一般很难达到非常满意;(2)药物治疗、康复治疗可以尽可能避免挛缩,适当运动,给予合适的装置帮助日常生活;(3)定期随访行为学、神经精神病学方面的异常。当MTS合并XLA时,治疗上积极抗感染、免疫球蛋白替代极为重要。
MTS是极为罕见的X连锁耳聋-肌张力障碍综合征[5]。临床上遇到男性患儿早期听力筛查未通过,出现神经性耳聋,并有进行性肌张力障碍需警惕该疾病。其中有部分患儿出现反复感染,需完善免疫相关检查,了解是否合并XLA,同时应为患者安排包括TIMMA18基因及BTK基因的基因检测协助诊断。对于有明确分子病因的患者及其家族成员,要进行遗传咨询和生育指导。
1 Roesch K,Curran SP,Tranebjaerg L,et al.Human deafness dystonia syndrome is caused by a defect in assembly of the DDP1/TIMM8a-TIMM13 complex.Hum Mol Genet,2002,11:477-486.
2 Rendtorff ND,Karstensen HG,Lodahl M,et al.Identification and analysis of deletion breakpoints in four Mohr-Tranebjærg syndrome(MTS) patients.Sci Rep,2022,12:14959.
3 Wang H,Wang L,Yang J,et al.Phenotype prediction of Mohr-Tranebjaerg syndrome(MTS) by genetic analysis and initial auditory neuropathy.BMC Med Genet,2019,20:11.
4 Neighbors A,Moss T,Holloway L,et al.Functional analysis of a novel mutation in the TIMM8A gene that causes deafness-dystonia-optic neuronopathy syndrome.Mol Genet Genomic Med,2020,8:e1121.
5 高儒真,樊悦,范欣淼,等.罕见Mohr-Tranebjaerg综合征家系遗传学分析.罕见病研究,2023,2:50-54.
6 Shaker M,Lorigiano TH,Vadlamudi A.Xq22.1 contiguous gene deletion syndrome of X-linked agammaglobulinemia and Mohr-Tranebjærg syndrome.Ann Allergy Asthma Immunol,2016,116:578-579.
7 Szaflarska A,Rutkowska-Zapa a M,Gruca A,et al.Neurodegenerative changes detected by neuroimaging in a patient with contiguous X-chromosome deletion syndrome encompassing BTK and TIMM8A genes.Cent Eur J Immunol,2018,43:139-147.
a M,Gruca A,et al.Neurodegenerative changes detected by neuroimaging in a patient with contiguous X-chromosome deletion syndrome encompassing BTK and TIMM8A genes.Cent Eur J Immunol,2018,43:139-147.
8 Mohr J,Mageroy K.Sex-linked deafness of a possibly new type.Acta Genet Stat Med.1960,10:54-62.
9 Tranebjaerg L,Schwartz C,Eriksen H,et al.A new X linked recessive deafness syndrome with blindness,dystonia,fractures,and mental deficiency is linked to Xq22.J Med Genet,1995,32:257-263.
10 Tranebjaerg L,Schwartz C,Eriksen H,et al.A new X linked recessive deafness syndrome with blindness,dystonia,fractures,and mental deficiency is linked to Xq22.J Med Genet.1995,32:257-263.