先天性凝血因子VII(coagulation factor VII,FVII)缺乏症是常染色体隐性遗传病[1],也是出血性疾病中最常见的一种,由 FVII 基因的异质性突变引起,FVII 完全缺乏症会导致围产期死亡,从危及生命的颅内出血到轻微的粘膜出血。患者的 FVIIc 水平差异不大,却可观察到多种出血症状,杂合子病例常无明显的出血症状,而纯合子病例则可能伴有重度出血表现[2]。FVII缺乏症的相关研究多以成人为主,而妊娠合并 FVII缺乏症相对少见,并发产后大出血的病例更是罕见。现报告1例妊娠合并严重纯合子遗传性FVII缺乏症并产后大出血病例的诊治经过并复习相关文献,以期提高临床医生对此类疾病的认识。
病例报告
患者女,30岁,因“停经9月余,发现凝血功能异常半年”于2022年6月27日收住院。患者15岁月经初潮,4/28天,量中、色正常,无痛经及血凝块史,白带量、色正常,无异味。孕2产1,2017年顺产一活男婴,现体健,末次月经(last menstrual period,LMP):2021年10月05日,预产期(expected date of childbirth,EDC):2022年07月12日。患者停经40余天自测尿酶标阳性并经B超确认怀孕。孕早期恶心、呕吐等早孕症状轻,无药物、毒物及放射线接触史,停经4月余自觉出现胎动至今,孕中晚期无头痛、头晕及胸闷等症状。孕期定期产检,NT、系统超声未见明显异常,唐筛提示:唐氏综合症风险率1:1579、18三体1:6286临界风险,后未行进一步检查,葡萄糖定量试验(oral glucose tolerance test,OGTT)未做。患者孕后期产检发现铁蛋白低,遂服用多糖铁复合物胶囊治疗至今。患者孕3月(2022年1月3日)于临夏州妇幼保健院产检发现纤维蛋白原(Fibrin,FIB)0.3 g/L,遂就诊于兰大一院(2022年1月10日)复查纤维蛋白原 FIB0.49 g/L,建议查找原因。患者于2022年5月19日就诊于我院血液科查凝血因子全套提示:凝血因子C(FIIC):78%(79~131),FVIIC154(50~129)诊断为“原发性血小板减少症”;2022年6月11日患者就诊于我科门诊复查FVIIC163(50~129),常规止凝血:FIB:0.59 g/L,凝血时间(thrombotic time,TT):28.5 s(10.3~17.6),2022年6月20日因“白细胞减少”就诊于血液科FVIIC166%(50~129),血栓弹力图:R3.9(5.0~10.0),K3.6(1.0~3.0),DIC:FIB:0.50 g/L,TT:28.4 s(10.3~17.6)AT-III:81%(83~128)尿干化学分析:vitc:2;血常规:MPV:11.40 fl(6.0~)。2022年6月27日患者于血液科复诊,血栓弹力图:MA(血块硬度)71.0,考虑系低纤维蛋白原血症,建议入院治疗。孕期无口腔、牙龈出血,无皮肤瘀点、瘀斑,无头晕、乏力,现为求进一步诊治遂就诊于我院,入院完善化验及检查:纤维蛋白原FIB 0.5 gL、凝血因子FVII活性166%、血栓弹力图:R 3.9 min、K 3.6 min;肝胆胰脾双肾超声未见明显异常;B超提示:宫内妊娠,单活胎,头位(ROA),胎盘II级;脐绕颈一圈(双顶径:8.6 cm,头围:31.8 cm,腹围:33.2 cm,股骨长:7.7 cm,胎儿心率132次分,羊水最大深度:4.6 cm,羊水指数:10.8 cm,羊水透声好,脐动脉SD:2.02,胎盘附着于子宫前壁)。患者近期无明显诱因出现下腹部发紧发硬,无阴道流血流液,我科以“1.妊娠合并凝血功能异常;2.孕37周+6,G2P1,ROA”收住。患者孕期神清、精神可,饮食睡眠可,二便正常,体重渐增。
诊疗经过
入院予纤维蛋白原(1 g)输注治疗,效果欠佳。2022 年 6 月28日请血液科会诊:患者G2P1,母、弟、子均系低纤维蛋白原血症,不排外先天性低纤维蛋白原血症建议基因检测,患者及家属拒绝,考虑无出血表现建议继续补充纤维蛋白原纠正TT,监测DIC。于6月29日(入院第2天) 开始连续或间断输入纤维蛋白原等血液制品,次日复查凝血功能并分别于2022年07月04日、07月09日输注FIB 1克(复查结果见表 1)。7月1日再次请血液科会诊评估,意见为:完善遗传学检测、动态监测弥散性血管内凝血(disseminated intravascular coagulation,DIC),必要时予以纤维蛋白原、冷沉淀等补充治疗,完善胎儿血管彩色超声示:宫内妊娠,单活胎,头位(ROA),胎盘IIIA级,胎儿脐绕颈1圈。向患者及家属告知病情考虑行COOK球囊促宫颈成熟、缩宫素引产。2022年07月09日硬膜外麻醉下患者经阴道分娩一3 035 g活男婴,Apgar评分10分,同时行人工剥离胎膜术,对合完整后予缩宫素10 u维持+麦角新碱宫颈注射+卡贝缩宫素1支静推治疗,共计出血约300 mL。7月12日(入院第16 天)患者恢复良好出院。出院后随访新生儿无凝血功能障碍及凝血因子异常,产妇分别于产后 42日、3月进行随访,一般状况良好,无出血症状。
表1 不同时间凝血功能及 FIB检查结果
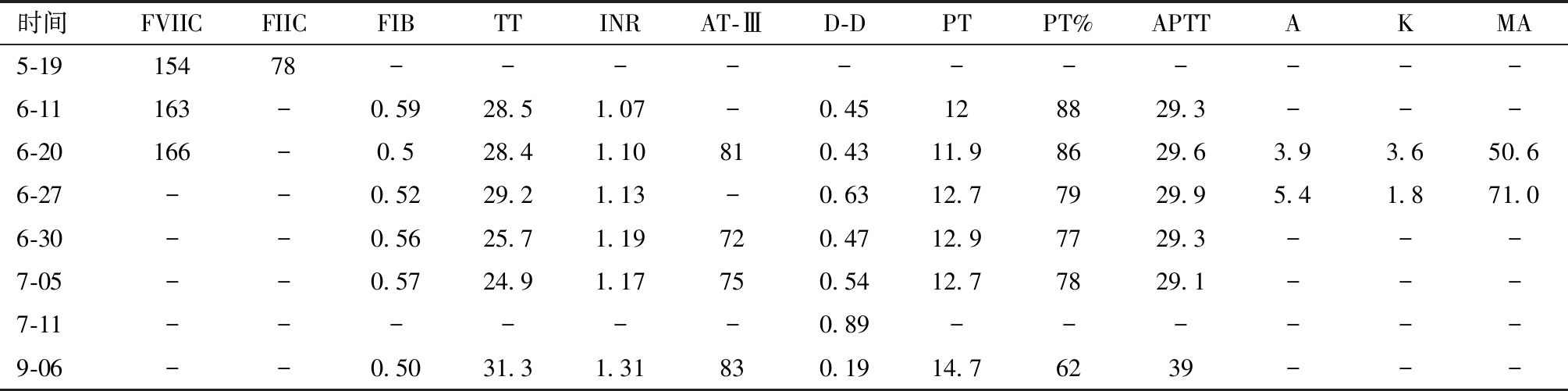
注:“-”代表无数值。FVIIC 纤维蛋白原VII,FIIC纤维蛋白原II,FIB纤维蛋白原,PT 凝血酶原时间,PT% 凝血酶原活动度,INR 国际标准化比值,APTT 活化部分凝血活酶时间,TT 凝血酶时间,AT-Ⅲ 抗凝血酶Ⅲ,D-D D-二聚体,R反应时间,K凝固时间,MA最大振幅。
时间FVIICFIICFIBTTINRAT-ⅢD-DPTPT%APTTAKMA5-1915478-----------6-11163-0.5928.51.07-0.45128829.3---6-20166-0.528.41.10810.4311.98629.63.93.650.66-27--0.5229.21.13-0.6312.77929.95.41.871.06-30--0.5625.71.19720.4712.97729.3---7-05--0.5724.91.17750.5412.77829.1---7-11------0.89------9-06--0.5031.31.31830.1914.76239---
讨论
FVII是一种由肝细胞产生的大小为50 kDa的依赖维生素K的丝氨酸蛋白酶,前体FVII蛋白有461个氨基酸,其中20个氨基酸作为信号肽被去除,40个氨基酸作为前肽被去除,成熟的401个残基蛋白质的相对分子质量为50kDa。羧化的GLA结构域包含 10个Gla 残基。FVII 在仅有 17 个氨基酸的极短活化肽中的Arg 152 处发生一次裂解而可被多种凝血蛋白酶和复合物激活(包括 FXa 和凝血酶),激活的FVIIa 由一条轻链和一条重链组成[3,4]。妊娠期间,凝血状态发生变化,表现为促凝活性增加(表现为因子 VII、因子 VIII、因子 X 和纤维蛋白原水平升高),抗凝活性降低(表现为纤维蛋白溶解和蛋白S活性降低),从而导致高凝状态[1]。因此,在一定程度上FVII可以预测PPH[5]。
FVII缺乏症可分为遗传性FVII缺乏症(inherited factor VII deficiency)及获得性FVII缺乏症(acquired factor VII deficiency)。先天性VII因子缺乏症是一种罕见的常染色体隐性遗传疾病,循环中的 FVIIa 约占血液中FVII总量的 1%。FVII 的编码基因位于第13号染色体的长臂上,与两个与维生素K依赖性蛋白/凝血因子有关的基因即因子 X(FX)和 PROZ(蛋白 与维生素 K 依赖性血浆糖蛋白相邻,FVII 缺乏症的发生是由于编码 FVII 的基因发生了突变,目前已发现 250 多种致病基因突变[6]。其特征是 FVII 活性水平降低,同卵型低于10%,异卵型为 20-60%,其与不同的出血表现有关,患有这种凝血功能障碍的患者在分娩时可能会有出血风险[7,8]。然而FVII缺乏症与出血表型之间的相关性很低[9],临床上妇女可能会出现大量月经出血,并由此导致缺铁性贫血、产后出血和出血性卵巢囊肿等[7]。
产后出血是产妇死亡的主要原因,凝血功能异常属于病因之一。FVII活性的实验室检测是FVII缺乏症诊断的一线方法,有助于结合临床病史管理患者,其他检测包括FVII免疫测定和基因检测[10]。本研究患者异常的凝血因子及明显的家族遗传提供了临床诊断依据。目前对于 FVII缺乏症的产科管理仍存在巨大挑战,其诊治多依赖于有限的病例报道和经验治疗,重点是提高血浆 FVII浓度。本例患者及早识别并评估分娩风险,预防性使用凝血因子替代疗法规避了出血风险。轻度出血的一线治疗主要是使用非特异性止血剂,如 DDAVP ©、氨甲环酸和激素类药物,但在病情较重、出血严重或对一线药物无效时,可能需要使用特异性因子替代品和/或血液制品作为二线治疗7。目前对于 FVII缺乏症患者的管理并无明确的指导方针,患者的治疗方式主要取决于 FVII 水平、出血发作的类型以及病情的严重程度等方面。尽管 FVII缺乏症在妊娠期极为罕见,但并发产后出血风险较高,在临床工作中应当重点关注 FVII缺乏症患者凝血因子变化特点及临床出血风险。错误或延误治疗可能增加患者死亡风险,应早期诊断、及时治疗及严密监测,尽可能改善不良妊娠结局,但具体的管理和诊疗方案尚无明确指南,仍需进一步探索。
1 Yoon HJ.Coagulation abnormalities and bleeding in pregnancy:an anesthesiologist′s perspective.Anesth Pain Med(Seoul),2019,14:371-379.
2 Bernardi F,Mariani G.Biochemical,molecular and clinical aspects of coagulation factor VII and its role in hemostasis and thrombosis.Haematologica,2021,106:351-362.
3 Winter WE,Greene DN,Beal SG,et al.Clotting factors:Clinical biochemistry and their roles as plasma enzymes.Adv Clin Chem,2020,94:31-84.
4 Batsuli G,Kouides P.Rare coagulation factor deficiencies(factors VII,X,V,and II).Hematol Oncol Clin North Am,2021,35:1181-1196.
5 Charbit B,Mandelbrot L,Samain E,et al.The decrease of fibrinogen is an early predictor of the severity of postpartum hemorrhage.J Thromb Haemost,2007,5:266-273.
6![]() A,Gęca T,Soko
A,Gęca T,Soko owska B,et al.Thromboelastometry as an ancillary tool for evaluation of coagulation status after rFVIIa therapy in a pregnant woman with severe hypoproconvertinemia-A case series and review of the literature.Int J Environ Res Public Health,2022,19:10918.
owska B,et al.Thromboelastometry as an ancillary tool for evaluation of coagulation status after rFVIIa therapy in a pregnant woman with severe hypoproconvertinemia-A case series and review of the literature.Int J Environ Res Public Health,2022,19:10918.
7 Winikoff R,Scully MF,Robinson KS.Women and inherited bleeding disorders - A review with a focus on key challenges for 2019.Transfus Apher Sci,2019,58:613-622.
8 Loddo A,Cornacchia S,Cane FL,et al.Prophylaxis of peripartum haemorrhage using recombinant factor VIIa(rfVIIa) in pregnant women with congenital factor VII deficiency:A case report and literature review.Eur J Obstet Gynecol Reprod Biol,2019,235:77-80.
9 Robinson KS.An overview of inherited factor VII deficiency.Transfus Apher Sci,2019,58:569-571.
10 Sevenet P,Kaczor DA,Depasse F.Factor VII deficiency:from basics to clinical laboratory diagnosis and patient management.Clinical and applied thrombosis/hemostasis,2017,23:703-710.