子宫内膜癌是发达国家最常见的妇科恶性肿瘤之一[1], 2020年,在北美、中欧和东欧地区子宫内膜癌的累积风险最高,在南非和亚洲国家,发病率的增长甚至更快[2-3]。在过去二十年中,全年龄组的发病率都增加了20倍,欧洲和北美的发病率比低收入国家更为突出[4]。
肥胖、糖尿病、高血压、雌激素暴露等是公认的子宫内膜癌发生发展的高危因素[5-6],但其确切的病因及发病机制尚不清楚,多认为是多基因调控的复杂过程,由于细胞增殖和凋亡失衡,导致子宫内膜上皮向恶性转化[7]。
锌指蛋白(zinc fingerprotein,ZNF)是一类具有手指状结构域的转录因子,人类基因组中可能有近1%的序列编码含有锌指结构的蛋白[8],在细胞分化、胚胎发育、基因的表达调控等方面都具有重要作用。ZNF695是ZNF C2H2家族中的一员,包含Krüpple相关盒(KRAB)结构域,其特征在于识别基因抑制因子[9]。在人类或其他物种正常组织中几乎没有发现它的存在。有学者对癌症基因组图谱(the cancer genome atlas,TCGA)数据库中肝癌的DNA甲基化和基因表达数据进行分析,发现ZNF695在肝癌中呈差异化表达,在cpg位点或cpg岛(cgi)水平上表现出DNA甲基化的变化[10];外显子全基因组微阵列分析显示,ZNF695是与卵巢癌相关的具有不同外显子分布的过表达基因,并推测其可能激活细胞增殖,从而导致细胞向恶性转化[11]。
子宫内膜癌细胞可通过多种信号通路或分子蛋白来调控细胞的增殖和凋亡,细胞周期蛋白依赖性激酶(cyclin-dependent kinases,CDK)及细胞周期蛋白依赖性激酶抑制剂(cyclin-dependent kinase inhibitors,CDKI)家族等则是常见的与细胞增殖相关的蛋白。而进展期肿瘤细胞向原位侵袭或远处转移则需要短暂或稳定的进行上皮-间质细胞转化(epithelial-mesenchymal transition, EMT)[12],E-cadherin及vimentin常被共同用作EMT的标志物来反应其发生过程。
ZNF695在子宫内膜癌中的研究尚未见相关报道,尚不清楚其与细胞增殖、EMT等变化的相关性。本研究结合生物信息分析的结果,拟在正常人子宫内膜及子宫内膜癌组织中检测ZNF695的表达情况,并观察ZNF695表达下调后癌细胞增殖、侵袭迁移能力的变化,通过检测ZNF695表达下调后E-cadherin、P21、MMP2、Vimentin的表达情况,了解ZNF695参与子宫内膜癌进展的可能机制。
材料和方法
一、实验材料
1.组织学样本、细胞样本:组织学样本来自2014至2016年湖北省麻城市人民医院妇产科手术或活检后保存完好的子宫内膜癌和正常子宫内膜组织标本共64例,其中子宫内膜癌组织44例,均为腺癌;正常子宫内膜组织20例,所有标本均再次请病理科确认病理学诊断。所有患者均为初次手术,子宫内膜癌患者术前未接受放化疗或激素治疗。标本由病理科常规甲醛固定、石蜡包埋并制成5 um厚的切片。
细胞样本为保存于华中科技大学同济医学院妇科实验室的Ishikawa(ISK)及HEC-1B细胞株。
二、方法
1.免疫组化:将标本石蜡包埋切片后,将所要做的指标ZNF695标记在切片上,并置于65℃烤箱中烘片2 h。取出切片,依次放入二甲苯Ⅰ、二甲苯Ⅱ各20 min,无水乙醇Ⅰ、无水乙醇Ⅱ各10 min,95%酒精、90%酒精、80%酒精、70%酒精各5 min,蒸馏水洗。经过PBS洗,H2O2封闭、修复等过程,最后加一抗、二抗显色复染,再将玻片架依次经过两次95%酒精、两次无水乙醇、两次二甲苯各5 min脱水透明,切片稍晾干后中性树胶封片,将封固好的切片晾干后于显微镜下观察,采集典型图像。
2.应用蛋白免疫印迹测P21、MMP2、E-cadherin、vimentin蛋白表达:设置正常对照组(细胞株)或空载体组细胞、转染效率最高的实验组细胞,冰上裂解、离心。将浓度为500 ug/mL的标准蛋白按0,1,2,4,8,12,16,20 uL的体积加入96孔板中,用PBS溶液将各孔体积补充至20 uL;取样品蛋白2 uL加入样品孔,PBS补足至20 uL,每个样品设4个复孔;计算需要加入的裂解液和蛋白上样缓冲液体积;配置凝胶;根据每个样品总蛋白的量计算每个样品具体的上样量进行电泳转膜,最后孵育一抗二抗并ECL显影。
3.Transwell小室迁移实验:取对数生长的细胞,制备细胞悬液并稀释至密度为1.5×105/mL,取200 uL加入上室,下室则加入600 uL含20%胎牛血清的培养基,每组设4个复孔,培养箱中培养24 h;取出小室用棉签轻轻擦拭上层后PBS冲洗滤膜3遍,下室加入甲醛600 uL固定,15 min后弃去甲醛,加入2%结晶紫甲醇溶液,15 min后冲洗结晶紫溶液,显微镜下观察迁移细胞数量。
4.CCK8增殖实验:取对数生长的两种细胞系细胞分别种于6孔板上;培养细胞长至80%~90%左右时处理形成悬液,计数确定浓度,以每孔4 000个细胞浓度接种于96孔板上,每孔100 uL,每组4个复孔;种板后在24,48,72,96 h时,分别在各时间点向各组加入CCK8 10 uL,孵育后计算细胞的增殖能力。实验重复三次。
5.结果判读:ZNF695染色以子宫内膜腺上皮细胞膜、胞浆或胞核出现棕黄颗粒或团块为阳性标准。在高倍镜下随机选取5个不同视野计算腺上皮细胞总数及阳性细胞数,阳性细胞所占比例小于10%为阴性,大于等于10%则为阳性。
6.统计学处理:应用SPSS19.0统计软件对数据进行分析,计数资料采用卡方检验,组间差异采用t检验。P<0.05表示差异有统计学意义。
结 果
一、生信分析
通过搜索CRN(Cancer RNA-Seq Nexus)网站发现ZNF695在子宫内膜癌中的表达明显高于正常内膜组织,如图1。并在Oncolnc网站上搜索子宫内膜癌中ZNF695的表达并绘制生存曲线,高表达者预后差(P=0.0243),见图2。
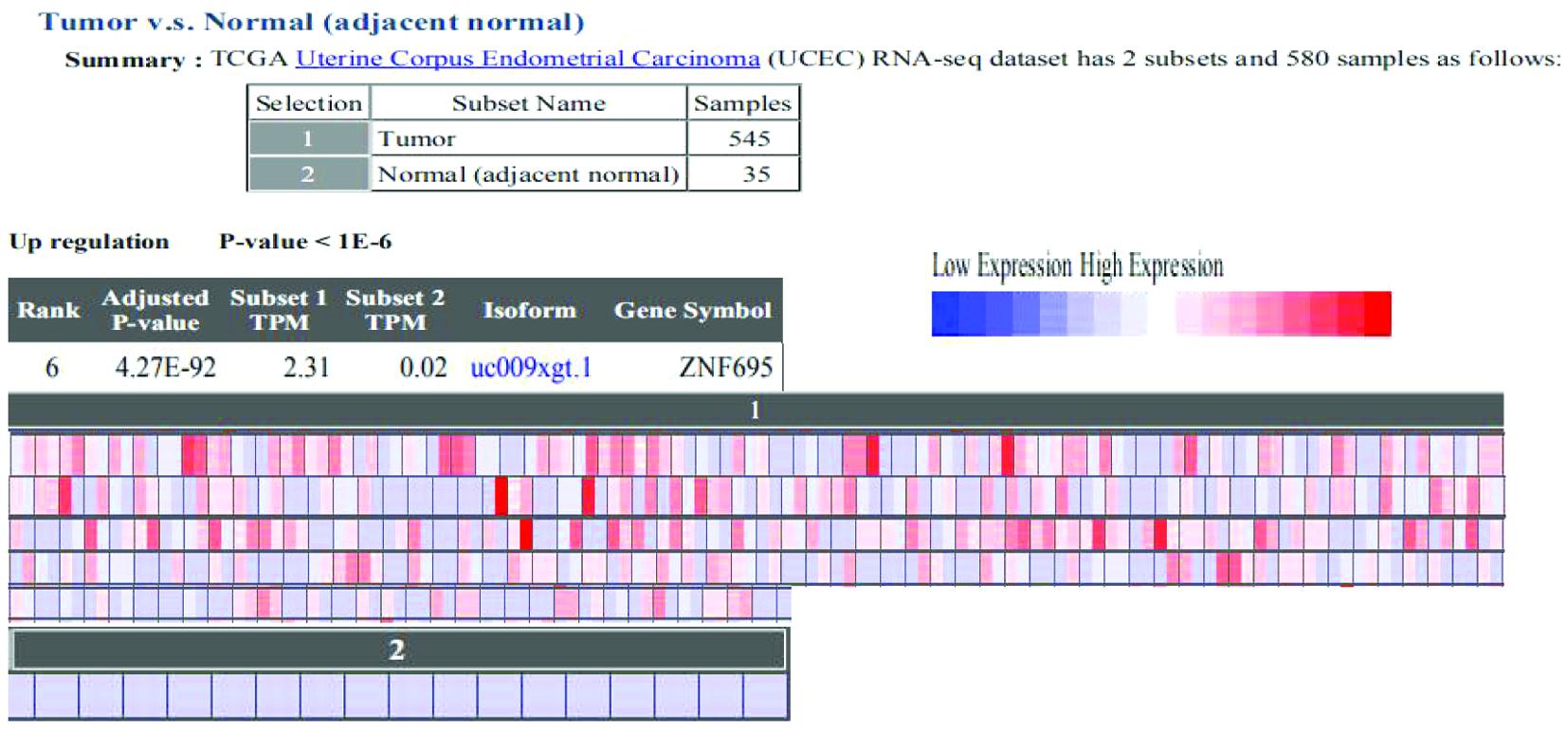
图1 ZNF695在子宫内膜癌中的表达
Figure 1 Expression of ZNF695 in Endometrial Cancer
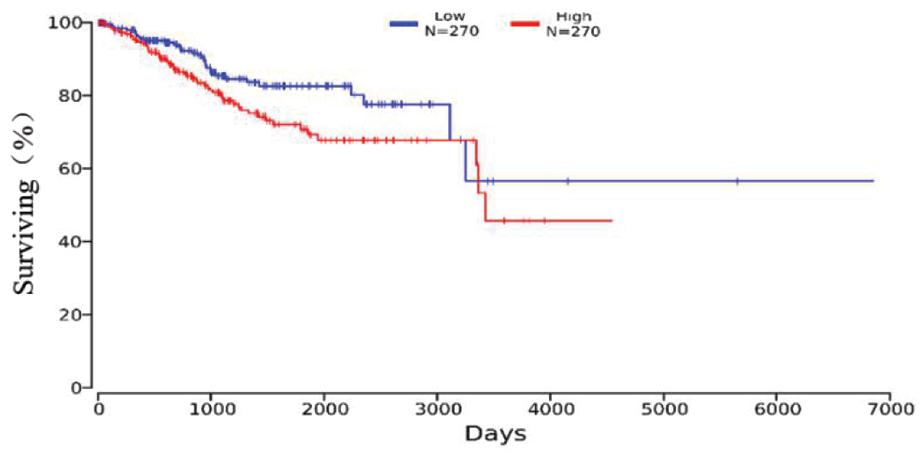
图2 ZNF695的表达与子宫内膜癌预后的关系
Figure 2 Association of the expression of ZNF695 and the prognosis of endometrial cancer
二、ZNF695蛋白在正常子宫内膜及子宫内膜癌组织中的表达
ZNF695蛋白着色主要定位于细胞膜,其在子宫内膜癌中的阳性表达率(47.7%,21/44)高于正常子宫内膜组(10.0%,2/20),差异具有统计学意义,见表1。校对子宫内膜癌的病理类型后,再次统计分析显示组间并无显著差异(P=0.071)。
表1 ZNF695在不同病理类型子宫内膜组织中的表达
Table 1 Expression of ZNF695 in endometrial tissues by different pathological type
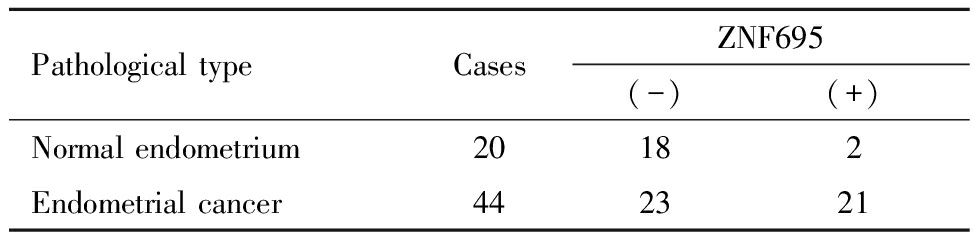
Pathological typeCasesZNF695(-)(+)Normal endometrium20182Endometrial cancer442321
三、ISK、HEC-1B细胞中ZNF695基因表达水平
将针对ZNF695基因的shRNA转入ISK、HEC-1B细胞中,结果显示,两种细胞系中ZNF695基因的表达较阴性对照(空载体组)显著降低(P=0.0002/0.0346),且在两种细胞系中,ZNF695-71516组的抑制效率均较明显,遂根据ZNF695-71516序列构建包装慢病毒质粒。
四、ISK、HEC-1B细胞中慢病毒转染质粒转染
将根据PCR筛选出的ZNF695-shRNA序列构建的慢病毒质粒转染两种细胞系48 h后,荧光显微镜下观察,可见各组的荧光表达信号均较强。分别提取两种细胞系中ZNF695干扰组及vector组的总蛋白,利用western blot法定量分析E-cadherin、Vimentin、P21、MMP2的蛋白表达。结果发现,HEC-1B细胞中E-cadherin及P21蛋白表达下降明显,Vimentin表达上升,差异有统计学意义,但ISK细胞中仅E-cadherin的表达下降显著,MMP2蛋白的表达变化无明显差异。见图3。
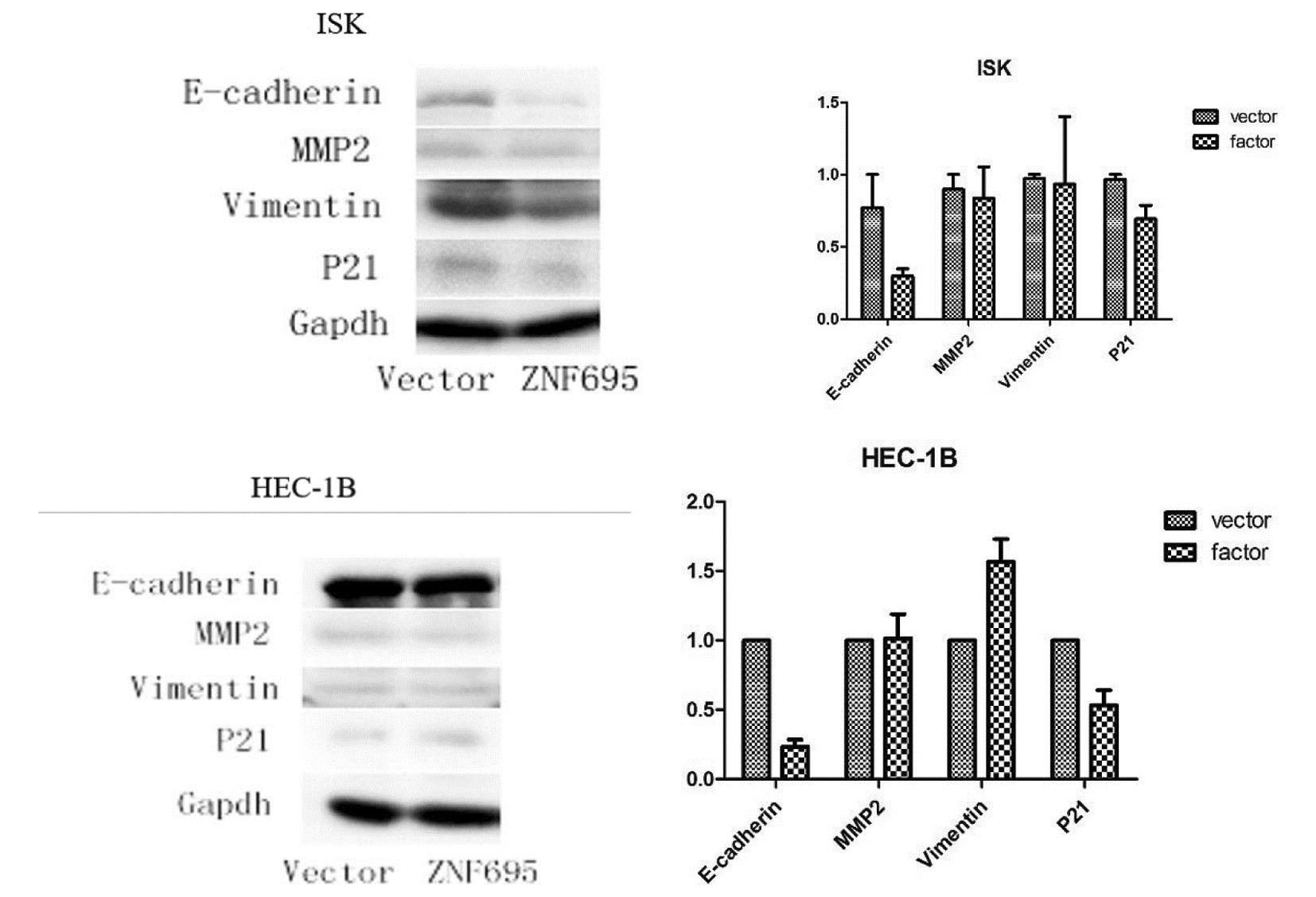
图3 ZNF695下调后与空载体组比较E-cadherin、MMP2、Vimentin、P21蛋白的表达变化
Figure 3 Comparison of the expression changes of E-cadherin, MMP2, Vimentin, and P21 proteins after downregulation of ZNF695 compared to the control vector group
五、ZNF695对细胞体外迁移能力的影响
运用transwell小室法检测经慢病毒转染的ZNF695干扰组与空载体组(vector)ISK、HEC-1B细胞细胞体外迁移能力。转染48 h后,两种细胞系中ZNF695干扰组的穿膜数较空载体组明显增多,差异有统计学意义 ,见图4。
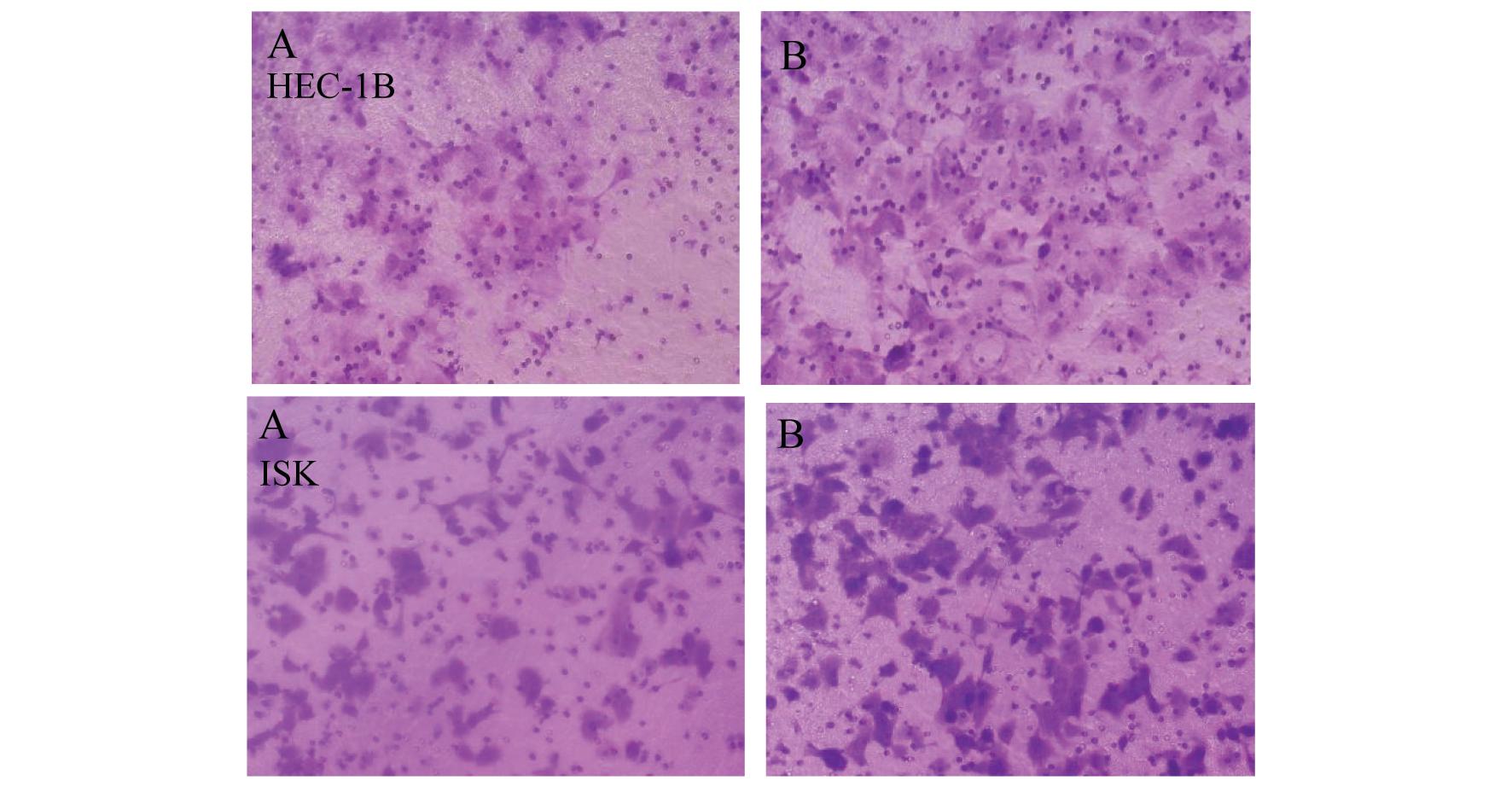
A:Vector group;B:ZNF695 interference group
图4 ZNF695表达下调后细胞迁移能力的变化(染色×200)
Figure 4 Changes in cell migration ability after downregulation of ZNF695 expression (staining under × 200 magnification times)
六、ZNF695对细胞体外增殖能力的影响
运用CCK8增殖实验检测ISK、HEC-1B细胞中干扰ZNF695表达后干扰组与空载体组(vector)细胞增殖能力的影响。48 h后,干扰组细胞的增殖能力较空载体组增强,两组比较差异有统计学意义。
讨 论
ZNF695是一种锌指蛋白,虽然目前人们对它了解不多,最接近的同系物也仅有64%的同源性[9],但它很可能是一种转录因子,ZNF695蛋白可能调节通过治疗如放疗、顺铂等引入的DNA修复相关基因的表达,亦可能由于改变多个基因的甲基化从而导致ZNF695的甲基化,这种改变对肿瘤细胞在最终的放化疗中存活至关重要[13]。Ke等[14]发现,ZNF695是前列腺癌放疗耐药性的重要标志物,与前列腺癌症细胞的增殖、侵袭和迁移密切相关,可能是影响前列腺癌微环境的重要因素[14-15]。Takahashi等[13]发现ZNF695的甲基化是影响食管鳞状细胞癌化疗耐药性的重要因素。一些研究还发现,ZNF695与乳腺癌[16]及卵巢癌[11]的预后密切相关。这些结果充分表明ZNF695与许多肿瘤的预后密切相关,并可能在恶性肿瘤的微环境中发挥重要作用。但以上均为推测的ZNF695与疾病相关的可能机制,目前尚无实际研究证明其在疾病的发生发展尤其是肿瘤中的作用,本实验以生物信息学的分析结果为基础研究了ZNF695与子宫内膜癌的相关性。
本研究通过CRN及Oncolnc网站发现ZNF695在子宫内膜癌中高表达,且与预后相关,并经过免疫组化证实了ZNF695的高表达,结果表明,ZNF695在内膜癌中的表达率为47.7%,明显高于正常内膜组织的10.0%,且差异有统计学意义,与生信分析结果一致。为了了解其在子宫内膜癌侵袭转移中的作用,本研究通过短发夹RNA干扰子宫内膜癌ISK及HEC-1B细胞中ZNF695蛋白的表达,结果转染后癌细胞的增殖迁移能力明显下降,同时,基于其可促进卵巢癌细胞增殖作用[11]的推测,初步探索ZNF695蛋白对P21、MMP2表达的调控作用;此外,为探究其是否与EMT有关,同时分析了其对E-cadherin及Vimentin蛋白的调控,结果ZNF695表达的下调同时伴有P21、E-cadherin的下调及Vimentin的上调,而MMP2则无明显影响,细胞实验提示子宫内膜癌中ZNF695可致肿瘤增殖能力降低并能抑制上皮-间质转化从而降低癌细胞的侵袭能力,其可能是通过调节P21、E-cadherin及Vimentin的表达来实现。根据以上细胞实验结果可知,ZNF695在子宫内膜癌中呈低表达,与免疫组化结果不一致,考虑ISK及HEC-1B分别为高分化及中分化腺癌细胞,因此在免疫组化中排除低分化的组织标本10个(8个阴性,2个阳性)后再次行卡方检验,结果显示ZNF695的表达在癌组织及正常组织中并无明显差异(P=0.071),而由于免疫组化中抗体效价、浓度、抗原修复、组织切片质量、染片等均会影响最终结果导致假阳性或假阴性,且本次实验中所用标本收集于2014至2016年,时间跨度大,其中有少数细胞碎片较多的石蜡片,不排除石蜡切块标本本身的影响导致免疫组化结果出现偏差。
综上所述,从细胞实验可推测ZNF695的表达与子宫内膜癌细胞的增殖迁移能力有关,本研究构建的ZNF695 shRNA稳定下调了细胞中ZNF695的表达,体外增殖、迁移实验结果显示,下调ZNF695的表达后子宫内膜癌ISK、HEC-1B细胞的增殖、迁移能力明显增强,但既往并无其在子宫内膜癌中的表达及作用机制的研究,且本实验中细胞实验与组织实验结果有一定差别,后续仍需重复免疫组化实验,收集近期的组织标本,排除可疑干扰因素,来验证ZNF695蛋白在子宫内膜癌组织中的表达情况,并扩大组织样本量,研究ZNF695蛋白表达与子宫内膜癌临床病理特征及生存预后的相关性,同时进一步探索其在子宫内膜癌增殖、迁移及促上皮-间质转化中的具体调节途径。
1 Torre LA,Bray F,Siegel RL,et al.Global cancer statistics,2012.CA Cancer J Clin,2015,65:87-108.
2 Kodada D,Hyblova M,Krumpolec P,et al.The Potential of Liquid Biopsy in Detection of Endometrial Cancer Biomarkers:A Pilot Study.Int J Mol Sci,2023,24:7811.
3 Sung H,Ferlay J,Siegel RL,et al.Global Cancer Statistics 2020:GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries.CA Cancer J Clin,2021,71:209-249.
4 Corr BR,Erickson BK,Barber EL,Fisher CM,Slomovitz B.Advances in the management of endometrial cancer.BMJ,2025,388:e080978.
5 Di Cristofano A,Ellenson LH.Endometrial carcinoma.Annu Rev Pathol,2007,2:57-85.
6 Uharcek P.Prognostic factors in endometrial carcinoma.J Obstet Gynaecol Res,2008,34:776-783.
7 Li Q,Qiu XM,Li QH,et al.MicroRNA-424 may function as a tumor suppressor in endometrial carcinoma cells by targeting E2F7.Oncol Rep,2015,33:2354-2360.
8 Hoovers JM,Mannens M,John R,et al.High-resolution localization of 69 potential human zinc finger protein genes:a number are clustered.Genomics,1992,12:254-263.
9 Friedman JR,Fredericks WJ,Jensen DE,et al.KAP-1,a novel corepressor for the highly conserved KRAB repression domain.Genes Dev,1996,10:2067-2078.
10 Sun XJ,Wang MC,Zhang FH,et al.An integrated analysis of genome-wide DNA methylation and gene expression data in hepatocellular carcinoma.FEBS Open Bio,2018,8:1093-1103.
11 Juárez-Méndez S,Zentella-Dehesa A,Villegas-Ruíz V,et al.Splice variants of zinc finger protein 695 mRNA associated to ovarian cancer.J Ovarian Res,2013,6:61.
12 Colas E,Pedrola N,Devis L,et al.The EMT signaling pathways in endometrial carcinoma.Clin Transl Oncol,2012,14:715-720.
13 Takahashi T,Yamahsita S,Matsuda Y,et al.ZNF695 methylation predicts a response of esophageal squamous cell carcinoma to definitive chemoradiotherapy.J Cancer Res Clin Oncol,2015,141:453-463.
14 Ke ZB,You Q,Chen JY,et al.A radiation resistance related index for biochemical recurrence and tumor immune environment in prostate cancer patients.Comput Biol Med,2022,146:105711.
15 Zhang L,Li Y,Wang X,et al.Five-gene signature associating with Gleason score serve as novel biomarkers for identifying early recurring events and contributing to early diagnosis for Prostate Adenocarcinoma.J Cancer,2021,12:3626-3647.
16 Shinden Y,Hirashima T,Nohata N,et al.Molecular pathogenesis of breast cancer:impact of miR-99a-5p and miR-99a-3p regulation on oncogenic genes.J Hum Genet,2021,66:519-534.