多囊卵巢综合征(polycystic ovary syndrome,PCOS)为妇科内分泌疾病,患者多存在卵巢多囊状态、胰岛素抵抗、糖脂代谢异常、排卵障碍以及继发性不孕症等症状[1]。PCOS的患病率呈逐年上升趋势,影响约5%~15%的育龄期女性,是妇女月经紊乱和排卵障碍性不孕的主要原因[2-3]。不孕症是育龄期PCOS女性最为困扰的问题之一,影响PCOS不孕患者的因素包括年龄、不孕持续时间以及是否具有全身或妇产科基础疾病等[4]。研究表明,不孕症病程对于促性腺激素诱导排卵(gonadotropin-induced ovulation,GND)和宫腔内人工授精(intrauterine insemination,IUI)治疗后活产率具有显著影响[5];此外,有研究指出,随着不孕年限的增加,不孕患者的欲望、唤醒、润滑、性高潮、疼痛等得分显著降低,对于不孕女性性生活产生负面影响[6]。目前多数研究旨在探讨不同不孕症病程的PCOS不孕患者妊娠结局及生活质量,鲜少有研究关注于其临床生化特征。因此,本研究针对于PCOS不孕症患者,根据其不孕症病程的长短进行分组,以探讨其临床生化特征,以期为临床研究提供理论依据。
资料与方法
1.病例来源及分组:本研究病例来源于“针刺和克罗米芬对多囊卵巢综合征无排卵妇女活产的影响”项目,这是一项针对于不孕症的大型随机对照实验,于2011年至2015年在中国多家医院分中心进行,样本量巨大[7]。本研究共纳入948例确诊为不孕症的患者,根据其不孕症病程的不同,对PCOS不孕症患者进行基线特征分析,按照其不孕症病程长短将其分为<12个月组(n=127例)、12≤~<36个月组(n=598例)和≥36个月组(n=223例)。纳入标准包括(1)依据鹿特丹标准(2003年修订)[8]确诊为PCOS;(2)年龄在20~40岁;(3)伴有排卵障碍性不孕;(4)丈夫精液常规结果在正常范围内;(5)签署知情同意书。排除标准包括(1)患有其他内分泌疾病;(2)夫妻双方因其他原因导致不孕症;(3)90 d内使用其他药物或激素;(4)45 d内存在流产、妊娠、分娩及哺乳者。
2.观察指标:(1)人体测量学指标。包括年龄、腰臀比(waist-to-hip ratio,WHR)、体质指数(body mass index,BMI)、舒张压、收缩压、子宫内膜厚度、多毛评分、痤疮评分、黑棘皮评分以及左、右卵巢体积。(2)既往生育史。包括初潮年龄、平均月经周期、既往流/引产、异位妊娠、早产。(3)性激素指标。包括黄体生成素(luteinizing hormone,LH)、卵泡刺激素(follicle stimulating hormone,FSH)、 LH/FSH、 孕酮(progesterone,P)、雌二醇(estradiol,E2)、游离睾酮(free testosterone,FT)、总睾酮(total testosterone,TT)、性激素结合球蛋白(sex hormone-binding globulin,SHBG)以及游离睾酮指数(free androgen index,FAI),FAI=TT/SHBG×100。(4)胰岛素及糖脂代谢指标。空腹胰岛素(fasting insulin,FINS)、空腹血糖(fasting blood glucose,FBG)、胰岛素抵抗指数 (homeostatic model assessment of insulin resistance,HOMA-IR)、 总胆固醇(total cholesterol,TC)、低密度脂蛋白(low-density lipoprotein cholesterol,LDL-C)、甘油三酯(triglycerides,TG)、高密度脂蛋白(high-density lipoprotein cholesterol,HDL-C)、载脂蛋白A(apolipoprotein A,ApoA)、 载脂蛋白B(apolipoprotein B,ApoB)以及脂蛋白(lipoprotein,LP)。并判断胰岛素抵抗(insulin resistance,IR)、高脂血症、代谢综合征(metabolic syndrome,MS)的发病比例。其中IR判定标准为HOMA-IR≥2.69,HOMA-IR= FINS(U/L)× FPG(mmol/L)/22.5;高脂血症依据文献[9]判定;MS依据文献[8]判定。
3.统计学处理:采用SPSS 25.0对数据统计分析,符合正态分布的定量数据以![]() 表示,组间比较行单因素方差分析,组内两两比较行LSD法;符合非正态分布的数据以M(P25,P75)表示,组间比较行Kruskal-Wallis H检验。定性数据以例(%)表示,组间比较行卡方检验,组内两两比较采用 Bonferroni法。P<0.05为差异有统计学意义。
表示,组间比较行单因素方差分析,组内两两比较行LSD法;符合非正态分布的数据以M(P25,P75)表示,组间比较行Kruskal-Wallis H检验。定性数据以例(%)表示,组间比较行卡方检验,组内两两比较采用 Bonferroni法。P<0.05为差异有统计学意义。
结果
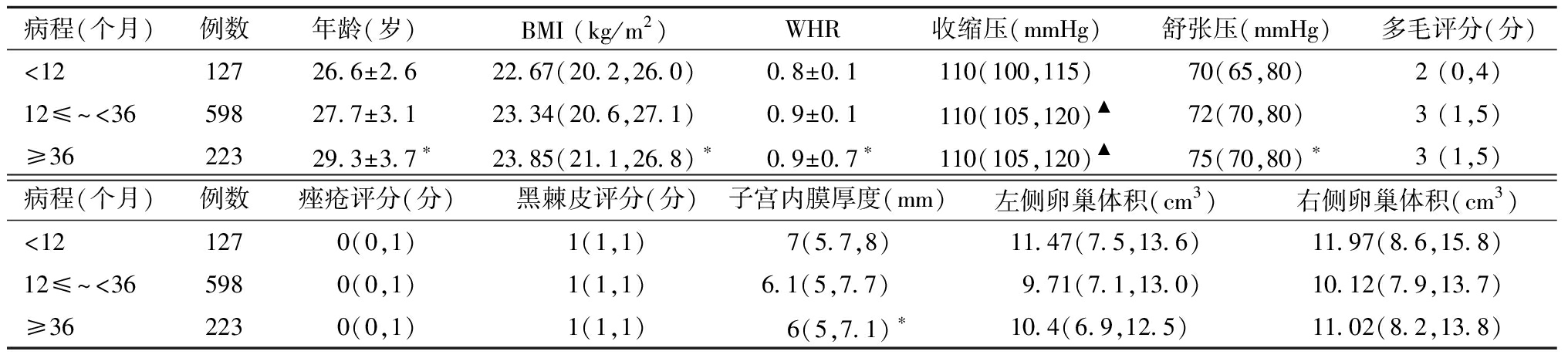
1.不同病程人体测量学指标比较:不孕症病程≥36个月组年龄、BMI、WHR、舒张压均大于不孕症病程<12个月组和12≤~<36个月组(P<0.05),子宫内膜厚度小于不孕症病程<12个月组和12≤~<36个月组(P<0.05),12≤~<36个月、不孕症病程≥36个月组收缩压大于不孕症病程<12个月组(P<0.05),其余指标差异无统计学意义。见表1。
表1 不同不孕症病程的PCOS不孕患者人体测量学指标差异
病程(个月)例数年龄(岁)BMI (kg/m2)WHR收缩压(mmHg)舒张压(mmHg)多毛评分(分)<1212726.6±2.622.67(20.2,26.0)0.8±0.1110(100,115)70(65,80)2 (0,4)12≤~<3659827.7±3.123.34(20.6,27.1)0.9±0.1110(105,120)▲72(70,80)3 (1,5)≥3622329.3±3.7∗23.85(21.1,26.8) ∗0.9±0.7∗110(105,120)▲75(70,80) ∗3 (1,5)病程(个月)例数痤疮评分(分)黑棘皮评分(分)子宫内膜厚度(mm)左侧卵巢体积(cm3)右侧卵巢体积(cm3)<121270(0,1)1(1,1) 7(5.7,8)11.47(7.5,13.6)11.97(8.6,15.8)12≤~<365980(0,1)1(1,1)6.1(5,7.7)9.71(7.1,13.0)10.12(7.9,13.7)≥362230(0,1)1(1,1) 6(5,7.1) ∗10.4(6.9,12.5)11.02(8.2,13.8)
与<12个月组和12≤~<36组比较,*P<0.05;与<12个月组比较,▲P<0.05
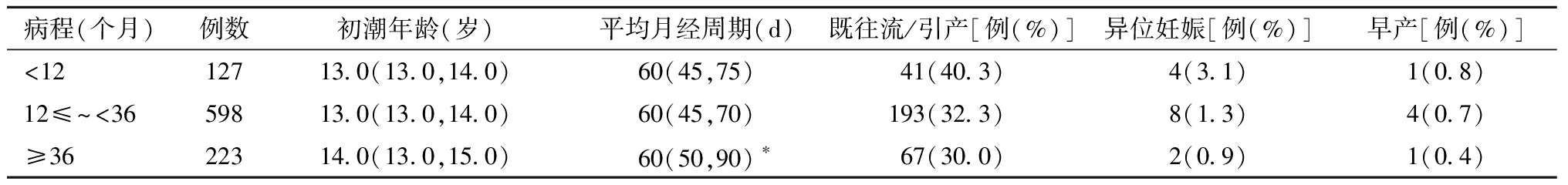
2.不同病程既往生育史差异:同12≤~<36个月组相比,不孕症病程≥36个月组患者的平均月经周期显著增加(P<0.05);其余指标组间差异均无统计学意义。见表2。
表2 不同不孕症病程的PCOS不孕患者既往生育史差异
病程(个月)例数初潮年龄(岁)平均月经周期(d)既往流/引产[例(%)]异位妊娠[例(%)]早产[例(%)]<1212713.0(13.0,14.0)60(45,75)41(40.3)4(3.1)1(0.8)12≤~<3659813.0(13.0,14.0)60(45,70)193(32.3)8(1.3)4(0.7)≥3622314.0(13.0,15.0)60(50,90) ∗67(30.0)2(0.9)1(0.4)
与12≤~<36组比较,*P<0.05
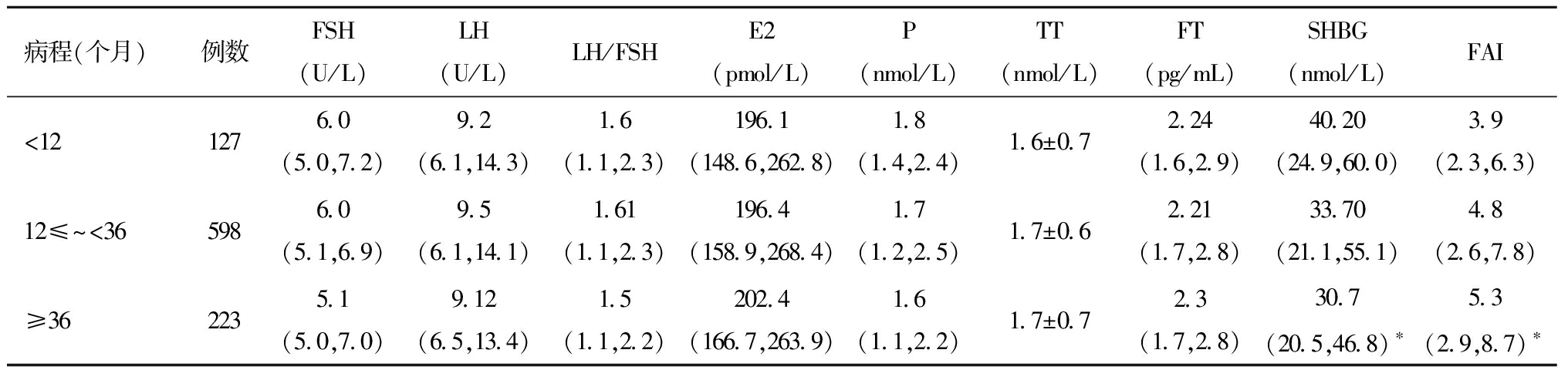
3.不同病程性激素指标差异:不同病程FSH、LH、LH/FSH、E2、P、TT、FT无差异(P>0.05)。不孕症病程≥36个月组SHBG低于<12个月组和12≤~<36个月组(P<0.05),FAI水平高于<12个月组和12≤~<36个月组(P<0.05)。不孕症病程与SHBG水平呈现负相关,与FAI水平呈现正相关,不同病程的TT水平呈现出升高趋势。见表3。
表3 不同不孕症病程的PCOS不孕患者性激素水平差异
病程(个月)例数FSH(U/L)LH(U/L)LH/FSHE2 (pmol/L)P (nmol/L)TT (nmol/L)FT (pg/mL)SHBG(nmol/L)FAI<121276.0 (5.0,7.2)9.2(6.1,14.3)1.6(1.1,2.3)196.1(148.6,262.8)1.8(1.4,2.4)1.6±0.72.24 (1.6,2.9)40.20(24.9,60.0)3.9(2.3,6.3)12≤~<365986.0 (5.1,6.9)9.5 (6.1,14.1)1.61(1.1,2.3)196.4(158.9,268.4)1.7(1.2,2.5)1.7±0.62.21(1.7,2.8)33.70(21.1,55.1)4.8(2.6,7.8)≥362235.1 (5.0,7.0)9.12 (6.5,13.4)1.5 (1.1,2.2)202.4(166.7,263.9)1.6(1.1,2.2)1.7±0.72.3 (1.7,2.8)30.7(20.5,46.8)∗5.3(2.9,8.7)∗
与<12个月组和12≤~<36组比较,*P<0.05
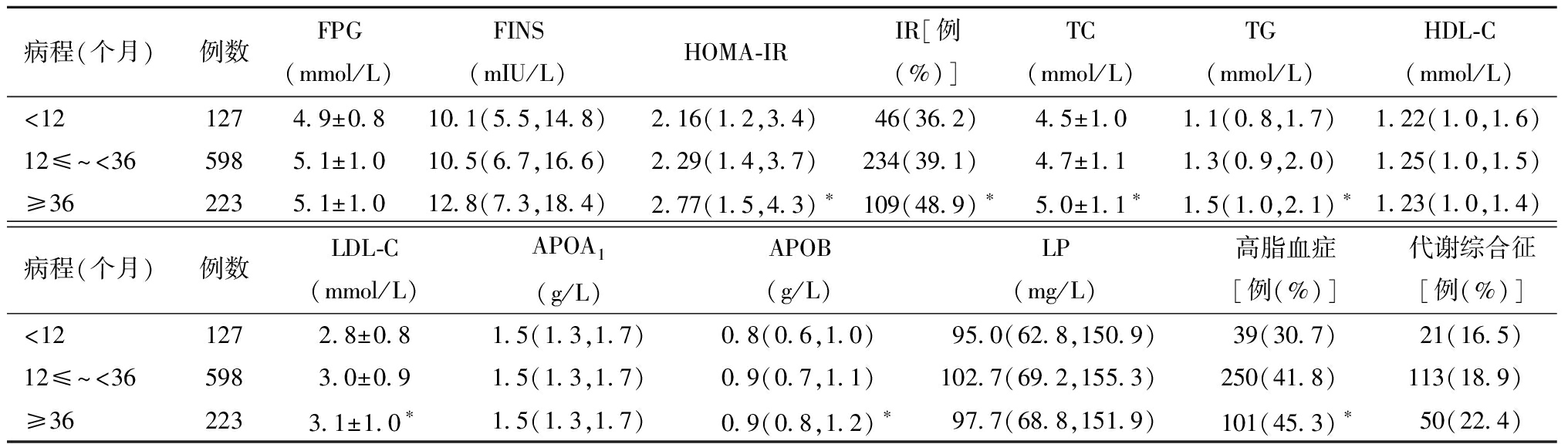
4.不同病程胰岛素及糖、脂代谢差异:不孕症病程≥36个月组的HOMA-IR、TC、TG、LDL-C、APOB均大于<12个月组和12≤~<36个月组(P<0.05),高脂血症、IR患病率高于<12个月组和12≤~<36个月组(P<0.05);不同病程FPG、FINS、HDL-C、APOA1、LP、代谢综合征无差异(P>0.05)。见表4。
表4 三组胰岛素及糖脂代谢差异
病程(个月)例数FPG(mmol/L)FINS(mIU/L)HOMA-IRIR[例(%)]TC(mmol/L)TG(mmol/L)HDL-C(mmol/L)<121274.9±0.810.1(5.5,14.8)2.16(1.2,3.4)46(36.2)4.5±1.01.1(0.8,1.7)1.22(1.0,1.6)12≤~<365985.1±1.010.5(6.7,16.6)2.29(1.4,3.7)234(39.1)4.7±1.11.3(0.9,2.0)1.25(1.0,1.5)≥362235.1±1.012.8(7.3,18.4)2.77(1.5,4.3)∗109(48.9)∗5.0±1.1∗1.5(1.0,2.1) ∗1.23(1.0,1.4)病程(个月)例数LDL-C(mmol/L)APOA1(g/L)APOB(g/L)LP(mg/L)高脂血症[例(%)]代谢综合征[例(%)]<121272.8±0.81.5(1.3,1.7)0.8(0.6,1.0)95.0(62.8,150.9)39(30.7)21(16.5)12≤~<365983.0±0.91.5(1.3,1.7)0.9(0.7,1.1)102.7(69.2,155.3)250(41.8)113(18.9)≥362233.1±1.0∗1.5(1.3,1.7)0.9(0.8,1.2)∗97.7(68.8,151.9)101(45.3)∗50(22.4)
与<12个月组和12≤~<36组比较,*P<0.05
讨论
不孕症的发生是由多种病因导致的生育期夫妇生殖健康不良事件,其主要病因为盆腔因素和排卵障碍,其中排卵障碍性不孕约占女性不孕的25%~35%,而以PCOS为主的卵巢病变是引起排卵障碍性不孕的主要原因[3]。PCOS导致排卵障碍的主要原因是下丘脑-垂体-卵巢(hypothalamic-pituitary-ovary,HPO)轴功能失调,不孕症也是PCOS患者就诊的主要原因之一。本研究主要对PCOS不孕症不同病程患者的基线特点进行探讨,结果表明患者不孕症病程越长,常伴有较为显著的肥胖、高雄激素血症、IR以及高脂血症且月经稀发程度也更为严重。
1.不孕症病程与人体测量学指标:本研究发现,不孕症的病程越长,患者的年龄、BMI、WHR、收缩压、舒张压越高;子宫内膜厚度越薄,这与大多数研究结果具有相似性。研究表明[10-11],超重或者肥胖是导致生殖能力下降和不孕症风险增加的主要原因,BMI指数直接影响女性的生殖结局,BMI越高,生殖结局越差,高BMI与高循环胰岛素水平相关,导致卵巢分泌雄激素水平增加,多余的脂肪组织通过芳香化酶的催化,转化为雌激素,对HPO轴产生负反馈并影响促性腺激素的产生,进而影响排卵和受孕等。BMI水平与不孕症病程呈现正相关,这一结果与国外研究结果相一致,在对计划妊娠的丹麦妇女进行研究发现[12-13],BMI升高与受孕率呈现负相关,BMI影响计划妊娠时间。WHR是中心性肥胖的重要指标,中心性肥胖是慢性低度炎症的关键因素[14],随着不孕症病程的延长,WHR增大,PCOS不孕症患者的慢性低度炎症反应增加,加重PCOS,从而产生恶性循环。在本研究中发现,随着不孕症病程的延长,收缩压和舒张压均有所增加(P<0.05),这与国外的一项研究结果相同,其机制可能与PCOS的高雄激素血症有关[15]。另外,针对于不孕症的治疗也可能会增加高血压的风险[16],提示在针对于不孕症的治疗过程中要关注远期并发症心血管疾病,积极预防未来心血管疾病的发生,针对性地进行体检等。多元Logistic回归分析显示[17],年龄、胚胎质量和子宫内膜厚度是临床妊娠率、活产妊娠率以及持续妊娠率显著影响因素,子宫内膜厚度逐渐增加,自然流产率呈下降趋势。Isaccs等[18]和Weissman等[19]建议在妊娠周期中,将子宫内膜厚度控制在7 mm及以上,以最大限度提高妊娠率,本研究发现,12个月≤不孕症病程<36个月、不孕症病程≥36个月组的患者子宫内膜厚度低于7 mm,不同病程之间差异具有统计学意义,这与上述研究结果相一致。
2.不孕症病程与既往生育史:对不同病程女性的既往生育史进行比较,发现病程≥36个月组的平均月经周期较长(P<0.05),月经稀发程度更为严重,月经稀发为PCOS月经紊乱的主要表现,与BMI、WHR、高雄激素血症、糖、脂代谢紊乱等密切相关,以上因素均会导致HPO轴功能紊乱,雌孕激素分泌异常,影响月经周期及排卵,进而导致不孕症患者病程延长。此外,有研究表明[20],月经周期为PCOS患者排卵和生化妊娠的独立影响因素,对于PCOS不孕患者的排卵率和生化妊娠率具有显著影响,这与本研究结果相类似。与此同时,Yu等[21]发现,月经稀发组和闭经组的生化妊娠率要高于月经规律组,这也从侧面佐证了本研究中不孕症病程长的患者伴有较长月经周期的研究结果。
3.不孕症病程与性激素:SHBG在人类生殖过程中发挥重要作用,它是由氨基酸残基组成的多肽链同型二聚体,是一种结合雌激素和雄激素并调节其生物活性的运输载体,经常被用作PCOS女性高雄激素血症的指标。SHBG既和机体异常代谢密切相关,还可对PCOS患者机体异常糖脂代谢、IR、高胰岛素血症(hyperinsulinemia,HI)的发生进展产生一定影响。SHBG在PCOS的发生发展中起着至关重要的作用,与PCOS的发病风险及长期预后息息相关。SHBG在肝脏中合成,对睾酮具有高亲和力,可调节血液中生物活性性激素的浓度,影响其生物利用度,低SHBG水平通常伴有高TT水平和高FAI水平[22-23]。本研究发现,不孕症病程与SHBG水平呈现负相关,与FAI水平呈现正相关且不同病程的TT水平呈现出升高趋势,这与上文研究结果相似。血清SHBG的水平影响妊娠结局,何均等[24]研究发现,同对照组相比,低水平SHBG患者雄激素水平升高,受精、胚胎着床与妊娠的发生率降低。这可能与PCOS患者的IR及高雄激素血症有关,机体SHBG水平降低,游离睾酮分泌增加,从而对胰岛素代谢产生影响,致使IR发生,促进胰岛素代偿性分泌,引发代偿性HI,影响卵泡功能,加快雄激素分泌,促进卵泡募集,致使窦卵泡数明显增加,抑制卵泡发育,引起排卵障碍,导致不孕症的发生及持续发展。肝细胞核因子-4α (HNF-4α)是参与SHBG合成的重要转录因子,HNF-4α与SHBG启动子中的顺式元件DR1结合启动转录,并通过调节糖脂代谢和炎症因子调节肝脏SHBG水平,通过下调表达HNF -4α影响SHBG,致使其血清水平降低,HNF-4α可经调节表达SHBG间接影响PCOS,HNF -4α可能通过参与调节卵泡代谢,为卵巢代谢提供能量,以保证受精和胚胎发育的完成[25-27]。
4.不孕症病程与胰岛素和糖、脂代谢:胰岛素和糖、脂代谢异常是影响PCOS不孕症发生发展的主要原因,本研究发现,不孕症病程较长的患者,IR和高脂血症的发生率较高。Mather等[28]证明,PCOS不孕症患者中,IR和高脂血症常同时出现,IR的发生是由于机体对胰岛素的敏感性降低,导致正常剂量的胰岛素生物学效应降低,机体对胰岛素调节糖代谢的敏感性减弱,致使胰岛B细胞代偿性的分泌胰岛素,以维持机体正常生理活动。陈丽等[29]研究发现,在正常生理状态下,胰岛素可以通过抑制脂肪细胞内激素敏感脂酶的活性,导致游离脂肪酸(NEFA和FFA)降低,同时胰岛素通过促进NEFA在脂肪细胞中再酯化变为TG贮存,IR可引发机体肌肉、脂肪组织的糖利用障碍,释放大量的FFA和NFFA,FFA进入肝脏后,影响肝脏合成与释放极低密度脂蛋白(VLDL),导致TG增多;此外,IR可以降低脂蛋白酶的活性,减少TG分解时间,延长清除时间,进而导致血脂异常,形成糖、脂代谢紊乱。本研究发现,不孕症病程≥36个月组的HOMA-IR、TC、TG、LDL-C、APOB等均高于<12个月组和12≤~<36个月组,差异具有统计学意义,研究结果与Mather[28]、陈丽等[29]研究结果相类似。IR和高脂血症互相影响,共同作用于PCOS不孕症女性,导致不孕时间延长,影响生殖结局。
本研究基于针刺和克罗米芬治疗PCOS不孕患者临床试验(PCOS Act)项目,对948例不同不孕症病程的PCOS不孕症女性进行基线分析,以探讨其基线特点,发现IR、糖、脂代谢紊乱及代谢综合征可能是导致不孕症患者病程延长的主要原因,为临床诊疗提供理论依据。
1 Escobar-Morreale HF.Polycystic ovary syndrome:definition,aetiology,diagnosis and treatment.Nat Rev Endocrinol,2018,14:270-284.
2 Azziz R,Carmina E,Chen Z,et al.Polycystic ovary syndrome.Nat Rev Dis Primers,2016,2:16057.
3 Palomba S.Is fertility reduced in ovulatory women with polycystic ovary syndrome? An opinion paper.Hum Reprod,2021,36:2421-2428.
4 Duffy J,Adamson GD,Benson E,et al.Top 10 priorities for future infertility research:an international consensus development study.Fertil Steril,2021,115:180-190.
5 Kuru Pekcan M,Tokmak A,Ulubasoglu H,et al.The importance of infertility duration and follicle size according to pregnancy success in women undergoing ovulation induction with gonadotropins and intrauterine insemination.J Obstet Gynaecol,2023,43:2173058.
6 Iris A,Aydogan Kirmizi D,Taner CE.Effects of infertility and infertility duration on female sexual functions.Arch Gynecol Obstet,2013,287:809-812.
7 Wu XK,Stener-Victorin E,Kuang HY,et al.Effect of Acupuncture and Clomiphene in Chinese Women With Polycystic Ovary Syndrome:A Randomized Clinical Trial.JAMA,2017,317:2502-2514.
8 Rotterdam ESHRE/ASRM-Sponsored PCOS consensus workshop group.Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome (PCOS).Hum Reprod,2004,19:41-47.
9 中国成人血脂异常防治指南制订联合委员会.中国成人血脂异常防治指南.中华心血管病杂志,2007,35:390-419.
10 Cena H,Chiovato L,Nappi RE.Obesity,Polycystic Ovary Syndrome,and Infertility:A New Avenue for GLP-1 Receptor Agonists.J Clin Endocrinol Metab,2020,105:e2695-2709.
11 Talmor A,Dunphy B.Female obesity and infertility.Best Pract Res Clin Obstet Gynaecol,2015,29:498-506
12 Ramlau-Hansen CH,Thulstrup AM,Nohr EA,et al.Subfecundity in overweight and obese couples.Hum Reprod,2007,22:1634-1637.
13 Wise LA,Rothman KJ,Mikkelsen EM,et al.An internet-based prospective study of body size and time-to-pregnancy.Hum Reprod,2010,25:253-264.
14 Mizgier M,Jarząbek-Bielecka G,Wendland N,et al.Relation between Inflammation,Oxidative Stress,and Macronutrient Intakes in Normal and Excessive Body Weight Adolescent Girls with Clinical Features of Polycystic Ovary Syndrome.Nutrients,2021,13:896.
15 Soria-Contreras DC,Oken E,Tellez-Rojo MM,et al.History of infertility and long-term weight,body composition,and blood pressure among women in Project Viva.Ann Epidemiol,2022,74:43-50.
16 Westerlund E,Brandt L,Hovatta O,et al.Incidence of hypertension,stroke,coronary heart disease,and diabetes in women who have delivered after in vitro fertilization:a population-based cohort study from Sweden.Fertil Steril,2014,102:1096-1102.
17 Lebovitz O,Orvieto R.Treating patients with "thin" endometrium-an ongoing challenge.Gynecol Endocrinol,2014,30:409-414.
18 Isaacs JD Jr,Wells CS,Williams DB,et al.Endometrial thickness is a valid monitoring parameter in cycles of ovulation induction with menotropins alone.Fertil Steril,1996,65:262-266.
19 Weissman A,Gotlieb L,Casper RF.The detrimental effect of increased endometrial thickness on implantation and pregnancy rates and outcome in an in vitro fertilization program.Fertil Steril,1999,71:147-149.
20 罗蓉,王宇,刘洋,等.不同月经稀发程度PCOS不孕患者的基线特征及妊娠结局的差异.国际生殖健康/计划生育杂志,2022,41:446-451.
21 Yu T,Wu D,Cao Y,et al.Association Between Menstrual Patterns and Adverse Pregnancy Outcomes in Patients With Polycystic Ovary Syndrome.Front Endocrinol (Lausanne),2021,12:740377.
22 叶雅萍,李萍.性激素结合球蛋白在生殖医学中的应用研究进展.生殖医学杂志,2022,31:273-277.
23 Lim SS,Norman RJ,Davies MJ,et al.The effect of obesity on polycystic ovary syndrome:a systematic review and meta-analysis.Obes Rev,2013,14:95-109.
24 何均,熊万宇,张昌军,等.性激素结合球蛋白对多囊卵巢综合征患者行IVF-ET促排卵效果及妊娠结局的预测.大连医科大学学报,2020,42:122-127.
25 Zhu JL,Chen Z,Feng WJ,et al.Sex hormone-binding globulin and polycystic ovary syndrome.Clin Chim Acta,2019,499:142-148.
26 Khan DR,Landry DA,Fournier É,et al.Transcriptome meta-analysis of three follicular compartments and its correlation with ovarian follicle maturity and oocyte developmental competence in cows.Physiol Genomics,2016,48:633-643.
27 Schatten H,Sun QY,Prather R.The impact of mitochondrial function/dysfunction on IVF and new treatment possibilities for infertility.Reprod Biol Endocrinol,2014,12:111.
28 Mather K,Anderson TJ,Verma S.Insulin action in the vasculature:physiology and pathophysiology.J Vasc Res,2001,38:415-422.
29 陈丽,郝丽娟.脂代谢异常与多囊卵巢综合征.生殖医学杂志,2019,28:832-835.