研究数据显示,中国男性不育症患者大约有3 500万[1]。经皮睾丸/附睾精子抽吸术(testicular sperm aspiration/percutaneous epididymal sperm aspiration,TESA/PESA)或显微取精手术解决了部分无精子症患者的生育问题,但多次穿刺活检将加重睾丸组织的损伤,使生精功能进一步下降[2]。因此,为减少睾丸穿刺取精的次数,避免重复穿刺引起相关并发症,也为预防其配偶取卵当日没有足够精子可用的问题,临床常选择应用微量精子冻存技术提前冻精。
冷冻和复苏过程中,精子暴露在物理和化学因素下,导致过度脱水、膜完整性丧失、顶体功能受损、线粒体损伤、代谢功能变化和DNA碎片化等[3]。精子在冷冻前与冷冻保护剂混合,可以降低其死亡率,保护精子结构和功能的完整性。甘草酸二铵(diammonium glycyrrhizinate,DG)是中药甘草根中有效成分的第三代提取物,具有抗氧化、抗炎、免疫调节和膜保护作用,较传统甘草提取物稳定性更好、溶解度更高、生物活性更强[4]。本文旨在探讨DG对微量精子冷冻及复苏的作用效果,进而为研发无生殖毒性的绿色冷冻保护剂提供理论依据。
对象与方法
1.对象:2022年10月至2023年10月在宁夏医科大学总医院生殖医学中心门诊就诊的精液正常者15例。
纳入标准:(1)年龄 20~35岁;(2)符合正常精液参考标准,即精液量≥1.5 mL、液化时间≤60 min、浓度≥15×106/mL、前向运动率(progressive motility,PR)≥32%、精子总活力(progressive motility+non-progressive motility,PR+NP)≥40%、存活率≥58%、正常形态精子百分率≥4%、抗精子抗体阴性。
排除标准:(1)染色体异常者;(2)睾丸或生殖器官发育异常,如隐睾、睾丸萎缩或阴茎异常者;(3)附属性腺有炎症、结核或肿瘤者;(4)睾丸、阴茎、前列腺有外伤或手术史者;(5)少、弱、畸形精子症和无精子症者;(6)既往患有肝肾、心脏血管、内分泌系统等全身性疾病或严重器质性疾病者;(7)淋病、梅毒、尖锐湿疣、生殖器疱疹、艾滋病、乙型及丙型肝炎等传染性疾病者;(8)有遗传病史和遗传病家族史者。
分组标准:研究组为DG、精子冷冻培养液、精子悬液混合,根据添加DG溶液的浓度不同分为研究组A(0.01 mg/mL)、研究组B(0.05 mg/mL)、研究组C(0.1 mg/mL);对照组为精子冷冻培养液和精子悬液混合;空白组为单纯精子悬液组。
本研究经本院伦理委员会审核批准。
2.DG溶液的配置:称取90% DG盐粉剂100 mg,加入PBS缓冲溶液,将其浓度分别调整为0.01 mg/mL、0.05 mg/mL、0.1 mg/mL备用。
3.精液样本的处理:按实验分组向冻存管中分别加入0.5 mL含有甘油、海藻糖、人血白蛋白和硫酸庆大霉素的精子冷冻培养液及等量的不同浓度的DG溶液,充分混匀;在精液样本中加入PBS缓冲溶液进行稀释,使其最终浓度调整为15~20×106/mL,检测冷冻前的各项精液参数及精子功能指标;向不同实验分组的冻存管中再分别加入0.5 mL稀释后的精液,将冷冻保护剂与精液充分混匀,室温平衡10 min。
4.冷冻复苏:将分装好的冻存管置于液氮表面上方5 cm处熏蒸10 min,10 min后完全投入-196℃液氮中保存,24 h后将冻存管从-196℃液氮中取出,室温下进行复温,待精子完全复苏后检测各项精液参数及精子功能指标。
5.检测方法:按照WHO《人类精液检查与处理实验室手册》第5版的方法,待精液完全液化后,采用BEION S3-3全自动精子质量分析仪、穗加SSA-IIplus精子形态全自动分析仪,自动分析计算精子的浓度、总活力(PR+NP)、PR等。用微量移液器吸取100 μL精液样本并添加膨胀液,制备涂片,计数200个精子中尾部膨胀精子数,重复计数两遍,计算膨胀精子的平均百分比,即为精子存活率。采用Diff-Quik精子形态快速染色液试剂盒检测精子畸形率,至少选取200个精子,分析其中正常精子和异常精子的比例。选用精子核完整性染色试剂盒,采用NovoCyteD1040流式细胞仪以及电脑配套NovoExpress检测系统,至少分析5 000个精子,观察染色情况。选用精子活性氧染色液(DCFH-DA法)试剂盒,用NovoCyteD1040流式细胞仪检测其荧光强度。选用人转录因子E2相关因子2(Nrf2)试剂盒、人血红素氧合酶1(HO-1)试剂盒检测Nrf2、HO-1水平(ELISA法)。
6.统计学处理:采用SPSS 26.0统计软件进行数据分析,符合正态分布的计量资料使用均数±标准差![]() 表示;两组间比较采用独立样本t检验;符合正态分布和方差齐性的多组间比较采用单因素方差分析;两指标间的相关性采用Spearman分析。以α=0.05为检验水准,P<0.05为差异有统计学意义。
表示;两组间比较采用独立样本t检验;符合正态分布和方差齐性的多组间比较采用单因素方差分析;两指标间的相关性采用Spearman分析。以α=0.05为检验水准,P<0.05为差异有统计学意义。
结果
1.体外孵育后各组精子总活力(PR+NP)及PR的比较:研究组C的精子总活力(PR+NP)和PR均明显高于研究组A、研究组B、对照组和空白组(P均<0.05),见表1。
表1 体外孵育后各组精子总活力(PR+NP)和PR的比较![]()
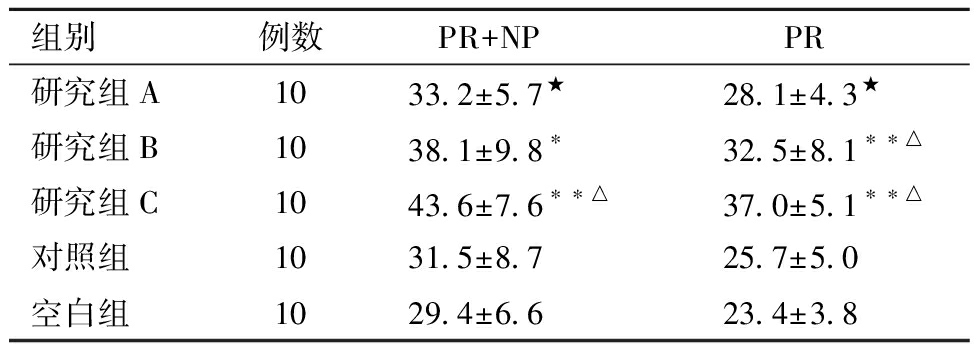
组别例数PR+NPPR研究组A1033.2±5.7★28.1±4.3★研究组B1038.1±9.8∗32.5±8.1∗∗△研究组C1043.6±7.6∗∗△37.0±5.1∗∗△对照组1031.5±8.725.7±5.0空白组1029.4±6.623.4±3.8
与空白组比较,*P<0.05,**P<0.01;与对照组比较,△P<0.01;与研究组C比较,★P<0.01
2.对照组冷冻复苏前后各项精液参数比较:冷冻复苏后的精子总活力(PR+NP)、PR、存活率均明显低于冷冻前,畸形率、DNA碎片率(DNA framentation,DFI)、活性氧(reactive oxygen species,ROS)均明显高于冷冻前(P均<0.001),见表2。
表2 冷冻复苏前后各项精液参数比较![]()

组别例数畸形率DFIROS冷冻前1594.9±1.2 5.2±2.020.4±3.6 复苏后1597.0±0.8∗12.2±3.3∗73.5±6.6∗
与冷冻前比较,*P<0.001
3.冷冻复苏后五组精子质量的比较:
(1)冷冻复苏后各组精子总活力和PR的比较。
研究组A的精子总活力和PR均明显高于研究组B、研究组C和空白组(P均<0.05);研究组B、研究组C和空白组的精子总活力和PR均明显低于对照组(P均<0.001),见表3。
表3 冷冻复苏后各组精子总活力和PR的比较![]()

组别例数PR+NPPR研究组A1530.8±5.4∗★★▲20.2±2.4∗★★▲研究组B1525.3±3.7∗△★17.1±3.3∗△★研究组C1521.7±2.7∗△14.8±2.3∗△对照组1532.5±6.1∗21.7±2.9∗空白组151.3±1.3 0.7±0.8
与空白组比较,*P<0.001;与对照组比较,△P<0.001;与研究组C比较,★P<0.05,★★P<0.001;与研究组B比较,▲P<0.01
(2)冷冻复苏后各组精子存活率、畸形率和DFI的比较。
研究组A的精子存活率明显高于研究组B、研究组C和空白组(P均<0.05),畸形率明显低于研究组B、研究组C和空白组(P均<0.05);研究组B、研究组C和空白组的精子存活率明显低于对照组,畸形率明显高于对照组(P均<0.001),见表4。
表4 冷冻复苏后各组精子存活率、畸形率和DFI的比较![]()
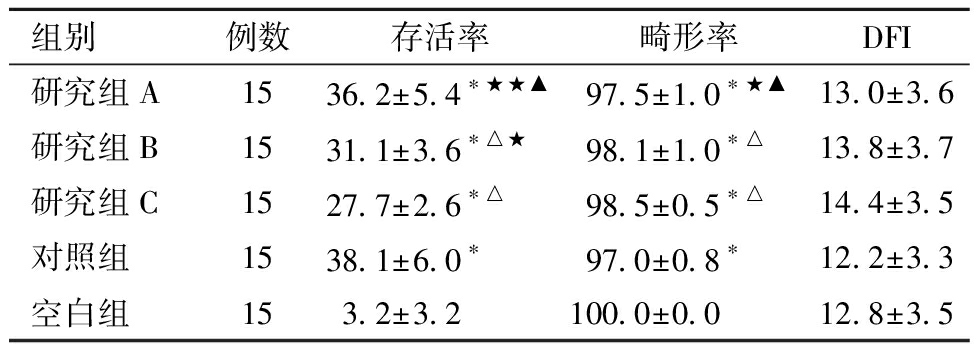
组别例数存活率畸形率DFI研究组A1536.2±5.4∗★★▲97.5±1.0∗★▲13.0±3.6研究组B1531.1±3.6∗△★98.1±1.0∗△13.8±3.7研究组C1527.7±2.6∗△98.5±0.5∗△14.4±3.5对照组1538.1±6.0∗97.0±0.8∗12.2±3.3空白组153.2±3.2100.0±0.012.8±3.5
与空白组比较,*P<0.001;与对照组比较,△P<0.001;与研究组C比较,★P<0.05,★★P<0.001;与研究组B比较,▲P<0.05
(3)冷冻复苏后精子总活力(PR+NP)、PR、存活率、畸形率之间的相关性分析。
精子总活力和PR与存活率呈显著正相关(P均<0.001);精子总活力、PR以及存活率与畸形率呈显著负相关(P均<0.001),见表5。
表5 冷冻复苏后精子总活力、PR、存活率、畸形率之间的相关性分析

指标 PR+NPrPPRrP存活率rP存活率0.99∗ 0.000 0.88∗0.000——畸形率-0.76∗ 0.000-0.86∗0.000 -0.75∗ 0.000
*P<0.001
4.冷冻复苏后五组精子氧化应激分子水平的比较:
(1)冷冻复苏后各组精子ROS、Nrf2和HO-1水平的比较。
研究组A的Nrf2水平明显高于对照组和空白组(P均<0.05);研究组B、研究组C的Nrf2和HO-1水平明显高于对照组和空白组(P均<0.01);研究组B的HO-1水平明显高于研究组A和研究组C(P均<0.05),见表6。
表6 冷冻复苏后各组精子ROS、Nrf2和HO-1水平的比较![]()
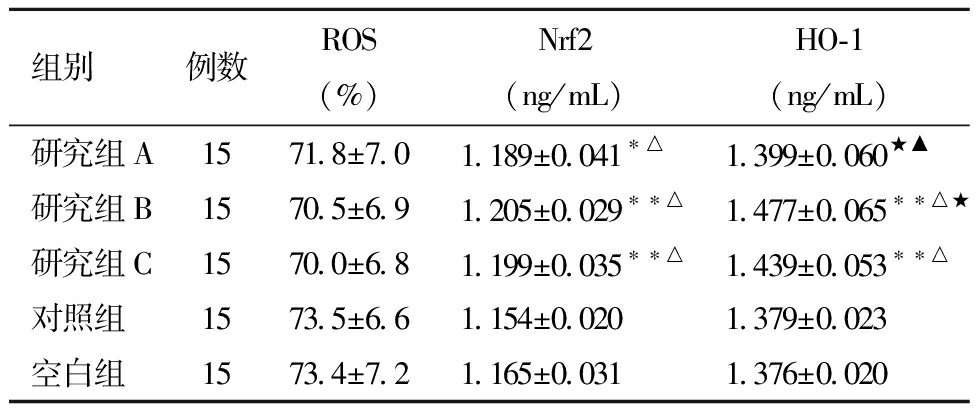
组别例数ROS(%)Nrf2(ng/mL)HO-1(ng/mL)研究组A1571.8±7.01.189±0.041∗△1.399±0.060★▲研究组B1570.5±6.91.205±0.029∗∗△1.477±0.065∗∗△★研究组C1570.0±6.81.199±0.035∗∗△1.439±0.053∗∗△对照组1573.5±6.61.154±0.0201.379±0.023空白组1573.4±7.21.165±0.0311.376±0.020
与空白组比较,*P<0.05,**P<0.01;与对照组比较,△P<0.01;与研究组C比较,★P<0.05;与研究组B比较,▲P<0.01
(2)冷冻复苏后精子ROS与Nrf2、HO-1水平间的相关性分析。
精子ROS与Nrf2呈显著负相关,Nrf2与HO-1呈显著正相关(P均<0.05),见表7。
表7 冷冻复苏后精子ROS与Nrf2、HO-1水平间的相关性分析
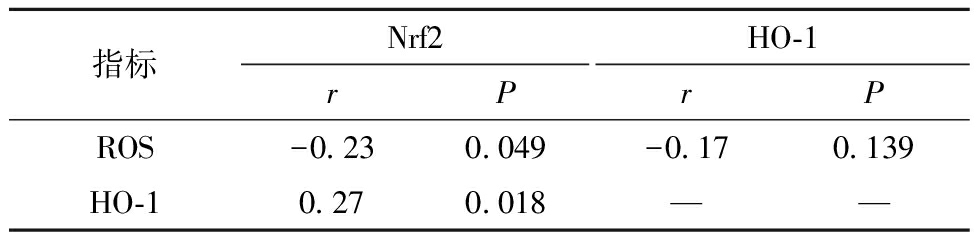
指标Nrf2rPHO-1rPROS-0.230.049-0.170.139HO-1 0.270.018— —
讨论
对于重度、极重度少弱精子症或青少年恶性肿瘤患者,精子冷冻保存是保留生育力的有效策略。精子在降温和升温过程中,细胞内氧化应激反应加剧,精子内外冰晶形成,导致精子膜破裂、线粒体损伤等,精子活力降低甚至凋亡[5]。Ozimic等[6]研究也证实冷冻-解冻程序会降低精子的活力。精子冷冻复苏后影响其活力的因素主要有:(1)细胞内外冰晶形成;(2)精子膜完整性破坏;(3)线粒体损伤;(4)DNA结构断裂;(5)冷冻保护剂的高溶质浓度等[7]。既往研究表明,在冷冻保护剂中加入甘氨酸、维生素E、α-生育酚、α-硫辛酸、左旋肉碱等抗氧化剂可以显著改善解冻后精子的运动能力[8-12]。DG作为甘草根中的主要活性成分,既往主要用于各种肝脏疾病抗炎及抗氧化治疗效果的观察,目前尚未见其用于精子冷冻培养液添加剂的研究。本研究发现,不同浓度的DG溶液孵育精子1 h后,精子活力较对照组和空白组均明显升高,添加0.1 mg/mL DG时的差异最显著(P均<0.01),说明不同浓度的DG溶液均可以发挥有益的细胞保护作用。这与Khan等[13]的研究结果相似,他们检测了不同浓度GL(50,100,200 μM)处理24 h对胃癌细胞活力的影响,均未显示出明显的毒性。且本研究添加0.01 mg/mL DG组冷冻复苏后的精子总活力和PR与对照组差异无统计学意义,但显著高于空白组(P<0.001),表明DG具有提升精子活力的积极作用。
精子存活率降低会影响男性生育能力[14]。王金宝等[15]研究发现,与精子存活率降低组相比,存活率正常组的PR及体外受精-胚胎移植(in vitro fertilization-embryo transfer,IVF-ET)临床妊娠率显著提高,生化妊娠率则减低,差异均具有统计学意义(P<0.05),且精子存活率与IVF-ET患者的助孕结局呈显著正相关(r=0.37,P<0.05)。为了减轻这种冷冻损伤作用,在冷冻保护剂中添加外源性抗氧化剂,可以保护精子质膜和顶体的完整性以及精子的受精能力,延长精子体外存活时间[16]。本研究显示,研究组A冷冻复苏后的精子存活率显著高于B组、C组及空白组(P均<0.05),畸形率显著低于B组、C组及空白组(P均<0.05);而研究组A的精子存活率及畸形率与对照组相比,差异均无统计学意义;由此显示0.01 mg/mL是DG溶液的最佳添加浓度。此外,本研究对精子常规参数、存活率及畸形率之间做了相关性分析,结果显示,精子总活力和PR与存活率之间显著正相关(分别r=0.99,r=0.88,P均<0.001),精子总活力、PR以及存活率与畸形率之间显著负相关(分别r=-0.76,r=-0.86,r=-0.75,P均<0.001)。随着添加的DG浓度升高会降低精子活力以及存活率,增加精子头部和尾部的畸形率,分析可能原因在于高浓度冷冻保护剂对精子细胞产生的渗透毒性作用。
DFI是指在各种应激条件下,发生DNA单链或双链断裂的精子占全部精子的百分比,是目前临床上用于精子核DNA完整性评估的重要指标[17]。麦选诚等[18]研究发现,男性不育症患者的DFI与精子活动率、PR存在明显的负相关(r=-0.58,r=-0.55,P均<0.01),与精子浓度之间无相关性(r=-0.05,P>0.05),且当DFI>19.5%时,精液质量有进一步降低的趋势。王金宝等[19]研究显示,DFI与精子存活率呈负相关(r=-0.59,P<0.05),与PR、hCG阳性率、临床妊娠率也呈负相关(r分别为-0.51、-0.51、-0.49,P均<0.05)。但也有研究显示,冷冻保存方法和冷冻保护剂并不会对精子DNA完整性产生明显影响[20]。本研究中随着添加DG的浓度增加,冷冻复苏后精子的活力和存活率均降低,DFI升高,精子中段和尾部的畸形率也明显增加。但本研究表明,研究各组冷冻复苏后的DFI与对照组和空白组之间比较,差异均无统计学意义,添加不同浓度DG溶液对精子DNA完整性的影响并不明显,表明DG作为抗氧化添加剂具有一定安全性。
傅龙龙等[21]通过透射电镜观察,精子冷冻复苏后质膜肿胀、线粒体结构疏松、线粒体嵴增宽,且复苏后精子内的ROS和MDA含量显著升高,总抗氧化能力和超氧化物歧化酶(superoxide oxygen species,SOD)活性显著降低,精子线粒体膜电位也明显减低,三磷酸腺苷(adenosine triphosphate,ATP)生成显著减少。此外,周广义等[22]结果显示精子DFI与ROS水平呈正相关(r=0.76,P<0.01)。本研究显示,在冷冻培养液中添加不同浓度的DG溶液均可以减少ROS的生成,且呈剂量依赖性,研究各组的Nrf2、HO-1的表达较对照组和空白组也明显上升;Spearman分析显示,Nrf2水平与ROS含量之间呈显著负相关(r=-0.23,P<0.05),Nrf2与HO-1水平之间呈正相关(r=0.27,P<0.05)。精子冷冻复苏过程中氧化应激反应加剧,诱导Nrf2及下游信号分子HO-1的表达水平升高,从而降低ROS的含量。因此,DG对精子超低温冷冻保存过程中氧化应激损伤的改善作用可能是通过激活Nrf2/HO-1通路,减少ROS生成,从而保护精子结构和功能的完整性。然而,如何添加最佳浓度的DG溶液从而显著改善渗透损伤效果以及对于其他保护作用机制还需进一步探究。
1 Inhorn MC,Patrizio P.Infertility around the globe:new thinking on gender,reproductive technologies and global movements in the 21st century.Hum Reprod Update,2015,21:411-426.
2 毛加明,刘德风,赵连明,等.睾丸穿刺活检对特发性非梗阻性无精子症患者显微取精成功率的影响.北京大学学报(医学版),2018,50:613-616.
3 王晓涵.采用-80℃冰箱冷冻保存人类精子的研究.安徽医科大学,2023.
4 Shi HJ,Song HB,Wang L,et al.The synergy of diammonium glycyrrhizinate remarkably reduces the toxicity of oxy-matrine in ICR mice.Bio Med Pharm,2018,97:19-25.
5 Kumar A,Prasad JK,Srivastava N,et al.Strategies to Minimize Various Stress-Related Freeze-Thaw Damages During Conventional Cryopreservation of Mammalian Spermatozoa.Biopreserv Biobank,2019,17:603-612.
6 Ozimic S,Ban-Frangez H,Stimpfel M.Sperm Cryopreservation Today:Approaches,Efficiency,and Pitfalls.Curr Issues Mol Biol,2023,45:4716-4734.
7 Ali Mohamed MS.Slow cryopreservation is not superior to vitrification in human spermatozoa; an experimental controlled study.Iran J Reprod Med,2015,13:633-644.
8 Nazif MS,Rehman ZU,Khan H,et al.Glycine Improved Cryopreserved Spermatozoa Quality in Achai Bull.Biomed Res Int,2022,2022:8282387.
9 Alonge S,Melandri M,Leoci R,et al.Ejaculation effect on blood testosterone and prostatic pulsed-wave Doppler ultrasound in dogs.Reprod Domest Anim,2018,53 Suppl 2:70-73.
10 Ratnani H,Suprayogi TW,Sardjito T,et al.Alpha-tocopherol improves sperm quality by regulate intracellular Ca2+ intensity (influx/efflux) of Simmental bull cattle sperm.Infect Dis Rep,2020,12:8721.
11 Shen T,Jiang ZL,Li CJ,et al.Effect of alpha-lipoic acid on boar spermatozoa quality during freezing-thawing.Zygote,2016,24:259-265.
12 Kooshesh L,Nateghian Z,Aliabadi E.Evaluation of L-Carnitine Potential in Improvement of Male Fertility.J Reprod Infertil,2023,24:69-84.
13 Khan U,Karmakar BC,Basak P,et al.Glycyrrhizin,an inhibitor of HMGB1 induces autolysosomal degradation function and inhibits Helicobacter pylori infection.Mol Med,2023,29:51.
14 汪珣,朱来晴,石亮.精子存活率检测在精液分析中的价值探讨.中国社区医师,2020,36:71-72.
15 王金宝,张玉强,韩越,等.精子DNA碎片指数结合精子存活率对辅助生殖患者助孕结局的预测价值.医学理论与实践,2024,37:296-298.
16 张星.黄芪多糖对奶山羊精液冷冻保存效果的影响.西北农林科技大学,2022.
17 常椿欣,吴正沐,王彦林.精子DNA碎片指数与精液常规参数及精子运动参数的相关性分析.中国计划生育学杂志,2022.
18 麦选诚,董云华,陈斌,等.不育患者精子DNA损伤和精液常规参数关系分析.中国男科学杂志,2016,30:19-22.
19 王金宝,张玉强,韩越,等.精子DNA碎片率及精子存活率联合检测对体外受精-胚胎移植助孕结局的预测价值分析.生殖医学杂志,2023,32:671-676.
20 Isachenko E,Isachenko V,Katkov II,et al.DNA integrity and motility of human spermatozoa after standard slow freezing versus cryoprotectant-free vitrification.Hum Reprod,2004,19:932-939.
21 傅龙龙,宋小芬,张开舒,等.冷冻复苏对人精子线粒体的影响.中华男科学杂志,2020,26:984-988.
22 周广义,吕慧杰,张花锦,等.精浆弹性蛋白酶、精液白细胞浓度、精子活性氧和精子DNA碎片指数间的相关性分析.中国校医,2023,37:786-789.