妇科恶性肿瘤发病率近年来有增长的趋势,是女性妇科疾病中主要的死亡原因。治疗失败的主要原因是局部的复发和远处的转移。相关研究已证实,人类肿瘤的生长和远处转移与血管的生成密切相关。近年来研究发现C-erbB-2基因和巨噬细胞移动抑制因子(migration inhibitory factor,MIF)与肿瘤血管的生成密切相关,可促进肿瘤的浸润和转移,对恶性肿瘤的预后及治疗有重要的意义。本文将根据国内外研究对C-erbB-2基因和MIF进行综述。
一、C-erbB-2基因
1.C-erbB-2基因的结构及生物学特性:C-erbB-2基因是一种原癌基因,又称为neu或HER-2基因,是于1981年在神经母细胞中首先被发现的癌基因,主要在胚胎发育时开始表达,成年后则在正常组织内很少有表达[1],其定位于染色体17q21区带,起始于35109922位点,终末于35138436位点,全长4.6 kb,基因编码的蛋白产物为跨膜糖蛋白p185,是具有酪氨酸激酶(tyrosine kinase,TK)活性的受体,由信号肽、配体结合区、跨膜区及胞质区4部分组成,与表皮生长因子(epidermal growth factor receptor,EGFR)高度同源,为82%能调节细胞的增殖和变异,在维持上皮组织的完整性起到重要的作用。
C-erbB-2是一种细胞来源的原癌基因,在正常情况下处于非激活状态,是细胞生长、分化、存活的重要调节者。目前尚未发现C-erbB-2受体的特异性配体,其与生长因子家族的中的其他成员形成异质二聚体,C-erbB-2异质二聚体结合比均质二聚体结合有更强的结合性和更强的刺激正常细胞和肿瘤细胞生长的活性,当间接与配体连接后,主要是激活Ras-raf/fMAPK(分裂素活化蛋白)途径、磷脂酰肌醇3-激酶(PI3K)/Akt途径、信号转导及转录激活途径及其他途径,参与细胞内信号的转导。当在某些因素的作用下被激活后,结构将会发生改变导致过度表达,使正常细胞生长、分化及凋亡过程遭到破环,进而显示出肿瘤转化活性。目前C-erbB-2基因有抑制细胞凋亡、上调血管内皮生长因子或血管通透因子、促进肿瘤血管形成、增加肿瘤细胞的侵袭能力、破坏机体组织抗侵袭屏障的作用。
2.C-erbB-2基因与新生血管的形成:C-erbB-2基因是一种原癌基因,早先主要研究抑制细胞凋亡方面,近年来越来越多的研究发现与新生血管的形成有关。C-erbB-2基因激活后可以通过多种信号转导通路,以血管内皮生长因子(vascular endothelial growth factor,VEGF)依赖性或非依赖性方式直接或间接调控血管新生,例如Izumi等[2]用抗C-erbB-2抗体处理neu过表达的乳腺癌细胞株SKBR-3,证明了C-erbB-2在部分上通过对VEGF的上调作用刺激肿瘤的新生血管作用,C-erbB-2基因通过影响癌细胞分泌的多种血管生成因子进行间接控制;Simeone等[3]证实C-erbB-2通过调控环氧合酶2(COX-2)来促进肿瘤新生血管的形成。另有学者应用RT-PCR和免疫组化对44例脑胶质瘤和26例脑膜瘤进行分析,发现在绝大多数的脑膜瘤中C-erbB-2 mRNA的表达率都很高,并且发现该蛋白主要集中分布于肿瘤的毛细血管周围[4],说明C-erbB-2和肿瘤的血管形成有关系。
3.C-erbB-2基因与肿瘤:C-erbB-2诱导肿瘤发生的基本要素是C-erbB-2的多拷贝、跨膜区的突变或过度表达,导致基因转录增加,引起C-erbB-2 mRNA水平升高,同时C-erbB-2蛋白的合成增加,从而在细胞表面过度表达,细胞过度生长。肿瘤的生长浸润及局部的转移都离不开肿瘤血管的参与,C-erbB-2作为表皮生长因子家族的一员,其作为增殖和变异的调解者在维持上皮组织的完整性起到重要的作用,是人类肿瘤中发生改变频率最高的癌基因之一。
近年来大量的研究证明[5-7],C-erbB-2基因在多种肿瘤中存在的过度表达与肿瘤的局部转移和侵袭力有关,在乳腺癌、宫颈癌、卵巢癌、子宫内膜癌、肾细胞癌、消化道肿瘤等都有过表达。多项研究表明,C-erbB-2基因在乳腺癌中与侵袭转移呈正相关,反映了肿瘤局部生长、浸润及淋巴道转移的能力,是早期复发和较短生存率和预后的检测指标[8-9]。另有研究[10]证实C-erbB-2在乳腺癌骨转移比早期的患者高表达,并有统计学意义(P=0.029),由此可以说明C-erbB-2的表达与肿瘤的侵袭和转移有关,可以作为肿瘤预后的指标之一。早有研究者利用免疫组化法发现乳腺癌患者中C-erbB-2基因蛋白表达阳性组血管生成高于阴性组,差异具有统计学意义(P<0.05)[11]。刘宜敏等[12]通过检测77例鼻咽癌患者中C-erbB-2与血管内皮生长因子的研究发现,VEGF的生血管机制可能与C-erbB-2的活性有关,C-erbB-2基因的高表达还能诱导VEGF的表达、促进肿瘤微血管生成,进而可以说明原癌基因2的表达与肿瘤血管生成有关,进而影响肿瘤的侵袭和转移能力,可以作为肿瘤预后的指标之一。
二、MIF
1.MIF基因及生物学特性:MIF是1966年在研究迟发型超敏反应时发现的一种由T细胞产生的细胞因子,MIF作为T淋巴细胞激活的产物,由于在体外抑制巨噬细胞移动而得名。人MIF基因348 bp,基因长度小于1 kb,定位于22q11.23,由3个外显子和2个内含子组成,3个外显子被2个短内含子分开,MIF分子含有115个氨基酸,分子质量为l2.5 kD,具有ot链和p链组成的三维结构,MIF的启动子上游调节元件,具有前炎症介质的基因特征[13]。与任何其他已知蛋白质之间无明显的同源性,目前不属于任何细胞家族。有研究发现CD74可能是MIF的膜受体,与CD74的胞外部分结合后,可激活细胞外信号调节激酶(ERK)的磷酸化等一系列的级联反应,从而产生各种生理效应[14],MIF的结构特点可能与MIF蛋白的生物学功能密切相关。MIF受下丘脑垂体控制,是一种多功能的细胞因子,在炎症、免疫、神经系统、内分泌、肿瘤、血管等方面都有研究,过去一直以为只是炎症和免疫反应的重要调节因子,近来研究[15]发现与肿瘤的发生密切相关,可能是通过直接影响正常细胞的分裂和癌基因诱导的恶性转化,还通过调节免疫反应、抑制抑癌基因的功能和促进肿瘤血管生成,从多个层次促进肿瘤的发生和发展。
2.MIF与恶性肿瘤:恶性肿瘤的发生是多种因素、多个基因共同参与的,其中血管的生成在恶性肿瘤的发展中起到重要的作用。近年来研究[16]发现,MIF可通过磷酸化来激活ERK/MAPK途径,促进肿瘤的增殖;抑制P53基因,减少细胞的凋亡,促进肿瘤细胞的发生和生长;促进肿瘤血管的生成,进而影响肿瘤细胞的侵袭和转移。
目前,在一些恶性肿瘤如肝细胞癌、非小细胞肺癌、前列腺癌、乳腺癌中,宫颈癌患者中都有表达,MIF反义RNA也可以抑制这些肿瘤的生长增殖。蔡施霞等[17]通过体内和体外实验来检测MIF对血管形成的关系的研究中发现,肉眼状态下MIF组出现类似血管瘤样的明显血管丛,而对照组仅发现少许的发丝样血管,计算血管密度结果发现MIF组血管数量明显多于阴性对照组,差异具有统计学意义。另有研究报道MIF可以上调VEGF(血管内皮生长因子)来促进肿瘤的血管生成和肿瘤的侵袭[18]。Hagemann等[19]通过对小鼠卵巢癌模型的研究发现,低浓度的MIF能减慢肿瘤的增长和增加细胞的凋亡,这和增加抑癌基因p53的磷酸化和降低Akt的磷酸化有关,并且发现MIF在在恶性腹水中强表达,证实了卵巢癌细胞自分泌产生的MIF刺激其他细胞因子,趋化因子,血管生成因子,可以促进肿瘤的局部浸润和肿瘤血管的形成,这和国内张利群等[20]的研究结果一致,都能促进肿瘤血管的形成和局部转移。Nishihira等[21]通过利用反义MIF基因抗体治疗结肠癌细胞的小鼠和对转MIF基因小鼠的研究发现,肿瘤的生长和相关的血管形成与MIF密切相关;徐天敏等[22]通过免疫组化对79例肝癌患者组织的研究证实MIF与VEFG呈正相关,与肿瘤的生长和转移有关,可以作为肿瘤进展和转移的指标之一。这些研究说明,MIF能促进肿瘤新生血管的形成,与肿瘤的生长、浸润和转移密切相关。
3.妇科恶性肿瘤与血管生成的关系:恶性肿瘤的生长、浸润、转移及复发均依赖于新生血管的形成。如果没有新生血管对肿瘤细胞的营养和支持,肿瘤组织的体积不超过1 mm,因而抗肿瘤血管生长,也是目前肿瘤治疗的研究热点。血管生成主要是通过肿瘤的血管从宿主细胞中获得所需的营养物质和提供转移所需的细胞因子促进肿瘤的生长和转移。目前最典型的促进血管生成的因子是VEGF,其受体的表达将会诱导肿瘤血管生成促进多种肿瘤的转移[23],肿瘤的促血管生长因子的表达使新生血管增加,在人类许多癌症中都证实与肿瘤的局部浸润、转移和预后有关。
三、展望
近几年的研究中越来越多的报道证实C-erb-B-2基因和MIF与血管生成有关,与肿瘤的生长、局部浸润、转移和预后有密切的相关性。肿瘤的浸润和转移是一个复杂的过程,与新生血管的形成有关。如果能确认C-erb-B-2基因和MIF在妇科恶性肿瘤中有直接的影响,那么联合检测C-erb-B-2基因和MIF将对恶性肿瘤的分级和预后有重要的参考价值,利用中和抗体来抑制肿瘤血管的新生,同样对提高妇科恶性肿瘤患者术后生存时间和生活质量有广阔的前景。
参考文献
1 Xu ZH,Ford BD.Uperegulation of cerbB recepters in rat brain after middle cerebrial arterial occlusion.Neurosci Lett,2005,375:181-186.
2 Izumi Y,Xu L,Fukumura D,et al.Tumor biology:herceptin acts as an anti-angiogenic cocktail.Nature,2002,416:279-280.
3 Simeone AM,Li YJ,Broemeling LD,et al.Cyclooxygenase-2 is essential for HER2/neu to suppress N-(4-hydroxyphenyl) retinamide apoptotic effects in breast cancer cells.Cancer Res,2004,64:1224-1228.
4 Andersson U,Guo D,Malmer B,et al.Epidermal growth factor receptor family(EGFR,CerbB-2-4) ingliomas and meningiomas.A cta Neuropathol,2004,108:135-142.
5 Uberall I,Kolar Z,Trojanec R,et al.The status and role of ErbB receptors in human cancer.Exp Mol Pathol,2008,84:79-89.
6 Yarden Y,Sliwkowski MX.Untangling the ErbB signalling network.Nature Reviews Molecular Cell Biology,2001,2:127-37.
7 Odicino F,Bignotti E,Rossi E,et al.HER-2/neu overexpression and amplification in uterine serous papillary carcinoma:comparative analysis of immunohistochemistry,real-time reverse transcription-polymerase chain reaction,and fluorescence in situ hybridization.Int J Gynecol Cancer,2008,18:14-21.
8 Bhatavdekar JM,Patel DD,Shah NG,et al.Prognostic significance of immunohistochemically localized biomarkers in stageⅡand stageⅢ breast cancer.a multivariate analysis.Ann Surg Oncol,2000,7:305.
9 Pérez-Regadera J,Sánchez-Mu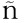 oz A,De-la-Cruz J,et al.Negative prognostic impact of the coexpression of epidermal growth factor receptor and c-erbB-2 in locally advanced cervical cancer.Oncology,2009,76:133-141.
oz A,De-la-Cruz J,et al.Negative prognostic impact of the coexpression of epidermal growth factor receptor and c-erbB-2 in locally advanced cervical cancer.Oncology,2009,76:133-141.
10 Linforth RA,Anderson NG,Knox WF,et al.CerbB2 oncoprotein expression is increased in breast cancer bone metastases.Endocrine/Breast,2001,88:5.
11 Toi M,Kashitani T,Tominaga T.Tumor angiogenesis is an independent prognostic indicator in primary breast carcinoma.Int J Cancer,1993,55:371.
12 刘宜敏,杨光伟,白守民,等.鼻咽癌组织中C-erbB-2的表达与血管生成的关系.南方医科大学学报,2007,27:1588-1600.
13 Kwak C,Ku JH.Initial tumor stage and grade as a predictive factor for recurrence in patients with T1 Grade 3 bladder cancer.J Urol,2004,171:149-152.
14 Bemhagen J,Krohn R,Lue H,et al.MIF is a noncognate ligand of CXC chemokine receptors in inflammatory and atherogenic cell recruitment.Nat Med,2007,13:587-596.
15 Bifulco C,McDaniel K,Leng L,et al.Tumor orowth-promoting properties of macrophage migration inhibitory factor.Cur Pharm Des,2008,14:3790-3801.
16 Baron N,Deuster O,Noelker C,et al.Role of macrophage migration inhibitory factor in primary glioblastoma multiforme cells.J Neurosci Res,2011,89:711-717.
17 蔡施霞,余细勇,林秋雄,等.MIF促进新生血管生成及其相关基因表达的研究.中国心血管杂志,2007,3:169-171.
18 Sun HW,Bemhaagen J,Bucala R,et al.Crystal structure at 2.6A° resolution of human macrophage migration inhibitory factor.PNAS,1996,93:5191.
19 Hagemann T,Robinson SC,Thompson RG,et al.Ovarian cancer cell-derived migration inhibitory factor enhances tumor growth,progression,and angiogenesis.Mol Cancer Ther,2007,6:1993-2002.
20 张利群,蔡知天,李清桃.MIF及VEGF在卵巢癌中的表达及其临床意义.中国妇幼保健,2008,23:4185-4188.
21 Nishihira J,Ishibashi T,Fukushima T,et al.Macrophage migration inhibitory factor (MIF):Its potential role in tumor growth and tumor-associated angiogenesis.Ann N Y Acad Sci,2003,995:171-82.
22 徐天敏,卫峥,张建中,等.原发性肝癌血清巨噬细胞移动抑制因子和血管内皮生长因子水平.江苏医药,2008,34:1203-1204.
23 Mizukami Y,Li J,Zhang X,et al.Hypoxia-inducible factor-1-independent regulation of vascular endothelial growth factor by hypoxia in colon cancer.Cancer Res,2004,64:1765-1772.