·综述·
透明带结合法用于ICSI精子筛选的研究进展
刘帅 陈志恒 王慧 马才启 梁云浩 杨丽 姜煜 孙玲
【摘要】 卵胞质内单精子注射(ICSI)是解决辅助生育中因严重男性因素造成不育的主要手段。自然受孕过程中,精子经过生殖道的层层筛选,相比之下,目前国内外的生殖中心仅通过形态及活力选择精子进行ICSI,缺乏有效的精子筛选策略。本文对基于精子功能筛选为目的的透明带结合法的相关文献进行回顾与总结,以期为此方法的临床应用提供参考。
【关键词】 透明带结合法; 卵细胞胞质内单精子注射; 精子筛选; 辅助生殖
基金项目:广州市卫生健康科技项目(20191A011027);中华医学会临床医学科研专项基金(18010210750)
作者单位:510623 广州,广州市妇女儿童医疗中心生殖医学中心
通讯作者:孙玲(sunling6299@163.com)
卵胞质内单精子注射(intracytoplasmic sperm injection,ICSI)能有效解决辅助生育中因男性精子不佳造成的不育问题。Nyboe等[1]多国家多中心的调查数据显示,ICSI在辅助生育中的使用率已由原来的39.6%上升到58.9%。目前,有些国家ICSI的使用率甚至已经达到了70%~80%[2]。虽然ICSI已经广泛应用,但妊娠结局仍不够理想。精子作为重要的父源基因载体,可影响胚胎发育的质量,从而影响最终的妊娠结局。许多男性不育均由基因缺陷所致,自然情况下射出精子的异常率高达50%~70%,精子经过层层筛选,只有活率高、结构正常的精子才能达到壶腹部,与卵母细胞结合,完成受精。ICSI规避了自然受孕中诸多筛选步骤,例如与生殖道筛选、卵冠丘筛选和卵透明带筛选等,因此,ICSI的应用可能会增加出生缺陷的风险。目前,文献报道的ICSI精子优选方法,大致可分为五类[3-4]:(1)基于精子膜电荷筛选;(2)剔除凋亡精子;(3)基于精子膜成熟度筛选;(4)精子形态学筛选;(5)精子功能筛选。本文着重对基于精子功能筛选为目的的透明带结合法用于ICSI精子筛选(ICSI using zona pellucida-bound spermatozoa,ZP-ICSI)的最新应用进行综述,并探讨其原理、可行性、优缺点和应用效果。
一、ICSI精子优选的必要性
在自然受孕过程中,有生育力的男性每次射出的精液中只有约14%(8%~25%)的活动精子可以与透明带结合,而低生育力男性人群,可以与透明带结合的活动精子甚至更少,平均为4.3%。此外,在与透明带结合的精子中,只有48%会启动顶体反应,可能会进一步完成精卵融合[5]。不论自然受孕还是体外受精(IVF),只有能与透明带结合的精子才有机会穿透卵透明带并完成受精。与ICSI相比,IVF具有相对高的胚胎发育率和妊娠结局,其中一个重要原因就是由于IVF会经历透明带与精子结合的生物学筛选过程,而这一过程在ICSI中被省略了。
传统的精子质量评价方式主要关注精子的形态和活率,上游法和密度梯度离心法是目前辅助生殖中常用的精子优选方法。这两种方法分别基于精子迁移和精子沉淀作用来筛选精子。然而,上游和密度梯度离心法无法满足精子其他特质的筛选,如精子DNA完整性、精子膜的成熟度、精子凋亡和精子超微结构等,而精子这些特质的缺陷往往是导致不育的关键因素。因此,目前很多研究把关注点放在精子成熟度和功能上,从提高辅助生殖的安全性和成功率出发,寻找更好的精子优选方法。其中ZP-ICSI是采用失去受精潜能的不成熟卵子去筛选高质量的精子,尽可能模拟自然选择的过程,弥补常规ICSI技术绕过顶体反应、精卵结合等自然受精生理过程的短板,以期提高ICSI的成功率。
二、ZP蛋白在受精中的作用
在生理条件下,透明带对物种间精卵识别及精子与顶体反应诱发起着重要的作用。ZP的表面存在大量糖基化蛋白,其多肽链上以N-连接或O-连接共价结合许多寡糖链和单糖链侧枝,例如甘露糖、N-乙酰葡糖胺等,其中分布最为丰富的是sialyl-LewisX链,即[NeuAcα2-3Galβ1-4(Fucα1-3)GlcNAc]序列,并且其在初级卵泡卵母细胞ZP中已稳定存在[6]。其功能是通过ZP糖蛋白中的寡糖和精子表面蛋白质相互作用,实现精卵识别并诱发顶体反应。人类精子与sialyl-LewisX或牛血清蛋白孵育后,精子与ZP的结合能力会大幅度下降。此外,sialyl-LewisX抗体可抑制半透明带结合实验中精卵结合的能力[7]。
Ganguly等[8]通过标记FITC研究重组人透明带糖蛋白(recombinant human zona pellucida,rhZP)与精卵结合及诱导顶体反应的相关性。结果显示,人类4种ZP糖蛋白均参与精卵结合,除了ZP2外,其余3种透明带糖蛋白均参与了顶体反应诱发。大肠埃希菌和杆状病毒系统中表达的rhZP1能与获能的精子头部前区结合,但不能与已完成顶体反应的精子结合。来自杆状病毒系统rhZP1能剂量性地诱发顶体反应,而来自大肠埃希菌rhZP1不能,提示ZP1在顶体反应中重要作用,其中人类ZP1中273~551 aa片段诱导顶体反应最强。来自原核和杆状病毒系统的rhZP2均能与已完成顶体反应的精子赤道区结合,但不与获能精子结合,说明ZP2在受精过程中是精子的次级受体。来自杆状病毒系统的rhZP3和rhZP4均能与获能精子的头部或赤道区域结合,但不能与已完成顶体反应的精子结合,这一实验结果证实了ZP3和ZP4为人类精子的初级受体[9]。考虑到重组DNA 技术获取的rhZP与天然人类透明带糖蛋白的差异,Chiu等[10-11]进行了纯化hZP蛋白功能性研究,结论基本一致。
三、ZP-ICSI在精子优选中的作用
1. 对精子蛋白的筛选:通常认为早期胚胎发育主要由卵子因素所调控,但现在研究证实,精子的基因在受精和卵裂初期,不是完全沉默的,而精子与透明带结合的能力,也是一种父源性对胚胎早期发育正向影响的机制[12]。精子与透明带的结合,可激活顶体的胞吐作用,暴露精子表面与卵母细胞特异性结合的位点。精卵相互作用所涉及的精子蛋白,如PH20、α-D-甘露糖苷酶、甘露糖结合蛋白、FA-1、选择素分子、α-岩藻糖苷酶、α1-3岩藻糖转移酶及hCRISP1等,与男性不育以及辅助生育结局是密切相关的[13-15]。良好的精子蛋白功能是精卵结合的前提,例如人类精子神经氨酸酶可消耗ZP的唾液酸残基,从而暴露ZP上的精子结合位点。倘若采用温和化学方法消耗人ZP唾液酸残基,精子-ZP结合反应减弱30%,但采用神经氨酸酶去除人ZP的唾液酸残基,精子-ZP结合反应却增强3倍[16]。虽然有诸多的精子受体被证实为ZP结合的特异蛋白,但单独的敲除某个单独特异蛋白基因,小鼠依然可以受孕[17]。由此可见,某个精子表面蛋白不能单独介导精子和透明带的相互作用,而是多个受体-配体相互配合的结果[10]。ZP-ICSI可对这些受体的表达水平进行一个综合性的筛选。
2.受精成功与否的敏感指标:精卵结合能力是受精成功与否的敏感指标,若存在缺陷是受精率低的主要原因。Liu等[18]收集IVF中获卵数≥3枚的病例,评估其精卵结合及融合能力。根据受精率将研究对象分为4组,即0%(n=369)、1%~25%(n=194)、26%~50%(n=81)、51%~95%(n=100)。受精率为0%研究组与受精率为51%~95%研究组的畸形精子率分别为36%及7%,两者差异有统计学意义。与此同时,受精率为0%的研究组中,70%的病例只有≤5条的活动精子与透明带结合。为了确定精卵结合存在缺陷,主要是卵子造成的还是精子造成的,在受精率为0%的研究组中,选取68位患者,每人随机选择4~5枚受精失败后的卵子,将其与有生育力的捐赠精液孵育2 h,结果显示,每枚重孵育后的卵子表面精子数为(96±12)条。由此可见,精卵间相互作用缺陷的原因,与卵子缺陷因素相比,更多是精子缺陷占主导因素。
3. 降低畸形精子率:精子与透明带结合能力,与精液浓度以及精子正常的形态学密切相关。文献报道,精子缺乏症的患者,通常精卵间的相互作用能力就差[19]。而正常生育力的男性(已育)人群,精液浓度>60×106/ ml组与≤60×106/ ml组的透明带诱发顶体反应率分别为(50±23)%、(37±15)%,差异具有统计学意义。与之相类似的,正常精子形态率≥15%组与<15%组的透明带诱发顶体反应率分别为(52±22)%、(40±20)%,差异亦具有统计学意义[20]。人类透明带选择性的与形态正常的精子结合,尤其是顶体大小合适且形态好的精子具有结合优势。Garrett等[21]研究证实,头部前区较大、光密度较低的精子和颈部异常较小、轴线高度对称的精子,更易与透明带结合。形态异常的精子,例如圆头精子没有顶体,就没有能力与透明带结合。
4. 顶体的去除:透明带结合法用于ICSI精子筛选有一个优势,当精子与透明带结合后,会引起顶体反应,顶体的内含物通过胞吐作用得到释放,减少了顶体的水解酶进入卵细胞,降低了毒性。ICSI技术可以应用在小鼠和人类上并获得正常的后代,而这种技术在其他物种里鲜有成功。事实上是由于小鼠和人类的顶体较小,虽然ICSI时会带入包含强大水解酶的顶体,但不会影响到卵母细胞[22]。与之相比,仓鼠就不行,由于该物种的顶体巨大,ICSI势必会导致卵母细胞的死亡。此外,多项临床研究证明,ZP诱发的顶体反应可作为辅助生育治疗中预测受精成功与否的敏感指标[20,23]。
5. DNA的完整性:辅助生育临床工作中,严重少精症、弱精子症、尤其是畸型精子症会影响精卵结合相互作用[24]。但是更多的患者的情况是常规精液检查正常,由于诸如精子DNA损伤等因素导致的微小缺陷,从而ICSI反复失败。卵母细胞能起到修复精子DNA的作用,父源性的DNA损伤可以经过卵母细胞的系统修复后,同样也可以受精,胚胎进一步发育,甚至受孕成功。但如果一份精液中精子DNA损伤有较高比例,不单影响与透明带结合的能力,还可影响受精率、胚胎发育、妊娠率及子代的健康[25]。学者们试图通过ZP-ICSI筛选出DNA完整的精子,应用吖啶橙荧光法可观察到,大多数能与透明带结合的精子(>90%)含有正常的DNA[26]。
四、ZP-ICSI的可行性
用于精子功能测试或ZP-ICSI研究的透明带来源可以是临床IVF病例中受精失败的卵子。未受精的卵子72~86 h内,仍具有与精子结合以及诱发顶体反应的功能。临床IVF实验中20%~30%的卵子通常会受精失败,然后被丢弃。而这部分卵子,经伦理委员会允许,且充分知情告知患者的情况下,95%的患者依从性很高,愿意将其进行研究或精子功能测试[18]。而ZP-ICSI临床应用时,透明带来源则通常是不成熟卵子。由于不能正常受精,不成熟卵子通常不会用来做ICSI。未成熟卵子和成熟卵子一样,具有与正常形态和完整DNA精子结合的生物学功能。因此,透明带结合实验可以采用同一周期收集的未成熟卵子[25]。如果全部为成熟卵子(≥6个),可选用其中的一个做透明带结合实验。活动精子的选择通常采用上游法或密度梯度离心法,将1×106~2×106条活动精子与卵子一起共培养2 h。正常生育力的男性,通常每个卵子平均有上百条的精子可结合在透明带上。精卵共同孵育后,将与透明带结合的精子重新回收,用于ICSI以期获得更好的临床结局。精子透明带结合实验很简单,经过短时间培训大多数胚胎学家都可以操作。但是有些特殊情况,并不适合ICSI前应用透明带结合法筛选精子。比如说有些病人,精子浓度、活力、正常形态率差或者整体精液质量十分差,或者精子是从附睾或睾丸获取的,像这样的情形,只能采用常规的精子筛选法[27]。
五、ZP-ICSI对妊娠结局的影响
ICSI技术为男性不育的治疗带来了革命性的推进。尽管现在ICSI的受精率还可以,但其胚胎的质量和植入率仍不够理想。许多学者不断探究采用ZP-ICSI是否可以提高受精率、优胚率、改善妊娠结局(表1)。最初将透明带结合法用于ICSI精子筛选的是Paes[22]团队。该团队探讨透明带结合法用于ICSI精子筛选是否可以提高受精率和获得更好的胚胎质量。该研究对象为40对接受ICSI治疗的夫妇,收集其治疗周期中不成熟卵子。研究组采用透明带结合法筛选精子,而对照组采用常规筛选的精子进行ICSI。研究显示,透明带结合筛选组与对照组的受精率分别为77.3%、76.8%,差异没有统计学意义。而优胚率分别为83.3%、70.0%,差异存在统计学意义(P=0.003)。Black等[28]做了类似的研究,结果显示,透明带结合筛选组与对照组在受精率、卵裂率、优胚率、种植率及妊娠率上差异没有统计学意义。但研究组与对照组相比,新鲜周期的种植率和临床妊娠率还是有所提高。Liu等[29]的研究结果验证了Paes团队的结论,透明带结合筛选组虽然受精率变化不大,但是可以显著提高优胚率及种植率。Casciani等[30]的实验小组研究结论和Black等的基本一致,虽然差异没有统计学意义,但是透明带结合筛选组抱婴率[Casciani:33.3% vs Black:31.6%]还是有所提高。与此同时,还观察到透明带精子结合效果与好的精子形态及浓度呈正相关趋势。金锐等[31]和Jin等[32]来自不同的两个团队,其研究数据均再次显示,透明带结合筛选组的优胚率及可利用胚胎率,与对照组相比,有显著性提高。
六、小结与展望
综上所述,由于卵母细胞资源有限,优选精子是改善ICSI技术的突破口之一。优选精子的关注点不仅要考虑精子的活力和形态,更应把是否筛选掉遗传物质异常的精子作为精子评估的重点。未来急需寻求一种简单、客观、高效和安全的精子优选方法,以期改善辅助生殖技术患者的临床结局。ZP-ICSI作为一种模拟生理状态来筛选正常的精子的方法,可以改善ICSI的妊娠结局,尤其适用常规ICSI反复失败、受精率低、精子严重畸形或DNA损伤的病例。该技术若要进行大规模的临床应用,仍需要进一步积累临床数据,严格评估其效果与可靠性。
表1 ZP-ICSI组与常规ICSI组的临床结局比较总结

作者(年份)研究组(例)对照组(例)受精率(%)研究组对照组卵裂率(%)研究组对照组优胚率(%)研究组对照组Paes等(2009)[22]404077.376.8——83.3∗70.0Black等(2010)[28]393970.569.646.453.646.453.6Liu等(2011)[29]535381.077.0——67.0∗42.0金锐等(2013)[31]272783.081.696.396.566.1∗50.8Casciani等(2014)[30]603895.095.5——62.257.0(A级)Jin等(2016)[32]384283.081.696.396.566.1∗50.8

作者(年份)研究组(例)对照组(例)可利用率(%)研究组对照组种植率(%)研究组对照组妊娠率(%)研究组对照组Paes等(2009)[22]4040——————Black等(2010)[28]3939——22.416.9☆41.729.0☆Liu等(2011)[29]5353——29.0∗17.0☆49.036.0☆金锐等(2013)[31]272776.0∗66.3——59.348.2Casciani等(2014)[30]6038——17.419.641.742.1Jin等(2016)[32]384276.0∗66.339.3∗23.160.547.6
注:*P<0.05; ☆新鲜胚胎移植周期
参考文献
1 Nyboe Andersen A,Carlsen E,Loft A.Trends in the use of intracytoplasmatic sperm injection marked variability between countries.Hum Reprod Update,2008,14:593-604.
2 Simopoulou M,Gkoles L,Bakas P,et al. Improving ICSI:A review from the spermatozoon perspective.Syst Biol Reprod Med,2016,62:359-371.
3 Jeyendran RS,Caroppo E,Rouen A,et al.Selecting the most competent sperm for assisted reproductive technologies.Fertil Steril,2019,111:851-863.
4 Said TM,Land JA.Effects of advanced selection methods on sperm quality and ART outcome:a systematic review.Hum Reprod Update,2011,17:719-733.
5 Liu DY,Garrett C,Baker HW,et al. Low proportions of sperm can bind to the zona pellucida of human oocytes.Hum Reprod,2003,18:2382-2389.
6 Pang PC,Chiu PC,Lee CL,et al.Human sperm binding is mediated by thesialyl-Lewis(x) oligosaccharide on the zona pellucida.Science,2011,333:1761-1764.
7 Clark GF.The role of carbohydrate recognition during human sperm-egg binding.Hum Reprod,2013,28:566-577.
8 Ganguly A,Bukovsky A,Sharma RK,et al.In humans,zona pellucida glycoprotein-1 binds to spermatozoa and induces acrosomal exocytosis.Hum Reprod,2010,5:1643-1656.
9 Gupta SK.Role of zona pellucida glycoproteins during fertilization in humans.J Reprod Immunol,2015,4:90-97.
10 Chiu PC,Wong BS,Chung MK ,et al.Effects of native humanzona pellucida glycoproteins 3 and 4 on acrosome reaction and zona pellucida binding of human spermatozoa.Biol Reprod,2008,79:869-877.
11 Chiu PC,Wong BS,Lee CL ,et al.Native humanzona pellucida glycoproteins:purification and binding properties.Hum Reprod,2008,23:1385-1393.
12 Chiu PC,Lam K,Wong R,et al.The identity ofzona pellucida receptor on spermatozoa:an unresolved issue in developmental biology.Semin Cell Dev Biol,2014,7:86-95.
13 Clark GF.A role for carbohydrate recognition in mammalian sperm-egg binding.Biochem Biophys Res Commun,2014,450:1195-1203.
14 Maldera JA,Weigel Mu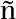 oz M,Chirinos M,et al.Human fertilization:epididymal hCRISP1 mediates sperm-zona pellucida binding through its interaction with ZP3.Mol Hum Reprod,2014,20:341-349.
oz M,Chirinos M,et al.Human fertilization:epididymal hCRISP1 mediates sperm-zona pellucida binding through its interaction with ZP3.Mol Hum Reprod,2014,20:341-349.
15 Petit FM,Serres C,Bourgeon F,et al.Identification of sperm head proteins involved in zona pellucida binding.Hum Reprod,2013,28:852-865.
16 宋力雯,汪玉宝.人类精卵结合与不育症的研究进展.中华男科学杂志,2005,11:611-614.
17 Avella MA,Xiong B,Dean J.The molecular basis of gamete recognition in mice and humans.Mol Hum Reprod,2013,19:279-289.
18 Liu DY,Baker HW.Defective sperm-zona pellucida interaction:a major cause of failure of fertilization in clinical in-vitro fertilization.Hum Reprod,2000,15:702-708.
19 Check JH,Bollendorf A,Wilson C.Failed fertilization with conventional oocyte insemination can be overcome with the ability of ICSI according to binding or failing to bind to the zona pellucida.Clin Exp Obstet Gynecol,2016,43:186-188.
20 Liu DY,Stewart T,Baker HW.Normal range and variation of the zona pellucida-induced acrosome reaction in fertile men.Fertil Steril,2003,80:384-389.
21 Garrett C,Liu DY,Baker HW.Comparison of human spermmorphometry assessment models based on zona pellucida selectivity.Soc Reprod Fertil Suppl,2007,65:357-361.
22 Paes Almeida Ferreira de Braga D,Iaconelli A Jr,CássiaSávio de Figueira R,et al. Outcome of ICSI using zona pellucida-bound spermatozoa and conventionally selected spermatozoa.Reprod Biomed Online,2009,19:802-807.
23 Abou-Haila A,Bendahmane M,Tulsiani DR.Significance of egg′s zona pellucida glycoproteins in sperm-egg interaction and fertilization.Minerva Ginecol,2014,66:409-419.
24 Liu DY,Baker HW.High frequency of defective sperm-zona pellucida interaction in in oligozoospermic infertile men.Hum Reprod,2004,19:228-233.
25 Ioannou D,Miller D,Griffin DK,et al. Impact of sperm DNA chromatin in the clinic.J Assist Reprod Genet,2016,33:157-166.
26 Liu DY,Baker HW.Human sperm bound to the zona pellucida have normal nuclear chromatin as assessed by acridine orange fluorescence.Hum Reprod,2007,22:1597-1602.
27 Liu DY.Could using the zona pellucida bound sperm for intracytoplasmic sperm injection (ICSI) enhance the outcome of ICSI?. Asian J Androl,2011,13:197-198.
28 Black M,Liu DY,Bourne H,et al. Comparison of outcomes of conventional intracytoplasmic sperm injection and intracytoplasmic sperm injection using sperm bound to the zona pellucida of immature oocytes.Fertil Steril,2010,93:672-674.
29 Liu F,Qiu Y,Zou Y,et al. Use of zona pellucida-bound sperm for intracytoplasmic sperm injection produces higher embryo quality and implantation than conventional intracytoplasmic sperm injection.Fertil Steril,2011,95:815-818.
30 Casciani V,Minasi MG,Fabozzi G,et al. Traditional intracytoplasmic sperm injection provides equivalent outcomes compared with human zona pellucida-bound selected sperm injection.Zygote,2014,22:565-570.
31 金锐,包俊华,白刚,等.精子透明带结合法优选精子行卵胞浆内单精子注射临床研究.生殖医学杂志,2013,22:155-158.
32 Jin R,Bao J,Tang D,et al.Outcomes of intracytoplasmic sperm injection using the zonapellucida-bound sperm or manually selected sperm.J Assist Reprod Genet,2016,33:597-601.
(收稿日期:2019-07-23)


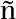 oz M,Chirinos M,et al.Human fertilization:epididymal hCRISP1 mediates sperm-zona pellucida binding through its interaction with ZP3.Mol Hum Reprod,2014,20:341-349.
oz M,Chirinos M,et al.Human fertilization:epididymal hCRISP1 mediates sperm-zona pellucida binding through its interaction with ZP3.Mol Hum Reprod,2014,20:341-349.