·生殖医学·
81例非预期卵巢低反应病例特点及危险因素分析
席思思 徐子衿 徐阳 尚鶄 王宁 薛晴
【摘要】 目的 分析卵巢储备功能正常患者在控制性卵巢刺激(COS)过程中出现非预期卵巢低反应的临床特征及危险因素。方法 回顾分析2012年1月至2017年12月于北京大学第一医院妇产科生殖中心接受体外受精-胚胎移植(IVF-ET)、单精子卵胞浆内注射(ICSI)辅助生殖技术治疗的发生非预期卵巢低反应的卵巢储备功能正常患者,年龄<40岁,基础卵泡刺激素(FSH)<10 IU/L,双侧窦卵泡数(AFC) 7~20个。根据年龄、基础FSH、AFC、COS方案选择同期行IVF/ICSI的卵巢正常反应患者进行1∶1配对,非预期卵巢低反应组(病例组)及卵巢正常反应组(对照组)各81个周期,比较两组的临床资料、治疗经过及妊娠结局。结果病例组体重、体重指数、基础FSH/黄体生成素均高于对照组(P均<0.05)。病例组促性腺激素(Gn)使用天数、绒毛膜促性腺激素(hCG)日雌二醇(E2)水平、hCG日孕酮水平、hCG日≥14 mm卵泡数低于对照组(P均<0.05),病例组hCG日孕酮卵泡比高于对照组(P<0.05)。病例组获卵数、MⅡ卵数、成胚数、优质胚胎数、可移植胚胎数及累积妊娠率均低于对照组(P均<0. 05)。条件Logistic回归分析显示,体重是发生卵巢非预期低反应的危险因素,基础LH是非预期卵巢低反应的保护因素。结论体重高、基础LH水平低的患者易发生非预期卵巢低反应,PFI值高、hCG日E2低及≥14 mm卵泡数少提示低获卵数及妊娠率。在制定COS方案时应结合多项指标评价卵巢功能,制定个体化的治疗方案,指导患者减轻体重或许可以减少非预期卵巢低反应的发生。
【关键词】 非预期卵巢低反应; 卵巢正常反应; 卵巢储备功能; BMI; 基础LH水平
作者单位:100034 北京,北京大学第一医院妇产科
通讯作者:薛晴(xueqingqq@hotmail.com)
Clinical characteristics and risk factors of unexpected poor ovarian response in 81 IVF / ICSI cycles
Xi Sisi, Xu Zijin, Xu Yang, Shang Jing, Wang Ning, Xue Qing.
Reproductive Medical Center of Obstetricsand Gynecology,Peking University First Hospital,Beijing 100034,China
[Abstract] Objective To study the clinical characteristics and risk factors of unexpected poor ovarian response in patients with normal ovarian reserve in IVF / ICSI cycles.MethodsThis study was focused on infertile women who were diagnosed with poor ovarian response but normal ovarian reverse, with an age < 40 years, follicle-stimulating hormone (FSH) < 10 IU/L and antral follicle count 7-20. A retrospective study was performed among the patients in Peking University First Hospital reproductive center from January 2012 to December 2017. The 81 cycles that had less than or equal to 3 retrieved oocytes were defined as studied cases. Each case was matched with one control cycle by age, basal FSH level, AFC and protocol of controlled ovarian stimulation (COS) and time of therapy. We examined between-group differences in terms of the clinical characteristics (in hCG day), process of therapy and pregnant outcomes.ResultsThe body weight, body mass index (BMI), basal FSH, and progesterone-to-follicle index (PFI) of case group were higher than that of control. Compared to the controls, the cases had a significantly lower level of gonadotropins days, estradiol, progesterone or counts of follicles ≥14 mm; and a significantly higher level of PFI. Additionally, cumulative pregnancy rate or number of retrieved oocytes, MII oocytes, embryos, high-quality embryos, or transplantable embryos was also significantly lower in cases than that in controls. Results of conditional logistic regression suggested that high BMI and low basal LH were risk factors of unexpected poor ovarian response.ConclusionHigh BMI and low basal LH increases the incidence of unexpected poor ovarian response. Higher PFI, lower estradiol, and smaller number of follicles ≥14 mm in the hCG day are associated with less retrieved oocytes and lower pregnancy rate. Individually specific COS need to be planned, according to evaluation of ovarian function. Losing weight may reduce the risk of unexpected poor ovarian response.
[Key words] unexpected poor ovarian response; normal ovarian response; ovarian reverse; BMI; basal LH level
卵巢低反应(poor ovarian response, POR)是卵巢对促性腺激素(gonadotropin, Gn)刺激反应不良的病理状态,主要表现为卵巢刺激周期发育的卵泡少、Gn用量多、获卵数少和临床妊娠率低,发生率在9%~26%[1]。高龄、子宫内膜异位症、卵巢手术及放疗史是导致卵巢反应性降低的重要因素。2015年中华医学会生殖医学分会发表的卵巢低反应专家共识指出“部分基础血清卵泡刺激素(FSH)及雌二醇(E2)等水平均正常、卵巢储备功能正常的患者,在超促排卵过程中出现POR,称为未预期的卵巢低反应(unexpected poor ovarian response)”[2]。此类卵巢非预期低反应患者在体外受精-胚胎移植(in vitro fertilization and embryo transplantation, IVF-ET)治疗前未能识别,只在控制性超促排卵(controlled ovarian hyperstimulation, COS)治疗中才体现出来[2]。能否在助孕治疗前通过评估患者资料、对患者的卵巢反应性全面预估并给予适宜的预处理及个体化的COS方案,是助孕成功的关键。目前针对非预期卵巢低反应的研究尚少,本文总结了北京大学第一医院妇产科生殖中心6年内发生的卵巢非预期低反应的临床资料,并与卵巢正常反应人群对比治疗经过及妊娠结局,旨在发现卵巢非预期低反应的危险因素,减少后续助孕患者的卵巢低反应的发生。
资料与方法
一、研究对象
回顾分析2012年1月至2017年12月于北京大学第一医院妇产科生殖中心接受IVF-ET、单精子卵胞浆内注射(intracytoplasmic sperm injection, ICSI)辅助生殖技术治疗的卵巢储备功能正常患者,排除输卵管积水、盆腔子宫内膜异位症、子宫腺肌症、子宫肌瘤、子宫内膜病变、卵巢肿瘤、卵巢手术史、多囊卵巢综合征及博洛尼亚共识预期POR患者[3]。
1.非预期卵巢低反应组(病例组):(1)年龄<40岁;(2)阴道超声提示早期双侧卵巢窦卵泡数(antral follicle count, AFC)7~20个;(3)FSH<10 U/L;(4)应用常规促排卵方案(不包括微刺激方案及自然周期取卵);(5)获卵数≤3个。本中心2012年至2017年6年内出现非预期卵巢低反应者共86个周期。
2.卵巢正常反应组(对照组):按照1∶1,对年龄、基础FSH、AFC、COS方案进行配对,选择同期(12个月内)行IVF/ICSI的卵巢正常反应组(获卵数≥4个)为对照组。配对标准为(1)年龄相差≤1岁;(2)AFC相差≤2个;(3)基础FSH相差≤1 U/L;(4)相同COS方案。匹配后病例组及对照组各81个周期(病例组余5个周期的患者资料未能与对照组匹配)。
二、COS方案
1. 短效降调长方案:黄体中期给予促性腺激素释放激素激动剂(gonadotropin releasing hormone agonist, GnRH-a) 进行垂体降调节,每日给予GnRH-a(曲普瑞林,0.1 毫克每支,辉凌制药有限公司;醋酸曲普瑞林,0.1毫克,法国易普生生物制药公司)0.1 毫克皮下注射,降调节16~18 d后开始应用个体化Gn(尿促性素,75 U每支,丽珠集团丽珠制药厂;尿促性素,75 U每支,辉凌制药;尿促卵泡素,75 U每支,丽珠集团丽珠制药厂;重组人促卵泡激素,75 U每支,默克雪兰诺有限公司)促进卵泡生长,Gn过程中GnRH-a用量减为每日0.05 毫克至注射人绒毛膜促性腺激素(hCG)日[4]。
2.减量降调长方案:月经周期第2~3天单次给予GnRH-a(醋酸曲普瑞林,3.75 毫克每支,法国易普生生物制药公司)0.94 毫克肌肉注射进行垂体降调节,注射后21 d若降调效果满意开始Gn促排卵治疗,应用Gn第5天起每日加用GnRH-a(曲普瑞林,0.1 毫克每支,辉凌制药有限公司;醋酸曲普瑞林,0.1 毫克,法国易普生生物制药公司)0.05 毫克至应用hCG日[5]。
3. 长效降调长方案:月经周期第2~3天单次给予GnRH-a(醋酸曲普瑞林,每支3.75 毫克,法国易普生生物制药公司)3.75 毫克肌肉注射进行垂体降调节,注射后28 d若降调效果满意开始Gn促排卵治疗[4]。
4. 半剂量超长降调方案:黄体中期给予GnRH-a(醋酸曲普瑞林,3.75 毫克/支,法国易普生生物制药公司)1.8毫克肌肉注射进行垂体降调节,于注射后28 d再次给予GnRH-a 1.8毫克肌肉注射,第二次注射后14 d评价降调效果,若降调效果满意开始Gn促排卵治疗[4]。
5. 拮抗剂方案:月经周期第2~3天开始给予Gn促进卵泡生长,当主导卵泡直径≥14 mm加用促性腺激素释放激素拮抗剂(gonadotropin releasing hormone antagonist, GnRH-ant)(注射用醋酸西曲瑞克,0.25毫克/支,德国百特)0.25毫克/天至hCG日[4]。
三、取卵、受精及胚胎移植过程
当2~3个主导卵泡直径≥18 mm时,予皮下注射hCG(重组人绒毛膜促性腺激素,250 微克每支,雪兰诺公司)250 微克,注射后36 h时取卵。根据男方精液情况选择IVF或ICSI方式受精,取卵后第3天予行胚胎移植。移植后28 天行经阴道超声检查,若于宫内见孕囊并见胎心考虑临床妊娠。
四、评价指标
根据BMI(body mass index)、不孕类型、不孕年限、基础FSH、基础LH、基础E2及AFC情况评价两组基线情况。比较两组Gn用量、Gn天数、LH用量、hCG日血清LH、hCG日血清E2、hCG日血清孕酮(P)、hCG日≥直径1.4 cm卵泡数、PFI(progesterone-to-follicle index, hCG日孕酮/直径≥1.4 cm卵泡数)、获卵数、MⅡ卵数、胚胎数、优胚数、可移植胚胎数、鲜胚移植率、种植率、临床妊娠率、流产率、累积妊娠率等指标,评价治疗经过及临床结局。优胚判定标准[5]:(1)卵裂球均一、无多核、空泡等现象;(2)碎片≤20%;(3)7~9细胞胚胎。
五、统计学处理
数据应用SPSS 24.0进行统计分析。因两组患者的临床资料数据为偏态分布,计量资料采用中位数、四分位数表示,计数资料采用例数、百分比表示。两组计量数据应用Mann-Whitney检验比较,计数资料应用χ2检验及Fisher精确检验比较。对可能的导致卵巢非预期低反应的危险因素进行条件Logistic回归分析。P<0.05为差异有统计学意义。
结 果
一、基线情况
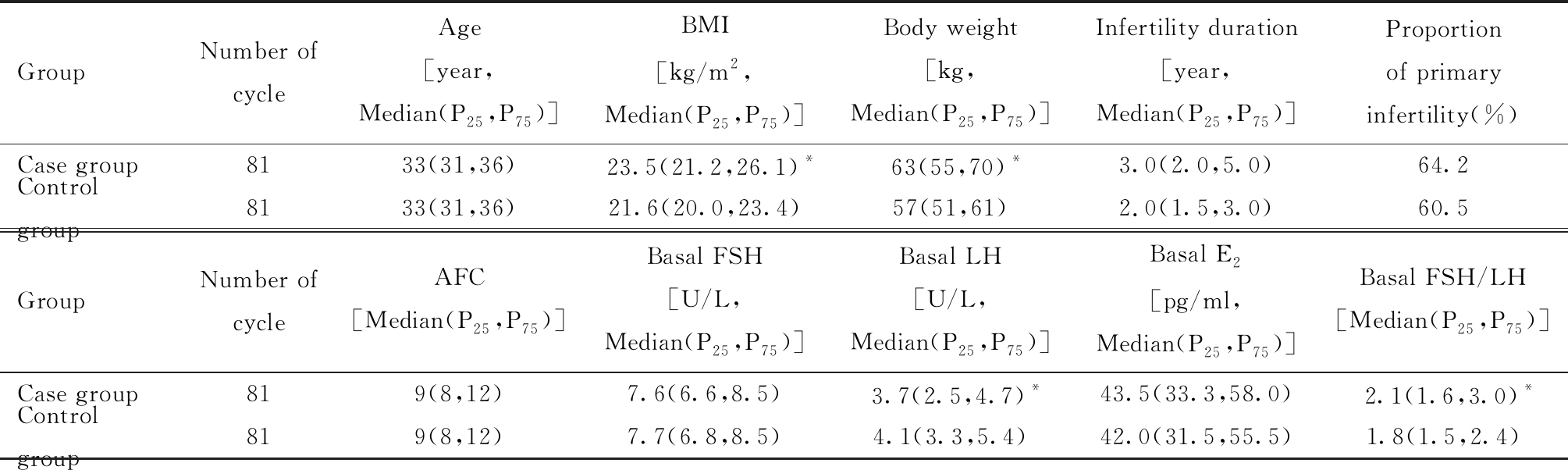
病例组及对照组各81个周期纳入分析,病例组BMI、体重、基础FSH/LH值高于对照组,病例组基础LH值低对照组,差异均有统计学意义;余各项指标差异无统计学意义。见表1。
二、治疗经过
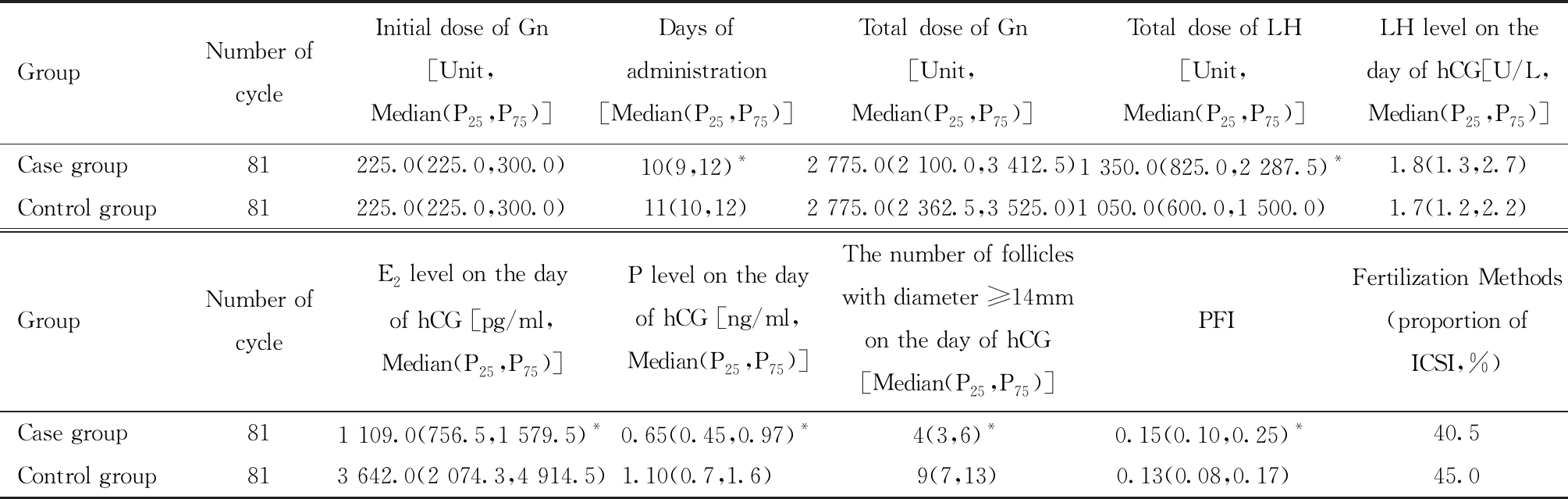
病例组及对照组COS方案分布相同,两组中短效降调长方案各22个周期,减量降调长方案各32个周期,长效降调长方案各1个周期,半剂量超长降调方案各6个周期,拮抗剂方案各20个周期。两组Gn启动量、Gn总量、hCG日血清LH值、ICSI比例差异无统计学意义。病例组Gn天数、hCG日血清E2、hCG日血清孕酮、hCG日≥14 mm卵泡数低于卵巢正常反应组,LH用药总量、PFI高于卵巢正常反应组。见表2。
三、临床结局
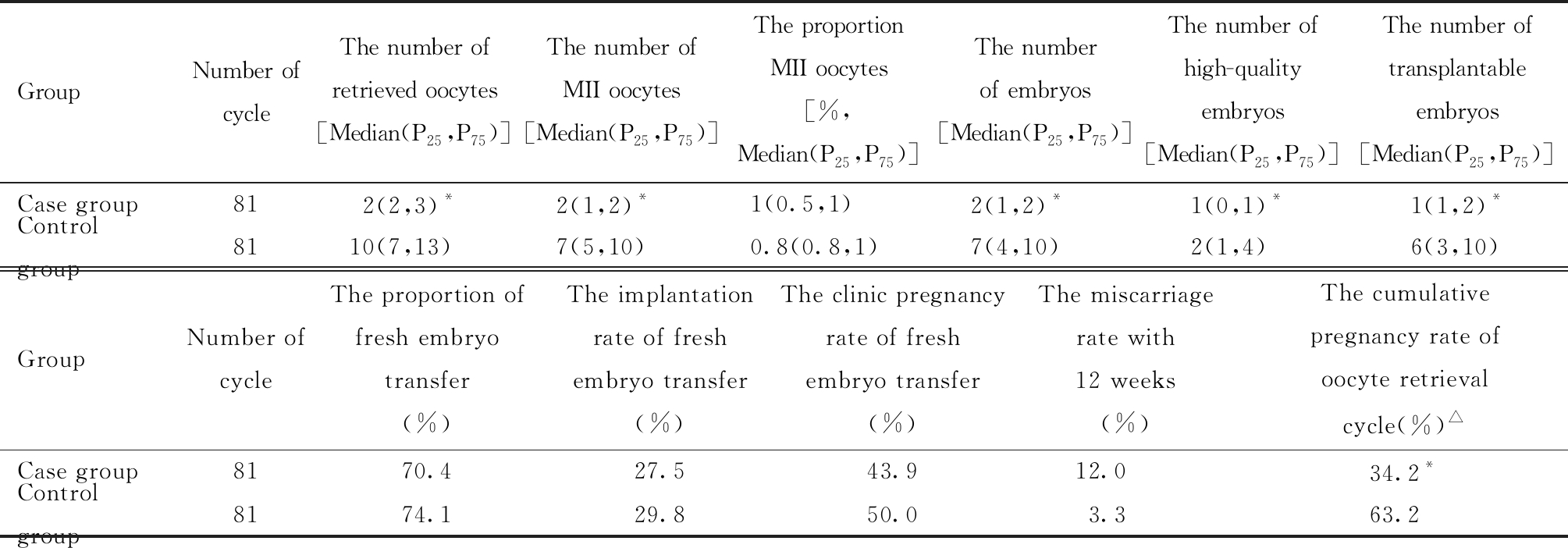
病例组获卵数、MⅡ卵数、成胚数、优质胚胎数、可移植胚胎数低于对照组(见表3)。病例组的鲜胚移植率、种植率、临床妊娠率、流产率与对照组相近,累积妊娠率显著低于对照组(见表3)。病例组取消鲜胚移植的原因前2位为无可移植胚胎(54.2%)、累积胚胎(33.3%)。对照组取消鲜胚移植的原因前2位为预防卵巢过度刺激(66.7%)、累积胚胎(9.5%)。将患者BMI、体重、基础LH、基础FSH/LH(以上4项为连续变量)、用药方案(根据是否进行降调节转换为分类变量)5项进行条件Logistic回归分析(筛选方法:前进法LR,筛选标准:P<0.05),结果显示,体重是非预期卵巢低反应的危险因素,基础LH是保护因素(见表4)。
表1 基线情况
Table 1 Summary of baseline characteristics
GroupNumber of cycleAge[year,Median(P25,P75)]BMI[kg/m2,Median(P25,P75)]Body weight[kg,Median(P25,P75)]Infertility duration[year,Median(P25,P75)]Proportion of primary infertility(%)Case group8133(31,36)23.5(21.2,26.1)*63(55,70)*3.0(2.0,5.0)64.2Control group8133(31,36)21.6(20.0,23.4)57(51,61)2.0(1.5,3.0)60.5GroupNumber ofcycleAFC[Median(P25,P75)]Basal FSH[U/L,Median(P25,P75)]Basal LH[U/L,Median(P25,P75)]Basal E2[pg/ml,Median(P25,P75)]Basal FSH/LH[Median(P25,P75)]Case group819(8,12)7.6(6.6,8.5)3.7(2.5,4.7)*43.5(33.3,58.0)2.1(1.6,3.0)*Control group819(8,12)7.7(6.8,8.5)4.1(3.3,5.4)42.0(31.5,55.5)1.8(1.5,2.4)
Compared with control group,*P<0.05
表2 治疗经过
Table 2 Summary of treatment indicators
GroupNumber of cycleInitial dose of Gn[Unit,Median(P25,P75)]Days of administration[Median(P25,P75)]Total dose of Gn[Unit,Median(P25,P75)]Total dose of LH[Unit,Median(P25,P75)]LH level on the day of hCG[U/L,Median(P25,P75)]Case group81225.0(225.0,300.0)10(9,12)*2 775.0(2 100.0,3 412.5)1 350.0(825.0,2 287.5)*1.8(1.3,2.7)Control group81225.0(225.0,300.0)11(10,12)2 775.0(2 362.5,3 525.0)1 050.0(600.0,1 500.0) 1.7(1.2,2.2)GroupNumber of cycleE2 level on the day of hCG [pg/ml,Median(P25,P75)]P level on the day of hCG [ng/ml,Median(P25,P75)]The number of follicles with diameter ≥14mm on the day of hCG [Median(P25,P75)]PFIFertilization Methods (proportion of ICSI,%)Case group811 109.0(756.5,1 579.5)*0.65(0.45,0.97)*4(3,6)*0.15(0.10,0.25)* 40.5Control group813 642.0(2 074.3,4 914.5)1.10(0.7,1.6) 9(7,13)0.13(0.08,0.17) 45.0
Compared with control group,*P<0.05
表3 临床结局
Table 3 Summary of clinical outcomes
GroupNumber ofcycleThe number of retrieved oocytes[Median(P25,P75)]The number of MII oocytes[Median(P25,P75)]The proportion MII oocytes[%,Median(P25,P75)]The number of embryos[Median(P25,P75)]The number of high-quality embryos[Median(P25,P75)]The number of transplantable embryos[Median(P25,P75)]Case group812(2,3)*2(1,2)*1(0.5,1)2(1,2)*1(0,1)*1(1,2)*Control group8110(7,13)7(5,10)0.8(0.8,1)7(4,10)2(1,4)6(3,10)GroupNumber ofcycleThe proportion of fresh embryo transfer(%)The implantation rate of fresh embryo transfer(%)The clinic pregnancy rate of fresh embryo transfer(%)The miscarriage rate with 12 weeks(%)The cumulative pregnancy rate of oocyte retrieval cycle(%)△Case group8170.427.543.912.034.2*Control group8174.129.850.03.363.2
Compared with control group,*P<0.05;△5 cycles in case group and 5 cycles in control group were not involved in the statistical analysis of the cumulative pregnancy rate because there were frozen embryos which have not yet been transferred yet
表4 卵巢非预期低反应多因素条件Logistic回归分析结果
Table 4 The estimated risk factors of unexpected poor ovarian response,
by the conditional logistic regression with multiple adjustments

FactorParameter(B)SEWaldPOR95% CIBMI0.070.0212.20<0.0011.071.03-1.11Basal LH level-0.330.127.270.010.720.57-0.92
讨 论
卵巢反应性与助孕结局密切相关。卵巢反应性与年龄、卵巢储备功能、卵巢手术史、卵巢放化疗史、子宫内膜异位症、COS方案、预处理治疗等多种因素密切相关。2011年欧洲人类胚胎与生殖学会在博洛尼亚形成了POR诊断的共识标准[3]:(1)高龄(≥40 岁)或存在其他卵巢反应不良的危险因素;(2)前次IVF周期常规方案获卵数≤3个;(3)卵巢储备下降(AFC<5~7个或AMH<0.5~1.1 mg/L);如果年龄<40岁或卵巢储备功能检测正常,患者连续2个周期应用最大化的卵巢刺激方案仍出现POR也可诊断;至少满足以上2条即可诊断为POR。近期国内研究显示,博洛尼亚标准中“预期的卵巢低反应者”在首次IVF/ICSI促排卵周期出现低反应的可能性极大,第二次促排卵周期再次出现低反应的可能降低至67.2%~71.4%[6]。再次促排卵周期出现低反应比例下降其原因与临床医师对患者前次周期低反应史的重视及再次超促排卵的治疗方案调整密切相关。能否在超促排卵前识别到低反应的可能性并及早给予干预是本研究开展的出发点。本研究显示非预期卵巢低反应组累积妊娠率约为卵巢正常反应组的1/2,采取措施减少非预期卵巢低反应的发生意义重大。
本研究的目标人群是卵巢刺激周期中卵巢储备功能正常却发生卵巢低反应的群体,除外既往卵巢手术史、子宫内膜异位症疾病的患者,将病例组与对照组在年龄、AFC、基础FSH方面进行匹配,减少卵巢储备功能差异对获卵及妊娠情况的影响。两组选取同期行IVF/ICSI治疗病例,选取相同的COS方案,减少用药方案及实验室或手术者因素对结局的影响。结果提示,非预期卵巢低反应组基础FSH/LH值高于对照组,基础LH低于对照组,这提示评价卵巢功能应采用多参数评估,不应仅关注基础FSH水平,还应关注基础LH水平。既往研究指出,一定浓度的基础LH是卵泡募集及发育过程中所必需的,基础FSH/LH值比单纯FSH值预测卵巢反应性更为准确,基础FSH/LH>2的患者卵巢反应下降[7],IVF周期取消率更高[8]。在FSH正常的患者群中,LH降低导致FSH/LH比例升高,而与基础LH水平低伴随出现的是IVF治疗的低获卵率、低妊娠率[9-10]。还有研究提示,基础LH小于3 U/L是POR的预测指标,该组人群接受COS治疗的雌激素峰值低、直径大于15 mm的卵泡数少,其原因推测可能与垂体与卵巢的相互作用失衡有关[11]。随着AMH的广泛应用,AMH与AFC成为临床评价临床反应性重要指标。文献提示AMH是卵巢反应性的有效独立预测因子[12-13],但因本研究是回顾性分析2012年至2017年的临床资料,而2016年以前本中心未开展AMH检查,所以评价卵巢反应性的主要靠性激素及AFC。在后续的临床工作中,应当重视AMH检查,选择适宜的治疗方案。对两组的基础资料分析还提示卵巢低反应组BMI及体重均高于对照组,既往研究也提示30~39岁女性群体BMI升高与卵巢体积呈负相关[14],随着体重指数的增加,生育力下降,所以动员并指导超重、肥胖患者在进入周期前减重势在必行。本研究中卵巢非预期低反应组患不孕症时间较对照组稍长(但差异未达统计学显著水平),既往研究未见相关报道,分析其原因不孕时间长可能与患有更多的不孕因素相关,进而可能影响助孕结局。
LH活性在卵母细胞的发育过程中发挥着重要的生物学作用,卵泡发育过程中过低的LH 会导致雌激素合成分泌障碍,进而影响卵泡的发育及成熟。既往研究显示,卵巢低反应患者在卵泡募集早期添加LH能够改善卵子成熟度和受精率,从而提高可以用胚胎率[2]。本研究中非预期卵巢低反应组促排卵过程中LH药物用量高于卵巢正常反应组,提示在促排卵过程中临床医师发现卵巢反应不佳的趋势时可能已经适当增加了LH用量,但未能逆转临床结局,今后针对基础LH偏低但FSH正常的患者,可尝试早期添加LH。本研究结果显示两组的Gn用药总量无明显差异,后续治疗过程中适当增加Gn用量或可改善临床结局[2]。既往研究还提示,Gn启动量对于卵巢反应性有一定作用,选择合理的Gn用量可以得到更多的获卵数[15],也有研究提示过高的Gn启动量不改善临床妊娠结局[16]。本研究中两组Gn启动量无明显差异,但非预期卵巢低反应组的体重值高于卵巢正常反应组,回归分析显示,体重是卵巢低反应的危险因素,在今后的临床工作中,应注意对体重较大的患者适当增加Gn启动量,或许能改善临床结局。
本研究中,卵巢正常反应组hCG日孕酮值稍高于卵巢低反应组,推测是由于卵巢正常反应组较多卵泡发育成熟分泌孕酮累积的结果。过高的孕酮与妊娠率降低相关,近年来,有学者提出PFI概念,并证实该比值与单纯孕酮值相比,对临床结局预测更加准确,高PFI组获卵数低[17-18]。本研究中非预期卵巢低反应组PFI值高于对照组、获卵数低于对照组,与既往文献报道一致[17]。
本研究存在一定的局限性:首先,本研究涉及样本量尚少,人群代表性仍有限,后续研究应扩大样本量;第二,本中心2012—2016年未普遍开展AMH的检查,研究未涉及患者的AMH资料,后续研究应完善该部分临床资料总结,总结治疗经验;第三,截至研究统计阶段,仍有10个周期存有冻胚未移植,研究统计的累积妊娠率为其余152个周期的临床妊娠情况。
综上所述,卵巢反应性与多种因素相关。体重高、基础LH水平低的患者易发生非预期卵巢低反应,PFI值高、hCG日E2低及hCG日≥14 mm卵泡数少提示低获卵数及妊娠率。在制定COS方案时应结合多项指标评价卵巢功能,制定个体化的治疗方案,指导患者减轻体重或许可以减少非预期卵巢低反应的发生。超促排卵治疗前及时识别潜在的卵巢低反应并提前给予干预,进而改善妊娠结局是生殖医学工作者的重要任务。
参考文献
1 Vollenhoven B,Osianlis T,Catt J.Is there an ideal stimulation regimen for IVF for poor responders and does it change with age?.J Assist Reprod Genet,2008,25:523-529.
2 武学清,孔蕊,田莉,等.卵巢低反应专家共识.生殖与避孕,2015,35:71-79.
3 Ferraretti,AP,La Marca A,Fauser BC,et al.ESHRE consensus on the definition of ‘poor response′ to ovarian stimulation for in vitro fertilization:the Bologna criteria.Hum Reprod,2011,26:1616-1624.
4 胡琳莉,黄国宁,孙海翔,等.促排卵药物使用规范(2016).生殖医学杂志,2017,26:302-307.
5 席思思,杨慕坤,曾诚,等.减量降调长方案与拮抗剂方案在卵巢储备功能低下患者中的临床疗效观察.中国实用妇科与产科杂志,2018,34:559-562.
6 柯慧,颜礼征.博洛尼亚标准卵巢低反应者在促排卵体外受精/卵胞质内单精子注射周期中的卵巢反应性.中华生殖与避孕杂志,2018,38:5-10.
7 余照娟,郭培培,黄苗苗,等.不同年龄段患者基础FSH/LH比值对IVF/ICSI-ET临床结局的预测价值.安徽医科大学学报,2017,52:269-272.
8 LiuKE,Greenblatt EM.Elevated day 3 follicle-stimulating hormone/luteinizing hormone ratio≥2 is associated with higher rates of cancellation in in vitro fertilization-embryo transfer cycles.Fertil Steril,2008,90:297-301.
9 Seckin B,Turkcapar F,Ozaksit G.Elevated day 3 FSH/LH ratio:a marker to predict IVF outcome in young and older women.J Assist Reprod Genet,2012,29:231-236.
10 Shrim A,Elizur SE,Seidman DS,et al.Elevated day 3 FSH/LH ratio due to low LH concentrations predicts reduced ovarian response.Reprod Biomed Online,2006,12:418-422.
11 Noci I,Biagiotti R,Maggi M,et al.Low day 3 luteinizing hormone values are predictive of reduced response to ovarian stimulation.Hum Reprod,1999,14:863-864.
12 黄会霞,于医萍,冯艳奇,等.基础抗苗勒管激素在卵泡期长效促性腺激素释放激素激动剂长方案中对卵巢反应性及妊娠结局的预测价值.中华生殖与避孕杂志,2018,38:351-356.
13 Nardo LG,Gelbaya TA,Wilkinson H,et al.Circulating basal anti-Mullerian hormone levels as predictor of ovarian response in women undergoing ovarian stimulation for in vitro fertilization.Fertil Steril,2009,92:1586-1593.
14 Zaidi S,Usmani A,Shokh IS,et al.Ovarian reserve and BMI between fertile and subfertile women.J Coll Physicians Surg Pak,2009,19:21-24.
15 Allegra A,Marino A,Volpes A,et al.A randomized controlled trial investigating the use of a predictive nomogram for the selection of the FSH starting dose in IVF/ICSI cycles.Reprod Biomed Online,2017,34:429-438.
16 陈艳,周爱莲.卵巢低反应者减量降调节并控制Gn启动剂量的体外受精结局.国际生殖健康/计划生育杂志,2018,37:28-31.
17 Shufaro Y,Sapir O,Oron G,et al.Progesterone-to-follicle index is better correlated with invitro fertilization cycle outcome than blood progesterone level.Fertil Steril,2015,103:669-674.e3.
18 Chen Y,Ma L,Wang S.The impact of an increased progesterone-to-follicle number ratio on live delivery rates in women with normal ovarian reserve.J Int Obstet Gynecol,2017,139:84-89.
(收稿日期:2019-07-29)



