子宫内膜不典型增生(atypical endometrial hyperplasia,AEH)是一种癌前病变,其发病主要与雌激素对子宫内膜的长期持续刺激有关。有大量研究表明,若不进行干预治疗,在15年内约三分之一的患者可发展为子宫内膜癌[1],甚至有研究显示其癌变率可高达50.0%[2]。近年来AEH发病率在世界范围内持续升高,发病趋于年轻化,且AEH患者合并不孕者达 22.0%~66.0%[3-5]。对于要求保留生育功能或无法手术的患者,有效的保守治疗方案十分重要。近年来,国内外保守治疗AEH的方案主要有口服孕激素、使用左炔诺孕酮宫内节育系统(LING-IUS,曼月乐)及促性腺激素释放激素(GnRHa)。本研究对曼月乐、孕激素及GnRHa治疗AEH患者子宫内膜逆转情况及临床疗效进行研究对比。
资料与方法
1. 一般临床资料:回顾性收集2016年1月—2018年4月就诊于哈尔滨医科大学附属第一医院,病理确诊为AEH且符合入选标准的75例患者资料。入选标准:(1)子宫内膜组织由本院病理科确诊为AEH;(2)年龄≤45岁,要求保守治疗;(3)近3个月内未规律服用激素类药物;(4)排除心脑血管疾病、肝肾功能异常、血液系统疾病及自身免疫系统等疾病的影响。(5)排除因个人原因终止治疗患者。
2. 研究方法:根据治疗方式不同分为三组,使用曼月乐治疗者为曼月乐组,孕激素治疗者为孕激素组,GnRHa治疗者为GnRHa组,每组各25例患者。所有患者均签署了知情同意书。三组患者治疗周期均为六个月,每治疗三个月行诊刮术一次,共两次。曼月乐组患者于月经期3~7日内将曼月乐放置宫腔内,经B超确定环的位置正常。患者于上环后三个月行第一次取环诊刮术,术后再次上环;三个月后第二次行取环诊刮术。孕激素组患者口服醋酸甲地孕酮或醋酸甲羟孕酮治疗,每日160~320 mg,连续口服三个月后行诊刮术;再次口服三个月后行第二次诊刮术。GNRHa组患者于月经期第2日给予GnRHa皮下注射,每间隔28日注射一次,3个周期后行诊刮术一次,共使用6个周期。三组患者均以治疗6个月后的诊刮病理结果作为最终疗效评价,同时记录6个月治疗期内患者的不良反应发生情况。
3. 临床观察指标:(1)子宫内膜逆转定义。有效:增生消失,内膜腺体萎缩,间质呈蜕膜样变;缓解:残留增生内膜,无不典型细胞残留或病理级别降低;无效:组 织 病 理 学 与 治 疗 前 相 同或加重。有效率=(有效例数+缓解例数)/每组总例数×100%。(2)不良反应发生情况。主要包括:阴道不规则流血,体重增加,恶心、呕吐,潮热盗汗、骨质缺失等更年期症状以及肝肾功能异常。不良反应发生率=不良反应发生例数/每组总例数×100%。
4. 统计学方法:使用SPSS 22.0统计软件包,计量资料采用![]() 表示,组间比较采用方差分析,计数资料采用构成比或率(%)表示,组间比较采用卡方检验,P<0.05表示差异具有统计学意义。
表示,组间比较采用方差分析,计数资料采用构成比或率(%)表示,组间比较采用卡方检验,P<0.05表示差异具有统计学意义。
结果
1.一般资料比较:患者一般临床资料无统计学差异,具有可比性,详见表1。
表1 三组间一般情况比较![]()

组别年龄(岁)体重指数(kg/m2)曼月乐组36.2±3.226.4±2.5孕激素组35.4±2.827.5±3.4GNRHa组36.8±4.626.8±5.2
2. 三组患者子宫内膜逆转情况比较:分析最终子宫内膜病理情况,三组间子宫内膜逆转有效率比较,差异具有统计学意义。两两比较结果显示,曼月乐组有效率大于孕激素组和GNRHa组,差异有统计学意义;孕激素组和GNRHa组之间差异无统计学意义。详见表2。
表2 三组间最终子宫内膜逆转有效率比较[例(%)]

组别有效缓解无效有效率∗曼月乐组9(36.0)14(56.0)2(8.0) 23(92.0)孕激素组9(36.0)10(40.0)6(24.0)19(76.0)#GNRHa组8(32.0)10(40.0)7(28.0)18(72.0) #
注:三组间比较,*P<0.05;与曼月乐组比较,#P<0.05
3. 三组患者不良反应发生情况比较:三组间不良反应发生率比较,差异无统计学意义,说明三组不良反应发生情况相似。但在随访过程中发现使用曼月乐治疗不良反应较其他组轻,均可耐受。详见表3。
表3 组间不良反应发生率比较[例(%)]
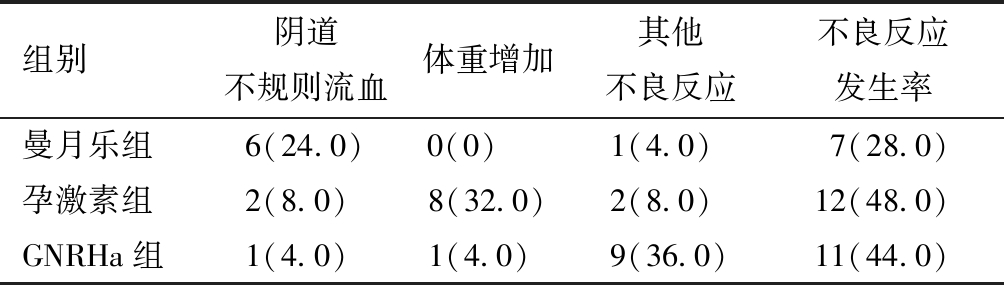
组别阴道不规则流血体重增加其他不良反应不良反应发生率曼月乐组6(24.0)0(0) 1(4.0) 7(28.0)孕激素组2(8.0) 8(32.0)2(8.0) 12(48.0)GNRHa组1(4.0) 1(4.0) 9(36.0)11(44.0)
讨论
针对无生育要求及绝经期患者,AEH的主要手术方式是筋膜外全子宫及双附件切除±盆腔及腹主动脉旁淋巴结切除[6],这种手术治疗方式的治愈率较高。由于AEH的发病率不断升高,且趋于年轻化,保留生育功能越来越重要,手术治疗会丧失生育能力的弊端导致很多患者选择保守治疗,因此为患者寻找更加有效安全的治疗方案是目前妇科医生所面临的挑战。
当前,针对AEH患者保留生育功能治疗的主要方法是大剂量口服孕激素,孕激素被认为能诱导抑制细胞转化和肿瘤进展的信号通路,醋酸甲地孕酮和醋酸甲羟孕酮已被广泛应用且疗效肯定[7-8],但在治疗中使用的剂量以及用药的时长等方面还没有具体的统一规范。长期大剂量口服孕激素导致的最明显的弊端是比较严重的副反应,如恶心呕吐、体重增加、乳房胀痛、肝肾功能损伤等,在本次研究随访中出现最多的不良反应为体重增加,达32.0%,此外有2例出现了阴道不规则流血,2例出现了恶心及肝功异常。由此而导致患者的依从性差,难以继续接受治疗,严重影响了患者的身体健康及心理状态,并限制了整体疗效[9]。近年来,GnRHa和曼月乐逐渐在AEH患者保留生育功能的临床治疗中得到应用,这两种治疗方案在使用上更加方便,并且不良反应也比较小,治疗效果也更确切[10-11]。
GnRHa是人工合成的GnRH衍生物,通过抑制下丘脑-垂体-卵巢轴从而抑制卵巢功能,使体内雌激素水平降低,抑制子宫内膜增生。有研究对GnRHa与甲羟孕酮治疗AEH进行了研究,结果显示GnRHa与甲羟孕酮治疗的疗效相近,差异无统计学意义[12],与本次研究结果相符。相比较口服孕激素,GnRHa具有每月使用一次的优点,可提高患者的依从性,但另一方面,由于GnRHa价格较贵、容易导致更年期症状及骨质丢失等原因导致无法长期使用。GnRHa的使用时间多在6月以内,并且停药后多有复发,停药后1.5~2年复发率为19%~25%[13]。本次研究中发现使用GnRHa治疗的患者中有36.0%出现了更年期症状,如潮热、盗汗及缺钙症状,患者对此表示有些不适,降低了生活质量。
本研究结果显示使用曼月乐治疗后子宫内膜逆转率达92.0%,明显高于孕激素组(76.0%)及GnRHa(72.0%),差异有统计学意义。而且曼月乐治疗具备可长期使用的优点。在2016年,英国皇家妇产科医师学院(royal college of obstetricians and gynaecologists,RCOG)和英国妇科内镜学会联合发布的《子宫内膜增生管理指南》中提出将曼月乐作为治疗AEH的首选方案[14]。美国国立综合癌症网络(national comprehensive cancer network,NCCN)指南也已经将曼月乐列为子宫内膜癌保守治疗方法之一。曼月乐由一个T型塑料支架构成,含有52 mg左炔诺酮,每日24 h持续且恒定释放20 μg左炔诺孕酮进入宫腔,有效期为5年[15]。释放的药物直接作用于子宫内膜,使其在内膜局部组织中的浓度高达470~1 500 ng/mL,抑制子宫内膜生长,导致内膜萎缩,使间质水肿和蜕膜样变,粘膜变薄,同时使上皮失去活性,血管受抑[16]。同时有少量的左炔诺孕酮(10%)释放入血,使低浓度的左炔诺孕酮持续存在于血液中,对下丘脑-垂体-卵巢轴产生影响,抑制排卵,平稳抑制子宫内膜的过度增殖[17-18]。有文献[18]表明,曼月乐内膜逆转率较口服孕激素高,且大大降低了全身用药所引起的体重增加、胃肠道反应、肝肾功能损伤等风险。其原因可能为:首先,孕激素的使用途径不同,口服孕激素在肝脏第一次代谢后通过血液作用于子宫内膜,其生物利用度约为5.2%,相比之下,曼月乐通过扩散直接作用于子宫内膜,在子宫内膜中,左炔诺孕酮作用的浓度是口服孕激素的100倍以上。其次,孕激素对子宫内膜的作用时间长短不一,左炔诺孕酮持续作用于子宫内膜,而口服孕激素仅在服用期间发挥作用。此外,曼月乐的依从率高于口服孕激素[19-20],可有效、持续地治疗AEH。但在Marnach[21]和Hubbs[22]等人的研究中发现使用曼月乐与孕激素治疗AEH相比,在子宫内膜逆转率上没有明显的差异,但使用曼月乐治疗的患者副作用小,子宫内膜可处在平稳抑制及受保护的状态,效果较优。相比较,口服孕激素更多导致了体重增加,GnRHa更多导致了更年期症状,均降低了患者的依从性及满意度。但是三组患者不良反应发生率无统计学差异,可能与本次实验样本量较小有关,待今后的大样本前瞻性研究证实。
近年来AEH的保守治疗逐渐增多,但在患者要求保守治疗时,应充分告知患者不典型子宫内膜增生有进展为子宫内膜癌的风险。在保守治疗期间应定期严格复查,治疗期间应每3个月进行一次子宫内膜活检,若连续2次病理为阴性,可间隔6~12个月随访一次,且需要长期随访,随访中出现疾病进展应及时更改治疗方案,避免病情进一步发展[23-24]。
综上所述,在AEH的保守治疗上,相比较孕激素及GnRHa,曼月乐能更有效地逆转AEH,且不良反应相对较轻,是治疗AEH的一种安全有效的方案,建议推广。
1 Kalogera E,Dowdy SC,Bakkum Gamez JN.Preserving fertility in young patients with endometrial cancer:current perspectives.Int J Womens Health,2014,6:691-701.
2 李龙,王月玲.子宫内膜增生与子宫内膜上皮内瘤变的临床病理分析.陕西医学志,2013,6:733-734.
3 Zhang Q,Qi G,Kanis MJ,et al.Comparison among fertility-sparing therapies for well differentiate early-stage endometrial carcinoma and complex atypical hyperplasia.Oncotarget,2017,8:57642-57653.
4 Committee on Gynecologic Practice,Society of Gynecologic Oncology.The American College of Obstetricians and Gynecologists Committee Opinion no.631. Endometrial intraepithelial neoplasia.Obstet Gynecol,2015,125:1272-1278.
5 唐世倩,李慧,张宇迪,等.子宫内膜不典型增生及早期子宫内膜癌患者保留生育功能的相关研究进展.北京医学杂志,2015,37:680-683.
6 Koh WJ,Abu-Rustum NR,Bean S,et al.Uterine Neoplasms,Version 1.2018,NCCN clinical practice guidelines in oncology.J Natl Compr Canc Netw,2018,16:170-199.
7 Guttinger A,Critchley HO.Endometrial effects of intrauterine levonorgestrel.Contraception,2007,75:S93-98.
8 苏椿淋,李昕,林金芳.子宫内膜不典型增生及早期子宫内膜样癌药物治疗的进展及前景.中华妇产科杂志,2015,9:715-717.
9 Kim MK,Seong SJ,Kim JW,et al.Management of endometrial hyperplasia with a levonorgestrel-releasing intrauterine system:A Korean gynecologic-oncology group study.Int J Gynecol Cancer,2016,26:711-715.
10 Laurelli G,Di Vagno G,Scaffa C,et al.Conservative treatment of early endometrial cancer:preliminary results of a pilot study.Gynecol Oncol,2011,120:43246.
11 Minig L,Franchi D,Boveri S,et al.Progestin intrauterine device and GnRH analogue for uterus-sparing treatment of endometrial precancers and well-differentiated early endometrial carcinoma in young women.Ann Oncol,2011,22:643-649.
12 宋宁,程迪,马晓欣,等.GnRH-a对子宫内膜非典型增生的治疗价值.现代肿瘤医学,2015,23:686-688.
13 全国卫生产业企业管理协会妇幼健康产业分会生殖内分泌学组.中国子宫内膜增生诊疗共识.生殖医学杂志,2017,10:6-9.
14 Royal College of Obstetricians andGynaecologists.Management of endometrial hyperplasia.Green-top guideline No.67 RCOG/BSGE joint guideline.London:RCOG Press,2016.
15 戚洁,范丽梅,路雪.左炔诺孕酮宫内缓释系统相关基础研究.中国妇幼保健,2015,30:3751-3754.
16 Vandenput I,Kuhne LC,Ewing PC,et al.Progesterone inhibits epithelial-to-mesenchymal transition in endometrial cancer.PLoS One 2012,7:e30840.
17 朱孝严,张炜旸,马慧芳,等.曼月乐在子宫内膜癌前病变中的应用进展.中国妇幼保健,2016,31:1568-1570.
18 El Behery MM,Saleh HS,Ibrahiem MA,et al.Levonorgestrel-releasing intrauterine device versus dydrogesterone for management of endometrial hyperplasia without atypia.Reprod Sci,2015,22:329-334.
19 赵楠,张萍.子宫内膜不典型增生患者保留生育功能的相关研究进展.中国计划生育和妇产科,2017,9:15-18.
20 Yuk JS,Song JY,Lee JH,et al.Levonorgestrel-releasing intrauterine systems versus oral cyclic medroxyprogesterone acetate in endometrial hyperplasia therapy:a meta-analysis.Ann Surg Oncol,2017,24:1322-1329.
21 Marnach ML,Butler KA,Henry MR,et al.Oral progestogens versus levonorgestrel-releasing intrauterine system for treatment of endometrial intraepithelial neoplasia.J Womens Health,2017,26:368.
22 Hubbs JL,Saig RM,Abaid LN,et al.Systemic and local hormone therapy for endometrial hyperplasia and early adenocarcinoma.Obstet Gynecol,2013,121:1172-1180.
23 Gallos ID,Krishan P,Shehmar M,et al.LNG-IUS versus oral progestogen treatment for endometrial hyperplasia:a long-term comparative cohort study.Hum Reprod,2013,28:2966-2971.
24 Corzo C,Santillan NB,Westin SN,et al.Updates on conservative management of endometrial cancer.J Minim Invasive Gynecol,2018,25:308.