目前,虽然乙肝免疫球蛋白(hepatitis B immunoglobulin,HBIG)联合乙肝疫苗对母婴阻断有效(阻断率>90%),仍存在部分垂直感染;尤其对于乙型肝炎病毒(hepatitis B virus,HBV)高载量者,婴儿感染率据报道可高达30%[1]。欧洲肝脏病学会(European Association for the Study of the Liver,EASL)管理指南(2017年)[2]、国内《乙型肝炎母婴阻断临床管理流程》[3]均推荐对高载量者行替诺福韦治疗。大量研究证实:孕期抗病毒应用替诺福韦能够减少病毒复制及感染,提高阻断效果[4-5]。而关于HBIG剂量不同方案的效果尚待进一步评价。虽然有研究[6]指出100 IU与200 IU的HBIG效用相当,但针对高HBV载量孕产妇,在应用替诺福韦的基础上是保持100 IU HBIG还是增加至200 IU,还有待明确。本研究分析替诺福韦前提下联合不同剂量HBIG在乙肝疫苗阻断母婴HBV传播中的效果,拟提供方案依据。现报告如下。
对象与方法
一、研究对象
1. 纳入排除标准:本研究为回顾性研究,选取2013年2月—2018年3月上海市公共卫生临床中心收治的HBV感染的高病毒载量妊娠妇女1000例。纳入标准:(1)中孕期HBV DNA>1×106 IU/mL;(2)乙肝病毒e抗原(HBV e Antigen,HBeAg)、乙肝病毒表面抗原(Hepatitis B Virus Surface Antigen,HBsAg)双阳;(3)符合HBV感染诊断[7];(4)年龄≥20岁;(5)接受抗病毒的孕期治疗,用药前胎儿生长情况经超声检查提示正常;(6)孕周<24周;(7)妊娠妇女充分知情。排除标准:(1)伴丙肝病毒、免疫缺陷病毒等感染或除此之外的传播性疾病;(2)孕期内分泌疾病、先兆流产史;(3)孕前6个月抗病毒用药史;(4)对替诺福韦禁忌者;(5)胎儿父亲(生物学)感染HBV;(6)非单胎妊娠;(7)肿瘤、凝血异常、肝硬化、肾病以及心、脑相关疾病;(8)精神疾病者。根据治疗方式分为乙肝免疫球蛋白100 IU组、乙肝免疫球蛋白200 IU组,各500例。二组一般资料比较,差异无统计学意义(P>0.05,表1)。
2. 治疗方法:乙肝免疫球蛋白100 IU组与乙肝免疫球蛋白200 IU组治疗方案见图1。妊娠妇女用药前确定肝功能正常;替诺福韦[葛兰素史克(天津)有限公司,国药准字H20153090,300 mg/片规格],HBIG(山东泰邦生物制品公司,国药准字S10930002,100 IU规格);乙肝疫苗使用剂型为国家标准。

图1 乙肝免疫球蛋白100IU组与乙肝免疫球蛋白200IU组治疗方案
Figure 1 The treatment plan of hepatitis B immunoglobulin 100IU group and hepatitis B immunoglobulin 200IU group
二、研究方法
1.收集资料:(1)基线资料:年龄、入组孕周、分娩史、基线与分娩前3d的HBV DNA(荧光定量PCR法所测)、丙氨酸转氨酶(alanine aminotransferase,ALT)(速率法所测)、HBeAg(ELISA法所测)、HBsAg(ELISA法所测)等。(2)新生儿情况(出生方式、1min Apgar评分等)。(3)不同时间(出生时、1月、7月)乙型肝炎表面抗体(hepatitis B surface antibody,抗-HBs)水平(化学发光微粒子免疫法)。(4)出生7月的HBeAg、HBsAg、抗-HBs阳性及阻断失败率。(5)干预过程不良反应。(6)两组随访24个月,统计HBV DNA阳性、抗-HBs阳性情况。
2.阻断失败标准[8]:出生7月后婴幼儿的HBsAg和(或)HBV DNA为阳性。
3. 统计学处理:采用统计软件SPSS 22.0分析数据,计数资料表示为%,行χ2检验;计量资料表示为![]() 行t检验;时点比较行重复测量方差分析。P<0.05为差异有统计学意义。
行t检验;时点比较行重复测量方差分析。P<0.05为差异有统计学意义。
结 果
一、一般资料比较
年龄、孕周、分娩史、HBV DNA等在乙肝免疫球蛋白100 IU组与乙肝免疫球蛋白200 IU组中比较,均无统计学差异,见表1。
表1 一般资料比较![]()

VariablesHBIG100 IU group(n=500)HBIG200 IU group(n=500)Age(year)27.5±3.627.2±3.8Gestational week at entry(week)22.2±1.422.3±1.5Childbirth history [n(%)]41.6(41.6)196(39.2)HBV DNA(Log10 IU/mL)7.9±0.67.8±0.5ALT(U/L)21.7±4.321.9±4.1HBeAg(Log10 IU/mL)3.1±0.13.1±0.2HBsAg(Log10 IU/mL)4.5±0.34.5±0.2HBV DNA(Log10 IU/mL)3.7±0.9∗3.8±0.8ALT(U/L)19.2±2.7∗19.4±2.9HBeAg(Log10 IU/mL)3.0±0.1∗3.0±0.2HBsAg(Log10 IU/mL)4.2±0.2∗4.2±0.1
二、新生儿情况比较
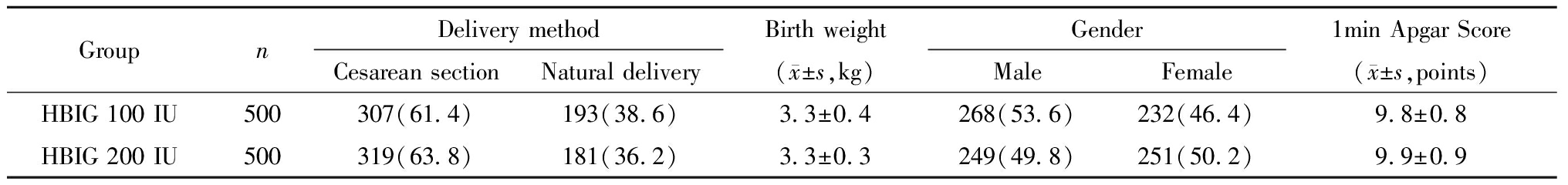
体重、性别、Apgar评分、分娩方式在乙肝免疫球蛋白100 IU组与乙肝免疫球蛋白200 IU组新生儿中的比较,均差异无统计学意义(P>0.05),见表2。
表2 新生儿情况比较[例(%)]
Table 2 Comparison of neonatal conditions[n(%)]
GroupnDelivery methodCesarean sectionNatural deliveryBirth weight(x±s,kg)GenderMaleFemale1min Apgar Score(x±s,points)HBIG 100 IU500307(61.4)193(38.6)3.3±0.4268(53.6)232(46.4)9.8±0.8HBIG 200 IU500319(63.8)181(36.2)3.3±0.3249(49.8)251(50.2)9.9±0.9
三、新生儿抗-HBs水平比较
新生儿抗-HBs水平的两组比较具有时点、组间、时点与组间交互的效应(P<0.05)。乙肝免疫球蛋白200 IU组抗-HBs水平在出生1月、7月高于乙肝免疫球蛋白100 IU组(P<0.05);而出生时抗-HBs水平的组间对比,差异无统计学意义(P>0.05),见表3。
表3 新生儿抗-HBs水平比较![]()
Table 3 Comparison of neonatal anti-HBs ![]()

GroupnAt birth1 months after birth7 months after birthHBIG 100 IU5002.6±0.9250.9±33.7737.2±152.1HBIG 200 IU5002.5±1.0295.8±42.9#764.1±146.3#
Note:Compared with theHBIG 100IU group,#P<0.05。
四、母婴阻断效果比较
乙肝免疫球蛋白200 IU组阻断失败率(3.6%)低于乙肝免疫球蛋白100 IU组(6.6%),抗-HBs阳性率(96.4%)高于乙肝免疫球蛋白100 IU组(93.4%),差异有统计学意义(P<0.05);其余2项阳性评估指标比较,差异无统计学意义(P>0.05),见表4。
表4 母婴阻断效果比较[例(%)]
Table 4 Comparison of mother-infant blocking effect [n(%)]

GroupnHBeAg positiveHBsAg positiveAnti-HBs positiveBlocking failureHBIG 100 IU group50047(9.4)27(5.4)467(93.4)33(6.6)HBIG 200 IU group50034(6.8)15(3.0)482(96.4)#18(3.6)#
Note:Compared with theHBIG 100IU group,#P<0.05。
五、安全性评价
两组妊娠妇女应用替诺福韦时,乙肝免疫球蛋白100 IU组7例(1.4%)出现呕吐,乙肝免疫球蛋白200 IU组3例(0.6%)恶心,6例(1.2%)呕吐,均症状自行缓解,总体治疗耐受性良好,未出现中途终止者。新生儿用药中,未发生药物源性过敏、发热等,乙肝免疫球蛋白100 IU组14例(2.8%)、乙肝免疫球蛋白200 IU组16例(3.2%)出现注射部位略红(χ2=0.137,P=0.711),但1~2 d内均消失,整体用药安全性好。
六、远期随访情况
对两组新生儿出生后实施24个月随访,乙肝免疫球蛋白100 IU组失访9例(1.8%),乙肝免疫球蛋白200 IU组失访11例(2.2%)。随访过程均不存在特殊用药史。HBV DNA阳性:乙肝免疫球蛋白100 IU组15例(3.1%,15/491),乙肝免疫球蛋白200 IU组8例(1.6%,8/489),两组比较差异无统计学意义(χ2=2.152,P=0.142);抗-HBs阳性:乙肝免疫球蛋白100 IU组459例(93.5%,459/491),乙肝免疫球蛋白200 IU组470例(96.1%,470/489),差异无统计学意义(χ2=3.440,P=0.064)。
讨 论
妊娠分娩阶段,母体中带有HBV的分泌物、血液等经过婴儿破损的皮肤粘膜可能会引起感染;胎盘绒毛血管在宫缩状态下可出现破裂,这直接造成母体血液渗入婴儿循环,增加传播危险[9]。资料显示:HBV DNA在分娩时呈高表达是危及传播的重要因素[10]。目前,高病毒载量被认为是HBV母婴传播的高危因素,同时也是HBV母婴阻断失败的一项重要原因。故针对这一特殊人群应尤为关注。且国内外各指南近年来均建议对病毒载量高的孕期妇女给予抗病毒药治疗。但关于婴儿出生后HBIG的应用剂量,各地不一,不同方案的效果也有待评价,尤其对于高病毒载量孕妇,在孕期应用抗病毒药物基础上,是否需要调整HBIG剂量,也有待进一步明确。
近年来国内外指南一并指出通过核苷(酸)类似物进行孕期抗病毒,临床实践颇有成效。如曹香芸等[11]研究表明:替诺福韦组分娩前HBV DNA为(2.89±0.56)IgIU/mL,显著低于用药前[(7.48±1.01)IgIU/mL]。Seo等[12]研究显示治疗后ALT、HBsAg等下降。本研究提示两组在替诺福韦干预下均有HBV DNA、HBeAg、ALT、HBsAg相比基线水平下降的表现,证实了替诺福韦效用。
HBIG是具有高效价特征的被动免疫剂,新生儿注射后有助于获得被动的免疫保护能力,这能够在一定程度上避免乙肝病毒感染。而联合疫苗能够帮助新生儿得到主动的免疫能力,形成保护抗体,达到感染阻断目的[13]。目前,关于HBIG剂量存在较多争议。Wei等[14]研究表明:HBIG100 IU和200 IU组7个月感染率1.5%(8/545)、1.9%(12/632),12个月HBsAg抗体阳性98.5%、97.1%,100 IU剂量足以辅助用于HBV阻断。《中华肝脏病杂志》刊发的一文[15]显示:200 IU HBIG有助于较快建立良好的免疫保护。本研究显示:乙肝免疫球蛋白200 IU组抗-HBs水平在出生1月、7月高于乙肝免疫球蛋白100 IU组,乙肝免疫球蛋白200 IU组阻断失败率(3.6%)低于乙肝免疫球蛋白100 IU组(6.6%),抗-HBs阳性率(96.4%)高于乙肝免疫球蛋白100 IU组(93.4%)。提示应用200 IU HBIG有助于在短期内帮助新生儿得到较好的免疫保护。高载量者传染力相对强,新生儿出生后应尽快给予早期有效的免疫保护,提高抗-HBs抗体水平[16]。资料显示抗-HBs水平维持>100 mIU/mL能够获得较高的安全度[17]。而出生7月时,二组抗-HBs水平也升高,这主要跟新生儿免疫系统得到进一步的完善[18]有关。但随访24个月二组HBV DNA阳性、抗-HBs阳性对比无差异,可能与本次研究纳入样本量有关。本组替诺福韦应用不良反应少,二组无统计差异;且新生儿无药物源性不良反应,提示安全性高。
综上所述,替诺福韦联合200 IU剂量HBIG在乙肝疫苗阻断HBV母婴传播中有助于短期内提高免疫保护及阻断效果,而长期效果与联合100 IU剂量HBIG相当,两种方案均安全可靠,临床可视情况选择100 IU剂量HBIG,减轻患者负担、减少医疗资源浪费。但鉴于抗病毒治疗的普遍和效果认可以及本院对高HBV载量者多数进行抗病毒干预,本次未将无抗病毒干预者纳入研究,今后有待多中心、大样本进行研究。
1 Sheng QJ,Wang SJ,Wu YY,et al.Hepatitis B virus serosurvey and awareness of mother-to-child transmission among pregnant women in Shenyang,China:An observational study.Medicine,2018,97:e10931.
2 Hu P,Ren H.Interpretations of EASL 2017 clinical practice guidelines on the management of hepatitis B virus infection.Chin J Hepatol,2017,25:415-418.
3 中国肝炎防治基金会,中华医学会感染病学分会,中华医学会肝病学分会.乙型肝炎母婴阻断临床管理流程.中华肝脏病杂志,2017,25:254-256.
4 Agarwal K,Brunetto M,Seto W,et al.96 weeks treatment of tenofovir alafenamide vs.tenofovir disoproxil fumarate for hepatitis B virus infection.J hepatol,2018,68:672-681.
5 阴敏,唐亮,姜百灵.富马酸替诺福韦酯治疗HBV感染孕妇的疗效 及垂直传播阻断效果.中华医院感染学杂志,2019,29:3632-3636.
6 周乙华,胡娅莉.预防乙型肝炎母婴传播的乙肝免疫球蛋白合理剂量:100 U单次注射.中华围产医学杂志,2018,21:109-111.
7 段雪飞.中国《慢性乙型肝炎防治指南(2015版)》要点解读.中华全科医师杂志,2016,15:409-412.
8 王亚萍,刘惠媛,石裕明,等.乙型肝炎病毒感染孕妇561例的临床特征及母婴阻断情况.广东医学,2018,39:569-572.
9 陈嵘,黄美玲,凌雪梅,等.替比夫定联合HBIG和乙肝疫苗阻断HBV母婴传播临床效果分析.实用肝脏病杂志,2019,22:752-753.
10 高庆伟,高鹏,丁楠,等.54例高病毒载量乙型肝炎e抗原阳性孕妇抗病毒短期干预的临床安全性及阻断乙型肝炎病毒母婴传播的效果.中国医师进修杂志,2019,42:649-653.
11 曹香芸,管艳萍,李倩,等.替诺福韦、替比夫定分别联合双重免疫方案对HBV母婴传播阻断效果的比较.肝脏,2019,24:503-506.
12 Seo KI,Bae SH,Sung PS,et al.Effect of antiviral therapy in reducing perinatal transmission of hepatitis B virus and maternal outcomes after discontinuing them.Clin Mol Hepatol,2018,24:374-383.
13 张宝芳,程明亮,张权,等.贵州地区HBeAg阳性乙型肝炎病毒高载量孕妇母婴阻断的临床研究.中华肝脏病杂志,2018,26:945-950.
14 Wei KP,Zhu FC,Liu JX,et al.The efficacy of two different dosages of hepatitis B immunoglobulin combined with hepatitis B vaccine in preventing mother-to-child transmission of hepatitis B virus:A prospective cohort study.Vaccine,2018,36:256-263.
15 王翠敏,韩国荣,江红秀,等.不同联合免疫策略对乙型肝炎病毒高载量孕妇所生婴儿抗-HBs水平的影响.中华肝脏病杂志,2015,23:493-497.
16 Fuqiang C,Joseph W,Polin C,et al.Considerations of antiviral treatment to interrupt mother-to-child transmission of hepatitis B virus in China.Int J Epidemiol 2018,47:1529-1537.
17 那妍,娄宪芝,张晓旭,等.乙肝病毒母婴阻断策略中替比夫定的疗效和安全性.中国医科大学学报,2019,48:398-401.
18 Yamashiki N,Yoshizawa A,Ueda Y,et al.The use of hepatitis B immunoglobulin with or without hepatitis B vaccine to prevent de novo hepatitis B in pediatric recipients of anti-HBc-positive livers.Pediatr Transplant,2018,22:e13227.