胎儿染色体核型分析作为产前诊断胎儿染色体异常的经典细胞遗传学方法,可检出染色体数目和结构异常,但对小于5 Mb的拷贝数变异(copy number variations,CNVs)却无法识别,而CNVs是许多发育障碍的重要遗传原因[1],染色体微阵列分析(chromosomal microarray analysis, CMA)中的单核苷酸多态性微阵列技术(single nucleotide polymorphism array, SNP-Array)已被认为是智障或多种先天性异常患者的首选检测方案[2],其不仅能识别非整倍体、三倍体和单亲二倍体,还能识别小于5 Mb的CNVs,但其对染色体结构异常和低比例嵌合却不及核型分析能稳定检出[3],SNP-Array技术可补充核型分析,提高了胎儿染色体异常检出率,对于预防和控制出生缺陷是有效的[4-5]。本文回顾性分析1 317例具有产前诊断指征的高危孕妇胎儿行G显带核型分析联合SNP-Array技术,分析其染色体结果及妊娠结局,以探讨其诊断价值。
资料与方法
一、一般资料
回顾性分析2018年8月至2020年5月因具有高龄、血清学筛查高风险、不良孕史、超声异常、夫妇染色体异常等产前诊断指征的1 317例高危孕妇,血清学筛查分为无创产前检测和唐氏综合症产前筛查,超声异常分为超声软指标阳性、超声结构异常、生长受限和羊水量异常,超声软指标包括脑室扩张、颅后窝池扩张、脉络丛囊肿、颈部透明层(nuchal translucency, NT)、颈后皮肤皱褶(nuchal fold, NF)、鼻骨发育不良、小脑发育不良、心内强回声灶、强回声肠管、胸腔积液、轻度肾盂扩张、胆囊增大、胃泡显示不清或偏小、长骨短、单脐动脉、脐带囊肿[6]。为排除其他指标干扰,特研究孤立性指标,以探讨其临床价值。孕妇及家属签署知情同意书后行介入性产前诊断穿刺术,取羊水或脐带血行SNP-array检测和G显带核型分析,孕妇年龄17~48周岁,平均(30.5±5.5)周岁;孕周17~34周,平均(22.7±4.5)周。
二、方法
1.介入性产前诊断穿刺术:因高龄、血清学高危、超声异常、不良孕史、夫妇染色体异常等之一或多项产前诊断指征的孕妇均行核型及SNP-array检测,孕17~24周行羊膜腔穿刺术,取羊水20 mL行G显带核型分析,10 mL行SNP-array检测;孕25周以后孕妇行脐带血穿刺术1 mL行G显带核型分析,0.5 mL行SNP-array检测。
2.G显带核型分析:常规37℃培养箱培养羊水5~6 d换液、隔天观察、择时收获、制片、G显带;37℃培养箱培养脐带血72 h、收获、制片、G显带,核型分析依据2016年染色体核型分析命名体制(International System for Human Cytogenetic Nomenclature, ISCN),常规细胞计数20个,如为嵌合核型计数100个,分析5个分散良好的染色体核型。核型异常指染色体数目或结构异常,不含多态性。
3.SNP-array检测:采用Affymetrix Cytoscan 750K Array(美国Affymetrix公司)进行全基因组芯片检测,提取DNA、片段化、标记信号、杂交及扫描,芯片仪读取数据应用ChAS4.0软件分析结果。依据CNVs位置、大小、DGV数据库、ISCA数据库、Decipher数据库、Clingen数据库报道等将结果分为致病性变异、可能致病变异、临床意义不明、可能良性变异、良性变异。SNP-Array异常指致病性变异、可能致病性变异、临床意义不明。
4.妊娠结局的随访:对所有孕妇分娩后4~6个月进行电话随访,了解妊娠结局和新生儿生长发育情况,针对染色体异常而选择分娩的婴儿于1岁左右进行追踪随访。
5.统计学处理:应用SPSS21.0统计软件,组间比较采用卡方检验、Fisher确切概率法,P<0.05为差异有统计学意义。
结 果
一、核型与SNP-Array检测结果
在1 317例胎儿染色体中,核型多态性44例(3.3%,44/1 317),核型异常152例(152/1 317,11.5%),SNP-Array异常241例(241/1 317,18.3%),两种检测比较,差异有统计学意义。152例核型异常中21-三体42例、18-三体10例(包括1例超雌)、13-三体3例、特纳12例、超雌12例(包括1例18-三体)、克氏17例、超雄10例、48,XXYY 1例、易位22例(包括1例倒位)、增加6例、缺失5例、衍生4例、倒位3例(包括1例易位)、额外标记染色体2例、重复1例、插入1例、其他2例。241例SNP-Array检测异常中致病性变异146例、可能致病性变异42例、临床意义不明53例,其中重复56例(片段206~82 900 kb)、缺失79例(片段104~53 900 kb)、杂合性丢失18例(片段3 100~32 630 kb)。
核型异常152例(152/1 317,11.5%),SNP-Array异常241例(241/1 317,18.3%)。两种检测联合应用染色体异常270例(270/1 317,20.5%),与核型异常检出率比较,差异有统计学意义。
核型与SNP-Array均异常123例(123/1 317,9.3%),其中致病性变异109例、可能致病性变异12例、临床意义不明2例,其中重复11例(片段3 420~82 900 kb),缺失18例(片段725~53 900 kb);核型正常中SNP-Array异常110例(110/1 121,9.8%),其中致病性变异35例、可能致病性变异28例、临床意义不明47例,其中重复42例(片段206~23 300 kb),缺失55例(片段104~12 070 kb),杂合性丢失18例(片段3 100~32 630 kb);SNP-Array正常中核型异常31例(31/1 076,2.9%),其中小于5%低比例嵌合3例,额外标记染色体1例,附加、易位、倒位、衍生、插入等27例。
二、核型与SNP-Array结果不符情况
1 121例核型正常胎儿中SNP-Array异常110例;1 076例SNP-Array正常胎儿中核型异常31例;123例两种检测均异常胎儿中结果不符4例,病例1核型为45,XN,der(13;14)(q10;q10),SNP-Array结果为1q21.1q21.2缺失;病例2核型为46,XN,13q?,SNP-Array结果为22q11.21q11.21缺失1.084Mb;病例3核型为46,XN,add(8)(p23)pat,SNP-Array结果为8p23.3p23.1缺失8.68Mb,足月顺产,随访至11个月发育未见异常;病例4核型为46,XN,add(21)(p13),SNP-Array结果为22q13.1q13.33重复。产前诊断指征与核型、CNVs相关性。
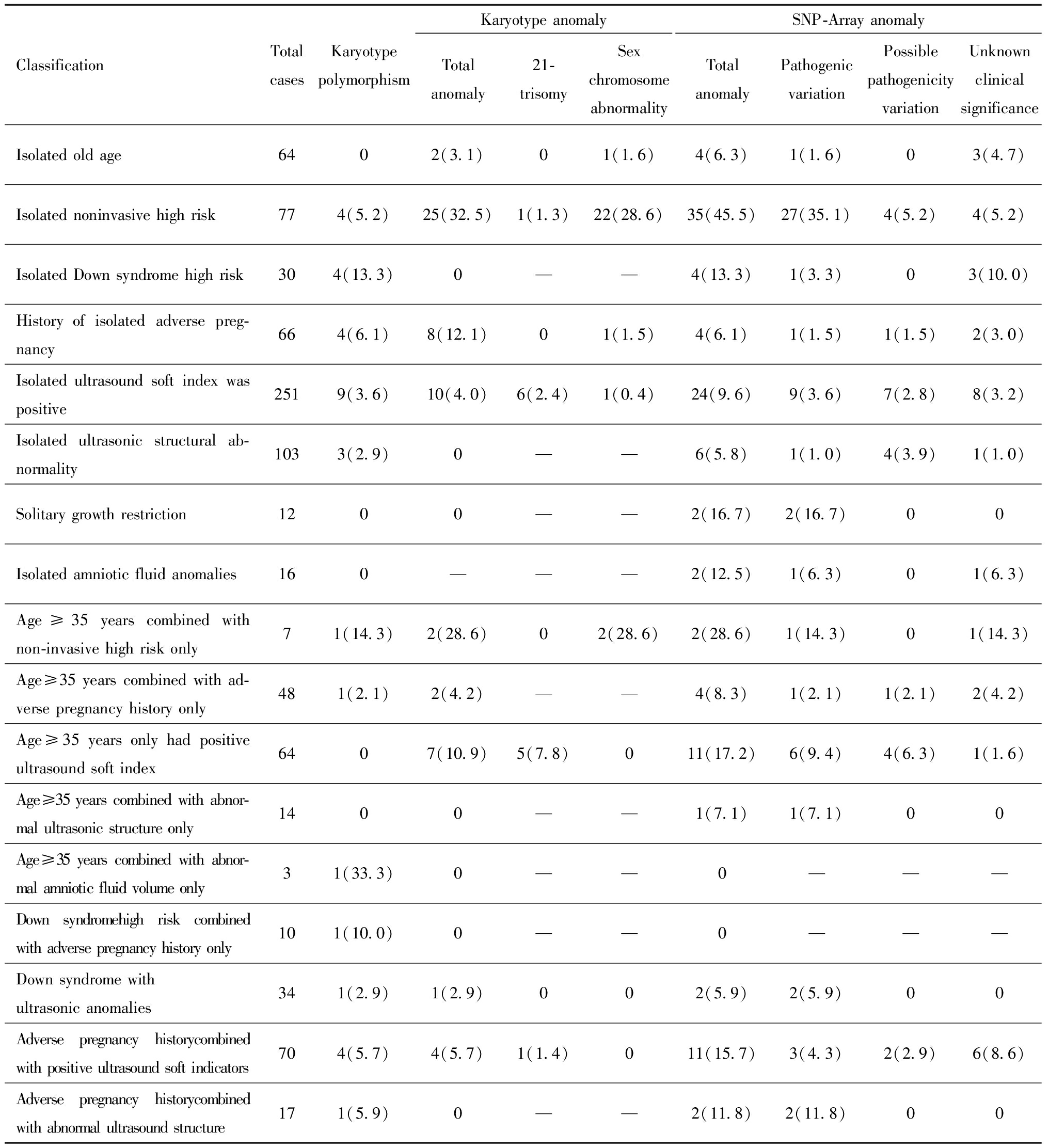
剔除其他高危因素,孤立性产前诊断指标中无创高危组核型与SNP-Array异常率最高。合并两类指标中,高龄仅合并无创高危组的胎儿核型及SNP-Array异常率最高。见表1。
表1 产前诊断指征与核型、CNVs相关性分析[例(%)]
Table 1 Correlation analysis of prenatal diagnostic indications with karyotype and CNVs[n(%)]
ClassificationTotalcasesKaryotypepolymorphismKaryotype anomalyTotal anomaly21- trisomySex chromosomeabnormalitySNP-Array anomalyTotalanomalyPathogenic variationPossible pathogenicity variationUnknown clinical significanceIsolated old age6402(3.1)01(1.6)4(6.3)1(1.6)03(4.7)Isolated noninvasive high risk774(5.2)25(32.5)1(1.3)22(28.6)35(45.5)27(35.1)4(5.2)4(5.2)Isolated Down syndrome high risk304(13.3)0——4(13.3)1(3.3)03(10.0)History of isolated adverse preg-nancy664(6.1)8(12.1)01(1.5)4(6.1)1(1.5)1(1.5)2(3.0)Isolated ultrasound soft index was positive2519(3.6)10(4.0)6(2.4)1(0.4)24(9.6)9(3.6)7(2.8)8(3.2)Isolated ultrasonic structural ab-normality1033(2.9)0——6(5.8)1(1.0)4(3.9)1(1.0)Solitary growth restriction1200——2(16.7)2(16.7)00Isolated amniotic fluid anomalies160———2(12.5)1(6.3)01(6.3)Age≥35 years combined with non-invasive high risk only71(14.3)2(28.6)02(28.6)2(28.6)1(14.3)01(14.3)Age≥35 years combined with ad-verse pregnancy history only481(2.1)2(4.2)——4(8.3)1(2.1)1(2.1)2(4.2)Age≥35 years only had positive ultrasound soft index6407(10.9)5(7.8)011(17.2)6(9.4)4(6.3)1(1.6)Age≥35 years combined with abnor-mal ultrasonic structure only1400——1(7.1)1(7.1)00Age≥35 years combined with abnor-mal amniotic fluid volume only31(33.3)0——0———Down syndromehigh risk combined with adverse pregnancy history only101(10.0)0——0———Down syndrome with ultrasonic anomalies341(2.9)1(2.9)002(5.9)2(5.9)00Adverse pregnancy historycombined with positive ultrasound soft indicators704(5.7)4(5.7)1(1.4)011(15.7)3(4.3)2(2.9)6(8.6)Adverse pregnancy historycombined with abnormal ultrasound structure171(5.9)0——2(11.8)2(11.8)00
三、孕龄与核型、CNVs相关性
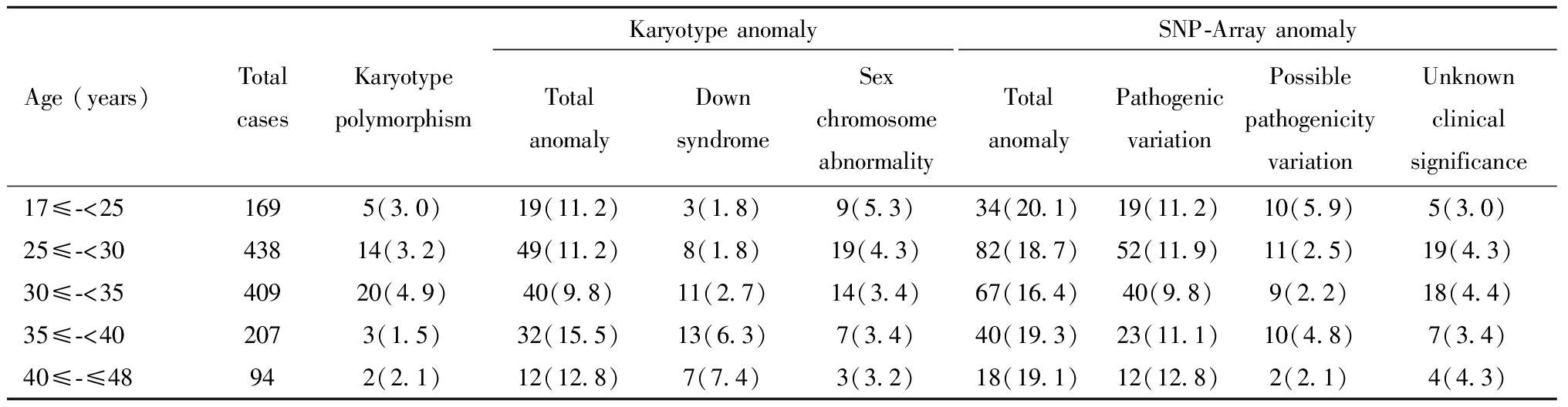
依据孕妇年龄分组,相关分析显示,21-三体发生率与年龄之间Pearson相关性(系数=0.901),显著性(双侧,系数=0.037)。进一步采用一元线性回归分析,年龄为自变量,21-三体发生率为因变量,系数=0.950,R2=0.902,F=37.007,P=0.004,说明21-三体发生率与年龄呈正相关,但年龄分组中CNVs与年龄没有相关性,见表2。
表2 年龄与核型、CNVs相关性分析[例(%)]
Table 2 Correlation analysis of age with karyotype and CNVs[n(%)]
Age (years)Total casesKaryotype polymorphismKaryotype anomalyTotal anomalyDown syndromeSex chromosome abnormalitySNP-Array anomalyTotal anomalyPathogenic variationPossible pathogenicity variationUnknown clinical significance17≤-<251695(3.0)19(11.2)3(1.8)9(5.3)34(20.1)19(11.2)10(5.9)5(3.0)25≤-<3043814(3.2)49(11.2)8(1.8)19(4.3)82(18.7)52(11.9)11(2.5)19(4.3)30≤-<3540920(4.9)40(9.8)11(2.7)14(3.4)67(16.4)40(9.8)9(2.2)18(4.4)35≤-<402073(1.5)32(15.5)13(6.3)7(3.4)40(19.3)23(11.1)10(4.8)7(3.4)40≤-≤48942(2.1)12(12.8)7(7.4)3(3.2)18(19.1)12(12.8)2(2.1)4(4.3)
四、不良孕史与核型、CNVs相关性
剔除其他高危因素,将不良孕史分为21-三体生育史、胎停育史和其他组,孤立性胎停育史组的胎儿核型异常率最高,其他不良孕史合并超声软指标阳性组SNP-Array异常率最高,孤立性21-三体生育史组的胎儿未检出染色体异常,见表3。
表3 不良孕史与核型、CNVs相关性分析[例(%)]
Table 3 Correlation analysis of adverse pregnancy history with karyotype and CNVs[n(%)]

ClassificationTotal casesKaryotype polymorphismKaryotype anomalyTotal anomalyDown syndromeSex chromosome abnormalitySNP-Array anomaly Total anomalyPathogenic variationPossible pathogenicity variationUnknown clinical significanceHistory of solitary trisomy 2181(12.5)0000000History of solitary abortive birth1904(21.1)001(5.3)01(5.3)0Isolated history of other adverse pregnancies423(7.1)4(9.5)01(2.4)3(7.1)1(2.4)02(4.8)21 Fertility history was only combined with positive ultrasound soft indicators122(16.7)1(8.3)——0———The history of fetal stop was only associated with positive ultrasound soft indicators3004(13.3)——2(6.7)—1(3.3)1(3.3)Other adverse pregnancy history combined with positive ultrasound soft indicators946(6.4)7(7.5)1(1.1)1(1.1)13(13.8)4(4.3)2(2.1)7(7.5)
五、超声软指标类型及超声异常数目与核型、CNVs相关性
在孤立性超声软指标阳性组中,SNP-Array共检出24例染色体异常,其中致病性变异共9例,为5例21-三体,1例18-三体,1例Y与X染色体比例异常(嵌合比例30%),1例Xq28重复和1例22q13.1q13.33重复;可能致病性变异7例,临床意义不明8例。
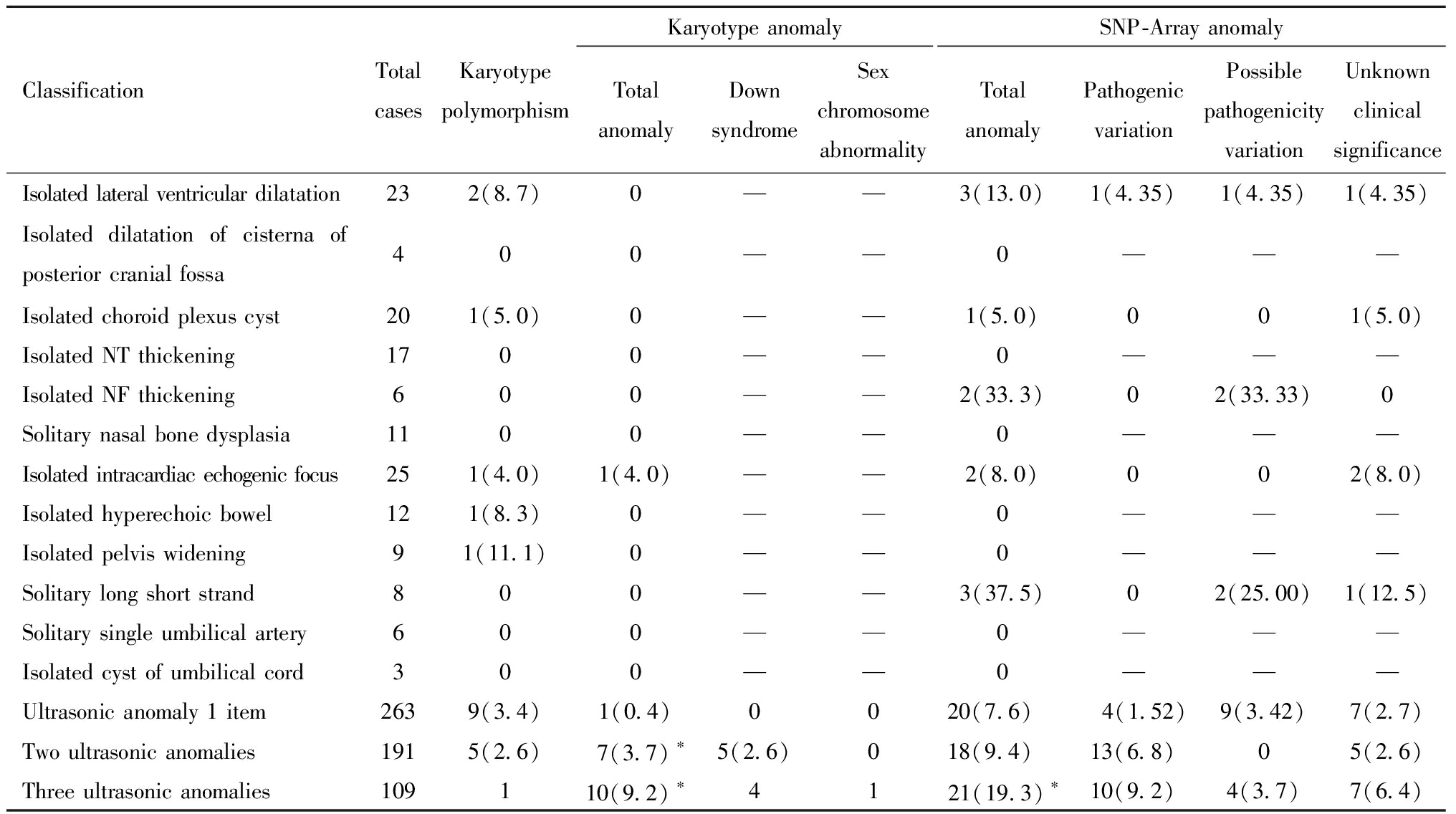
剔除其他高危因素,在孤立性超声软指标阳性分组中,核型分析仅孤立性心内强回声灶的胎儿检出染色体异常[46,XN,ins(13;4)(q22;q31q35)],SNP-Array检测孤立性长骨短的胎儿染色体异常率最高,其次依次是孤立性NF增厚、孤立性侧脑室扩张。剔除其他高危因素,仅超声异常组中随超声异常数目增加,核型和SNP-Array染色体异常率随之升高,差异有统计学意义,见表4。
表4 超声软指标类型及超声异常数目与核型、CNVs相关性分析[例(%)]
Table 4 Correlation analysis of the types of ultrasonic soft indexes and the number of ultrasonic anomalies with karyotype and CNVs[n(%)]
ClassificationTotal casesKaryotype polymorphismKaryotype anomalyTotal anomalyDown syndromeSex chromosome abnormalitySNP-Array anomaly Total anomalyPathogenic variationPossible pathogenicity variationUnknown clinical significanceIsolated lateral ventricular dilatation232(8.7)0——3(13.0)1(4.35)1(4.35)1(4.35)Isolated dilatation of cisterna of posterior cranial fossa400——0———Isolated choroid plexus cyst201(5.0)0——1(5.0)001(5.0)Isolated NT thickening1700——0———Isolated NF thickening600——2(33.3)02(33.33)0Solitary nasal bone dysplasia1100——0———Isolated intracardiac echogenic focus251(4.0)1(4.0)——2(8.0)002(8.0)Isolated hyperechoic bowel121(8.3)0——0———Isolated pelvis widening91(11.1)0——0———Solitary long short strand800——3(37.5)02(25.00)1(12.5)Solitary single umbilical artery600——0———Isolated cyst of umbilical cord300——0———Ultrasonic anomaly 1 item2639(3.4)1(0.4)0020(7.6) 4(1.52)9(3.42)7(2.7)Two ultrasonic anomalies1915(2.6)7(3.7)∗5(2.6)018(9.4) 13(6.8)05(2.6)Three ultrasonic anomalies109110(9.2)∗4121(19.3) ∗10(9.2)4(3.7)7(6.4)
Compared with ultrasound abnormality 1, *P<0.05
六、12例胎儿SNP-Array异常父母验证结果及妊娠结局
父母验证的SNP-Array异常胎儿中7例来源于父母,父母表型均正常,其中1例因足内翻选择终止妊娠,其他均顺利分娩,随访至1周岁左右发育未见异常。另外5例SNP-Array异常胎儿为新发变异,其中1例胎儿核型及FISH均正常,SNP-Array为可能致病性变异,父母验证SNP-Array均正常,临床遗传咨询后选择继续妊娠后顺利分娩,随访至1岁6个月,发育未见异常,其他4例均选择终止妊娠。
讨 论
单核苷酸多态性是指基因组中DNA某一特定核苷酸位置上发生转换、颠换、插入或缺失等变化,而且任何一种等位基因在群体中的频率不小于1%[7]。CMA是一种以微阵列为技术基础的高分辨率全基因组染色体变异检测技术,近年来在临床已广泛应用。相比于基于微阵列的比较基因组杂交(array-based comparative genomic hybridization,aCGH)和低深度全基因组测序(CNV-seq)技术,SNP-Array技术对于染色体非整倍体和拷贝数变异的检测与aCGH和CNV-seq技术相当,但对于单亲二倍体、三倍体和一定比例嵌合体的检测优势更为突出,而且CNV-seq测序深度低有可能会漏检,SNP-Array以高分辨率、高准确性的优点,与传统核型分析联合应用可以更好地指导临床遗传咨询[8]。
任何单一的产前诊断检测方法均有漏检或误检的可能,本研究中,SNP-Array的异常检出率(18.3%)相比核型分析的异常检出率(11.5%)提高了26.8%,两者联合应用的染色体异常检出率达到20.5%。若仅行核型分析而不进行SNP-Array检测,其染色体异常漏检率达9.8%,包括致病性变异35例,可能致病28例。而若仅行SNP-Array检测而不进行核型分析,其染色体异常漏检率达2.9%,包括小于5%低比例嵌合3例,额外标记染色体1例,附加、易位、倒位、衍生、插入等27例,需结合SNP-Array结果方能进行更精准的遗传咨询,若SNP-Array没有致病性CNVs,可以考虑继续妊娠。123例两种检测均异常胎儿中结果不符4例,其中1例核型示46,XN,add(8)(p23)pat,SNP-Array示8p23.3p23.1缺失8.68 Mb,由此分析核型提示8号染色体增加未知起源遗传物质,有可能是多态性变异,因没有引起拷贝数变异,故SNP-Array无法识别,但检出8号染色体p23.3p23.1区段存在约8.68 Mb的缺失,根据DGV、ISCA、Decipher与Clingen数据库综合分析,该片段为可能致病性变异[9],经SNP-Array夫妇验证,缺失片段来源于父亲,但父亲表型正常,经过深度遗传咨询,夫妇决定保留胎儿,该婴儿足月顺产,出生后6个月及11个月随访婴儿身体及智力发育均未见异常。另1例核型示46,XN,13q?,SNP-Array示22q11.21微缺失,由此分析核型提示13号染色体长臂可疑异常,也有可能是多态性变异,没有引起拷贝数变异,故SNP-Array未检出,而SNP-Array提示22号染色体缺失1.084 Mb,可能致病性变异,核型未检出,也补充了结果,建议夫妇验证,但孕妇及家属选择终止妊娠未验证。而另1例核型示46,XN,add(21)(p13),SNP-Array示22q13.1q13.33微重复,由此分析是22号染色体微重复的部分到了21号染色体。由此可见,SNP-Array技术较核型分析染色体异常检出率高,两者联合应用可弥补各自不足,提高染色体异常检出率,核型结果与SNP-Array结果相互补充,可以更精准的分析染色体异常,有利于临床咨询及再生育指导[10-11]。
剔除其他高危因素,本研究中,探讨孤立性产前诊断指标对胎儿染色体的影响,其中孤立性无创高危组核型与SNP-Array异常率最高,尤其SNP-Array可检出核型不可识别的CNVs,可见,核型联合SNP-Array在无创高危孕妇的产前诊断中体现出较高的临床应用价值[12-13]。在年龄分组中,21-三体发生率与年龄呈正相关,而孤立性高龄组SNP-Array检测致病性变异检出率仅为1.6%,年龄分组中CNVs与年龄没有相关性,可见SNP-Array检测应涉及到所有年龄段的高危孕妇[14]。
在孤立性不良孕史中,孤立性胎停育史组的胎儿核型异常率最高,其他不良孕史合并超声软指标阳性组SNP-Array异常率最高,而染色体异常是胎停育的最常见原因,具有胎停育史的孕妇其胎儿再次患染色体异常的发生率仍较高[15-17]。而孤立性21-三体生育史组的胎儿未检出染色体异常,因剔除其他高危因素,可能与样本量较少有关,还需扩大样本量进一步研究。
在孤立性超声软指标阳性组中,SNP-Array共检出24例染色体异常,其中致病性变异共9例,为5例21-三体,1例18-三体,1例Y与X染色体比例异常(嵌合比例30%),1例Xq28重复和1例22q13.1q13.33重复;可能致病性变异7例,临床意义不明8例。在超声软指标分组中,核型分析仅孤立性心内强回声灶的胎儿检出染色体异常,为46,XN,ins(13;4)(q22;q31q35),可见心内强回声灶仍不排除染色体异常可能。其他孤立性超声软指标核型分析没有检出染色体异常,但SNP-Array却能检出CNVs,其中SNP-Array检测孤立性长骨短的胎儿染色体异常率最高,其次依次是孤立性NF增厚、孤立性侧脑室扩张,且随超声异常数目增加,核型和SNP-Array染色体异常率随之升高。早在2013年CMA就已经被美国妇产科医师学会和母胎医学协会推荐作为超声结构畸形胎儿的首选技术应用于产前诊断,可见,超声异常尤其是超声软指标阳性的胎儿其染色体异常的发生率较高,传统核型分析存在局限性,SNP-Array检测已成为超声异常胎儿产前诊断首选一级检测方案[18-19],而SNP-Array检测异常后应父母加以验证,但因SNP-Array费用较高,无法普及。本研究中父母SNP-Array验证的异常胎儿中7例来源于父母,父母表型均正常,其中1例因足内翻选择终止妊娠,其他均顺利分娩,随访至1周岁左右发育未见异常。另外5例SNP-Array异常胎儿为新发变异,其中1例胎儿核型及FISH均正常,SNP-Array为可能致病性变异,父母验证SNP-Array均正常,临床遗传咨询后选择继续妊娠后顺利分娩,随访至1周6个月,发育未见异常,其他4例均选择终止妊娠。可见,染色体异常胎儿应双亲验证并结合进一步连续超声检查及遗传咨询,以指导孕妇是否继续妊娠。
综上所述,21-三体发生率与年龄呈正相关,无创高危、胎停育史、长骨短、NF增厚和侧脑室扩张提示染色体异常风险升高,心内强回声灶仍不排除染色体异常的可能,遗传咨询中双亲验证后的家系综合分析仍十分重要,核型分析联合SNP-Array技术可提高染色体异常检出率,核型结果与SNP-Array结果相互补充,可以更精准的分析染色体异常,有利于遗传咨询及再生育指导,是高危孕妇胎儿首选的产前诊断方案。
1 Hu P,Wang Y,Sun R,et al.Copy Number Variations with Isolated Fetal Ventriculomegaly.Curr Mol Med,2017,17:133-139.
2 Cheung SW,Bi W.Novel applications of array comparative genomic hybridization in molecular diagnostics.Expert Rev Mol Diagn,2018,18:531-542.
3 Xiang J,Ding Y,Song X,et al.Clinical Utility of SNP Array Analysis in Prenatal Diagnosis:A Cohort Study of 5000 Pregnancies.Front Genet,2020,11:571219.
4 Cai M,Lin N,Lin Y,et al.Evaluation of chromosomal abnormalities and copy number variations in late trimester pregnancy using cordocentesis.Aging(Albany NY),2020,12:15556-15565.
5 Huang H,Cai M,Wang Y,et al.SNP Array as a Tool for Prenatal Diagnosis of Congenital Heart Disease Screened by Echocardiography:Implications for Precision Assessment of Fetal Prognosis.Risk Manag Healthc Policy,2021,14:345-355.
6 李胜利,罗国阳.胎儿畸形产前超声诊断学(第2版).北京:科学出版社,2017,6:899-919.
7 汪维鹏,倪坤仪,周国华.单核苷酸多态性检测方法的研究进展.遗传,2006,28:117-126.
8 王曲悠,胡婷,陈林,等.基于二代测序技术的基因组拷贝数变异检测在产前诊断中的应用.中华医学遗传学杂志,2022,39:949-953.
9 陈新英,潘汉斌,曾书红,等.罕见的8p部分缺失伴重复患儿1例的临床及遗传学分析.中华医学遗传学杂志,2023,40:96-100.
10 史珊珊,潘观玉,杨艳东,等.应用SNP array诊断一例5p缺失综合征合并11q部分三体胎儿.中华医学遗传学杂志,2016,33:195-199.
11 郭依琳,王莉,薛淑文,等.SNP-array技术应用于超声检查异常胎儿产前诊断的研究.中华妇产科杂志,2018,53:464-470.
12 赵军红,代鹏,朱若男,等.2 398例孕妇外周血游离胎儿DNA产前筛查阳性结果的验证与分析.中华妇产科杂志,2020,55:679-684.
13 卜秀芬,曾黎,李红玉,等.染色体微阵列分析对于无创产前检测提示异常的孕妇的诊断价值.中华医学遗传学杂志,2021,38:541-544.
14 Lin YH,Jong YJ,Huang PC,et al.Detection of copy number variants with chromosomal microarray in 10 377 pregnancies at a single laboratory.Acta Obstet Gynecol Scand,2020,99:775-782.
15 余宏盛,郭红,沈双双,等.染色体核型分析联合SNP-array技术在不良妊娠史孕妇产前诊断中的应用.中华妇产科杂志,2018,53:155-159.
16 Qu S,Wang L,Cai A,et al.Exploring the cause of early miscarriage with SNP-array analysis and karyotyping.J Matern Fetal Neonatal Med,2019,32:1-10.
17 Mao J,Wang H,Li H,et al.Genetic analysis of products of conception using a HLPA/SNP-array strategy.Mol Cytogenet,2019,12:40.
18 Srebniak MI,Diderich KE,Joosten M,et al.Prenatal SNP array testing in 1000 fetuses with ultrasound anomalies:causative,unexpected and susceptibility CNVs.Eur J Hum Genet,2016,24:645-651.
19 Wang J,Zhang Z,Li Q,et al.Prenatal diagnosis of chromosomal aberrations by chromosomal microarray analysis in foetuses with ventriculomegaly.Sci Rep,2020,10:20765.